Clear Sky Science · pl
Fosforan sfingozyny-1 promuje wyczerpanie limfocytów T CD8 w raku piersi poprzez egzosomalny transfer TGFBR2
Dlaczego to ma znaczenie dla leczenia raka
Wiele nowoczesnych terapii przeciwnowotworowych ma na celu uwolnienie własnego układu odpornościowego organizmu, zwłaszcza cytotoksycznych limfocytów T CD8, by atakowały guzy. Jednak w wielu rakach piersi te komórki stają się zmęczone i nieskuteczne — stan znany jako wyczerpanie — a immunoterapia często działa tylko umiarkowanie. Badanie to ujawnia wcześniej ukryty sposób, w jaki guzy piersi „usztywniają” chemicznie limfocyty T CD8 na odległość, pokazując nową ścieżkę sygnałową, którą można by zablokować, aby pomóc istniejącym immunoterapiom działać lepiej.
Tłuszczowa cząsteczka, która kształtuje mikrośrodowisko guza
Naukowcy skupili się na fosforanie sfingozyny-1 (S1P), cząsteczce sygnałowej o tłuszczowej naturze występującej w wysokim stężeniu w raku piersi. Wiadomo już, że S1P sprzyja tworzeniu naczyń krwionośnych w guzach, ich rozprzestrzenianiu się i oporności na leczenie. W tym badaniu zespół sprawdził, czy S1P także pomaga guzom unieszkodliwiać limfocyty T CD8 w ich otoczeniu. Kiedy hodowano ludzkie komórki raka piersi z S1P, a następnie współhodowano je z ludzkimi limfocytami T CD8, komórki T dzieliły się znacznie mniej, nawet gdy nie mogły się fizycznie kontaktować z komórkami nowotworowymi. Ta supresja bez kontaktu zasugerowała, że komórki guza uwalniają jakiś rodzaj cząstek przenoszących komunikaty do pożywki.
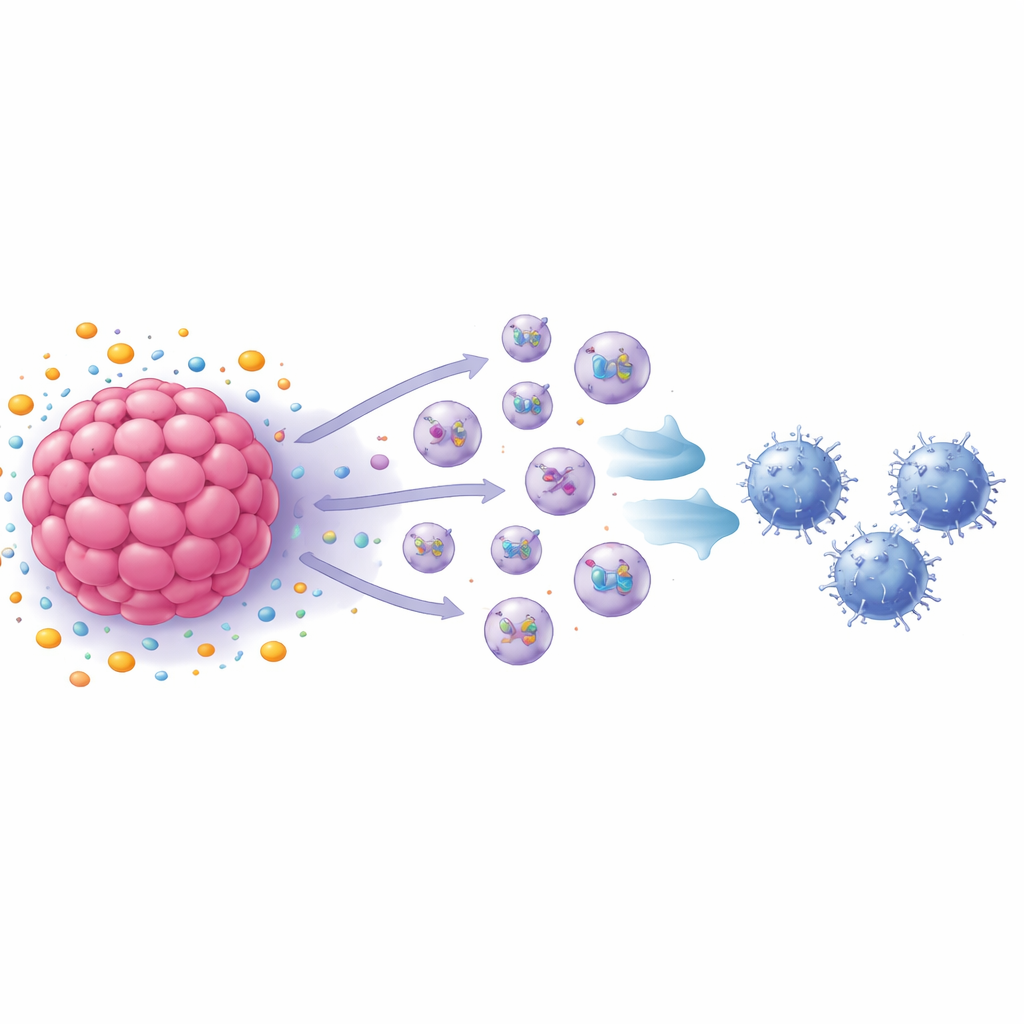
Maleńkie pęcherzyki jako posłańcy supresji odporności
Zespół zwrócił następnie uwagę na egzosomy — nanometrowe pęcherzyki uwalniane przez komórki, które przenoszą białka i inne molekuły do odległych celów. Zablokowanie produkcji egzosomów w dużej mierze przywróciło wzrost limfocytów T CD8, a analiza wykazała, że komórki raka piersi traktowane S1P wydzielały znacznie więcej egzosomów niż komórki nietraktowane. Gdy te egzosomy dodano bezpośrednio do aktywowanych limfocytów T CD8, komórki T spowalniały proliferację i zaczynały wykazywać cechy wyczerpania, w tym kilka markerów powierzchniowych i wewnętrznych związanych ze „zmęczonymi” komórkami odpornościowymi. W eksperymentach na zwierzętach egzosomy z komórek raka piersi myszy traktowanych S1P przyspieszały wzrost guza i zwiększały odsetek wyczerpanych limfocytów T CD8 w guzach, podczas gdy egzosomy z komórek pozbawionych kluczowego receptora działały odwrotnie.
Receptor zawarty w egzosomach wyrządza szkodę
Analizując, co czyni te egzosomy tak szkodliwymi, naukowcy zbadali białka związane z układem odpornościowym wzbogacone w ich ładunku. Stwierdzili, że jedno białko — receptor transformującego czynnika wzrostu beta 2 (TGFBR2) — było wyraźnie zwiększone na egzosomach po leczeniu S1P, podczas gdy inny dobrze znany białkowy punkt kontrolny, PD-L1, nie był. Egzosomy łączyły się z limfocytami T CD8 i dostarczały TGFBR2 na powierzchnię komórek T, skutecznie wyposażając je w dodatkową kopię receptora, który uruchamia programy prowadzące do wyczerpania wewnątrz komórki. Gdy zespół zablokował TGFBR2 na egzosomach przeciwciałem lub zmniejszył jego poziom w komórkach nowotworowych, egzosomy nie mogły już tłumić aktywności komórek T ani indukować markerów wyczerpania, a limfocyty T CD8 odzyskały zdolność do produkcji kluczowych cząsteczek efektornych.
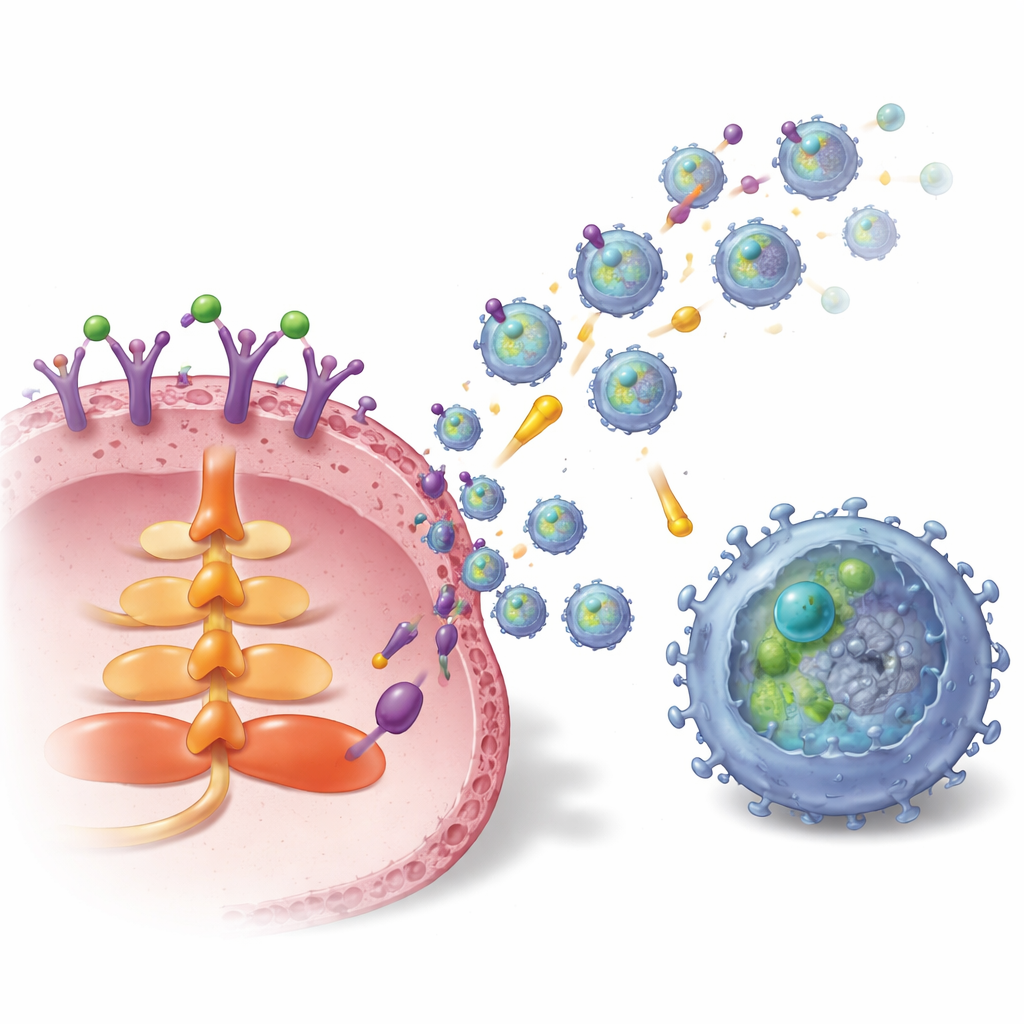
Jak guz ładuje i wysyła te pęcherzyki
Badanie następnie odwzorowało wewnętrzne połączenia łączące S1P z produkcją egzosomów i pakowaniem TGFBR2. Aktywacja konkretnego receptora S1P na komórkach raka piersi, zwanego S1P1, włączała szlak sygnałowy AKT i białko ruchu Rab27a, z których oba są kluczowe dla uwalniania egzosomów. Równocześnie S1P1 zwiększał ilość i stabilność TGFBR2 w komórkach nowotworowych. Działo to na dwa sposoby: po pierwsze poprzez uruchomienie czynnika transkrypcyjnego LEF1, który podnosi ekspresję genu TGFBR2, a po drugie przez podwyższenie poziomów deubikwitynazy USP8 za pośrednictwem szlaku ERK–CREB1. USP8 spowalnia rozkład TGFBR2, pozwalając na zgromadzenie większej liczby receptorów i ich zapakowanie do egzosomów. W próbkach guzów piersi od pacjentów zarówno S1P1, jak i TGFBR2 występowały w większym nasileniu w tkance guza i w egzosomach pochodzących z guza niż w sąsiedniej tkance prawidłowej, a wyższy poziom TGFBR2 na egzosomach korelował z większą liczbą wyczerpanych limfocytów T CD8.
Co to oznacza dla pacjentów
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że niektóre raki piersi tworzą chemiczne środowisko bogate w S1P, które instruuje komórki guza, by wypuszczały maleńkie pęcherzyki naładowane receptorem TGFBR2, wyłączającym limfocyty T CD8. Te pęcherzyki działają jak ukryte przesyłki, które przeprogramowują pobliskie komórki zabójcze, czyniąc je ospałymi i tolerancyjnymi wobec guza. Wskazanie łańcucha zdarzeń S1P–S1P1–TGFBR2, w tym wewnętrznych przełączników kontrolujących uwalnianie egzosomów i gromadzenie receptorów, sugeruje kilka nowych celów terapeutycznych. Hamowanie sygnalizacji S1P, blokada S1P1 lub uniemożliwienie docierania lub stabilizacji TGFBR2 na egzosomach mogłoby zmniejszyć wyczerpanie limfocytów T CD8 i uczynić istniejące immunoterapie bardziej skutecznymi dla pacjentów z rakiem piersi.
Cytowanie: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Słowa kluczowe: immunoterapia raka piersi, wyczerpanie limfocytów T CD8, fosforan sfingozyny-1, egzosomy, sygnalizacja TGFBR2