Clear Sky Science · it
La sfingosina-1-fosfato promuove l’esaurimento delle cellule T CD8 nel carcinoma mammario tramite trasferimento esosomico di TGFBR2
Perché è importante per il trattamento del cancro
Molte terapie oncologiche moderne puntano a liberare il sistema immunitario dell’organismo, in particolare le cellule T CD8 citotossiche, per attaccare i tumori. Tuttavia, in molti carcinomi mammari queste cellule diventano affaticate e inefficaci, uno stato noto come esaurimento, e l’immunoterapia spesso funziona solo in modo modesto. Questo studio rivela un meccanismo finora nascosto con cui i tumori mammari “sedano” chimicamente le cellule T CD8 a distanza, svelando una nuova via di segnalazione che potrebbe essere bloccata per migliorare l’efficacia delle immunoterapie esistenti.
Una molecola lipidica che modella il microambiente tumorale
I ricercatori si sono concentrati sulla sfingosina-1-fosfato (S1P), una molecola segnalatrice simile a un lipide presente a livelli elevati nel carcinoma mammario. S1P è già nota per favorire la crescita dei vasi tumorali, la diffusione e la resistenza alle terapie. In questo lavoro il team si è chiesto se S1P aiuti anche i tumori a disarmare le cellule T CD8 nel loro intorno. Quando hanno coltivato cellule di carcinoma mammario umano con S1P e le hanno poi co-coltivate con cellule T CD8 umane, le T hanno proliferato molto meno, anche quando non potevano toccare fisicamente le cellule tumorali. Questa soppressione senza contatto suggeriva che le cellule tumorali rilasciassero nel mezzo particelle in grado di veicolare messaggi.
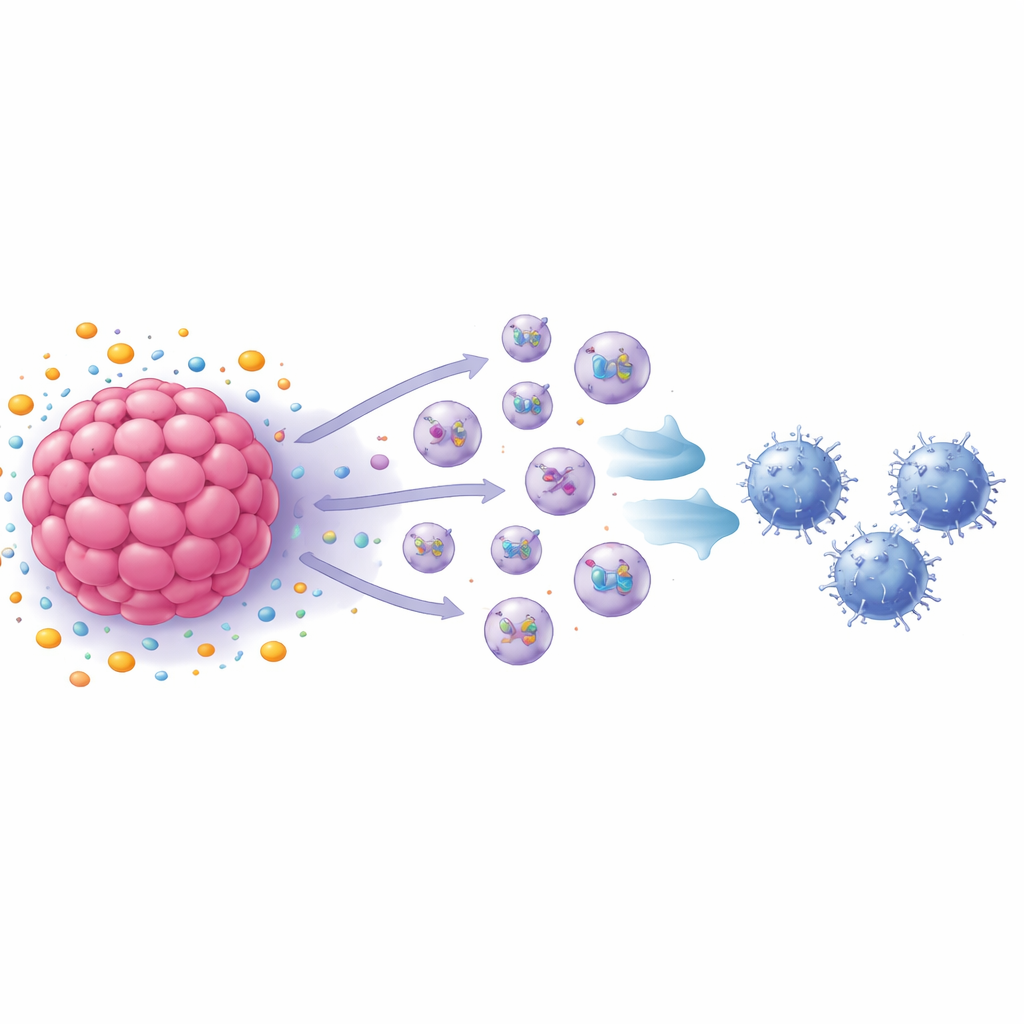
Vescicole minuscole come messaggeri della soppressione immunitaria
Il gruppo si è quindi concentrato sugli esosomi—vescicole di dimensioni nanometriche rilasciate dalle cellule che trasportano proteine e altre molecole verso bersagli distanti. Bloccare la produzione di esosomi ha in gran parte ripristinato la crescita delle cellule T CD8, e l’analisi ha mostrato che le cellule di carcinoma mammario trattate con S1P rilasciavano molti più esosomi rispetto alle cellule non trattate. Quando questi esosomi sono stati aggiunti direttamente a cellule T CD8 attivate, le T hanno rallentato la proliferazione e hanno cominciato a mostrare i segni distintivi dell’esaurimento, inclusi diversi marcatori di superficie e intracellulari associati a cellule immunitarie logore. In esperimenti su animali, gli esosomi provenienti da cellule tumorali murine trattate con S1P hanno accelerato la crescita tumorale e aumentato il numero di T CD8 esaurite all’interno dei tumori, mentre gli esosomi da cellule prive di un recettore chiave avevano l’effetto opposto.
Un recettore confezionato negli esosomi causa il danno
Per capire cosa rendeva questi esosomi così dannosi, gli scienziati hanno analizzato le proteine legate all’immunità arricchite nel loro contenuto. Hanno trovato che una proteina, il recettore del fattore di crescita trasformante beta 2 (TGFBR2), era fortemente aumentata sugli esosomi dopo il trattamento con S1P, mentre un’altra proteina checkpoint ben nota, PD-L1, non lo era. Gli esosomi si fondevano con le cellule T CD8 e trasferivano TGFBR2 alla superficie delle T, dotando di fatto le cellule T di una copia aggiuntiva di un recettore che attiva programmi di esaurimento all’interno della cellula. Quando il gruppo ha bloccato TGFBR2 sugli esosomi con un anticorpo o ne ha ridotto i livelli nelle cellule tumorali, gli esosomi non sono più riusciti a sopprimere l’attività delle T né a indurre i marcatori di esaurimento, e le cellule T CD8 hanno recuperato la capacità di produrre molecole chiave per l’attacco.
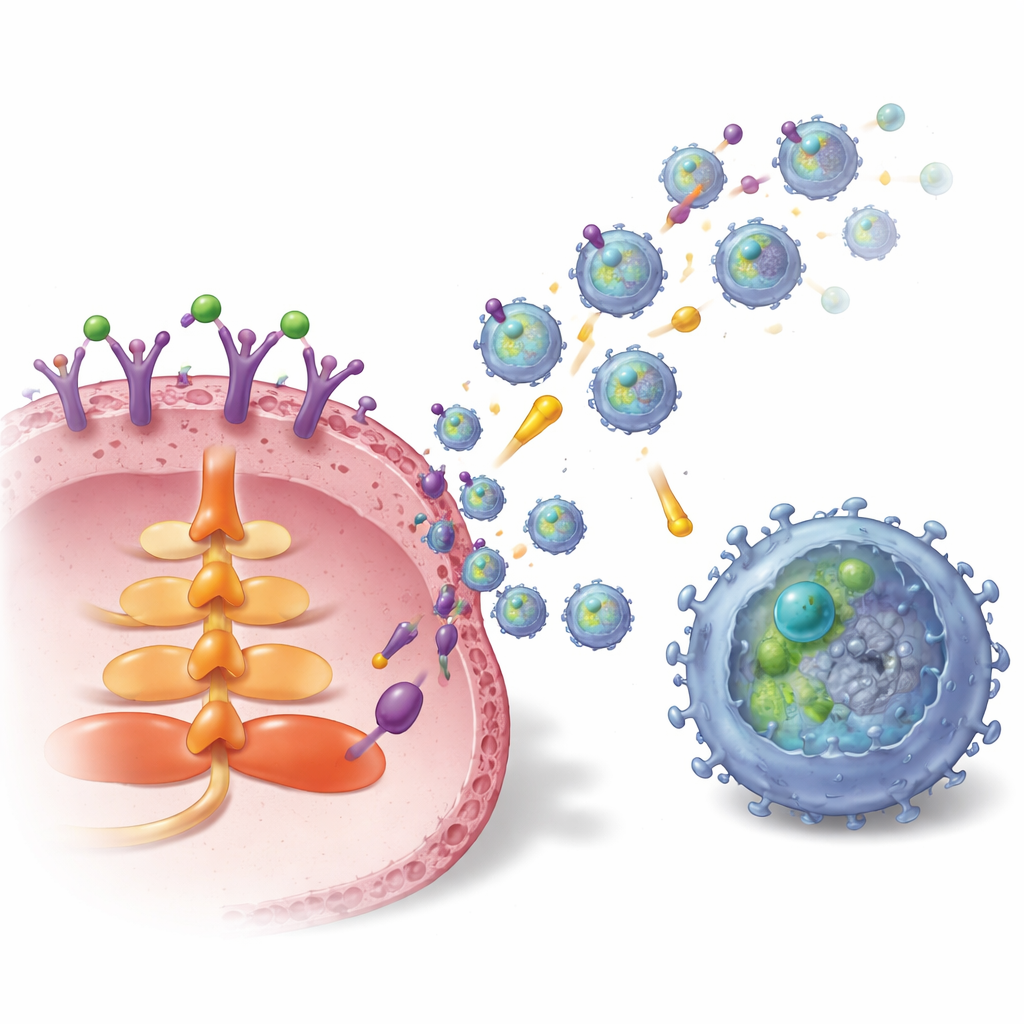
Come il tumore carica e lancia queste vescicole
Lo studio ha quindi mappato il circuito interno che collega S1P alla produzione di esosomi e al caricamento di TGFBR2. L’attivazione di un recettore specifico per S1P sulle cellule di carcinoma mammario, chiamato S1P1, attivava la via di segnalazione AKT e una proteina di traffico denominata Rab27a, entrambe cruciali per il rilascio degli esosomi. Allo stesso tempo, S1P1 aumentava la quantità e la stabilità di TGFBR2 all’interno delle cellule tumorali. Ciò avveniva in due modi: innanzitutto attivando un fattore di trascrizione, LEF1, che incrementa l’espressione genica di TGFBR2; in secondo luogo innalzando i livelli di una deubiquitinasi, USP8, tramite una via di segnalazione ERK–CREB1. USP8 rallenta il degrado di TGFBR2, consentendo a più recettore di accumularsi e di essere incapsulato negli esosomi. Nei campioni di tumore mammario dei pazienti, sia S1P1 sia TGFBR2 erano più elevati nel tessuto tumorale e negli esosomi derivati dal tumore rispetto al tessuto normale circostante, e livelli più alti di TGFBR2 negli esosomi correlavano con un maggior numero di cellule T CD8 esaurite.
Cosa significa per i pazienti
Per un lettore non specialista, il messaggio centrale è che certi carcinomi mammari creano un ambiente chimico ricco di S1P che istruisce le cellule tumorali a rilasciare minuscole vescicole cariche di un recettore, TGFBR2, che spegne le cellule T CD8. Queste vescicole agiscono come pacchetti stealth che riprogrammano le cellule killer vicine a diventare pigre e tolleranti nei confronti del tumore. Identificando la catena di eventi S1P–S1P1–TGFBR2, compresi gli interruttori intracellulari che controllano il rilascio degli esosomi e l’accumulo del recettore, questo lavoro suggerisce diversi nuovi bersagli farmacologici. Inibire la segnalazione S1P, bloccare S1P1 o impedire che TGFBR2 raggiunga o si stabilizzi sugli esosomi potrebbe ridurre l’esaurimento delle cellule T CD8 e rendere le immunoterapie esistenti più efficaci per le pazienti con carcinoma mammario.
Citazione: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Parole chiave: immunoterapia nel carcinoma mammario, esaurimento delle cellule T CD8, sfingosina-1-fosfato, esosomi, segnalazione TGFBR2