Clear Sky Science · fr
Le sphingosine-1-phosphate favorise l’épuisement des lymphocytes T CD8 dans le cancer du sein via le transfert exosomal de TGFBR2
Pourquoi cela compte pour le traitement du cancer
De nombreuses thérapies anticancéreuses modernes visent à libérer le propre système immunitaire du corps, et en particulier les lymphocytes T CD8 cytotoxiques, pour attaquer les tumeurs. Pourtant, dans de nombreux cancers du sein, ces cellules deviennent fatiguées et inefficaces, un état appelé épuisement, et l’immunothérapie n’est souvent que faiblement efficace. Cette étude révèle un mécanisme jusque-là caché par lequel les tumeurs mammaires « sédatent » chimiquement les lymphocytes T CD8 à distance, mettant en lumière une voie de signalisation nouvelle qui pourrait être bloquée pour améliorer l’efficacité des immunothérapies existantes.
Une molécule lipidique qui façonne le microenvironnement tumoral
Les chercheurs se sont concentrés sur le sphingosine-1-phosphate (S1P), une molécule de signalisation de type lipidique présente à des niveaux élevés dans le cancer du sein. On sait déjà que le S1P favorise l’angiogenèse tumorale, la dissémination et la résistance aux traitements. Ici, l’équipe a demandé si le S1P aide aussi les tumeurs à neutraliser les lymphocytes T CD8 dans leur voisinage. Lorsqu’ils ont cultivé des cellules cancéreuses mammaires humaines en présence de S1P puis les ont mises en co-culture avec des lymphocytes T CD8 humains, ces derniers se sont divisés beaucoup moins, même en l’absence de contact physique avec les cellules tumorales. Cette suppression sans contact a suggéré que les cellules tumorales libéraient des particules porteuses de messages dans le milieu.
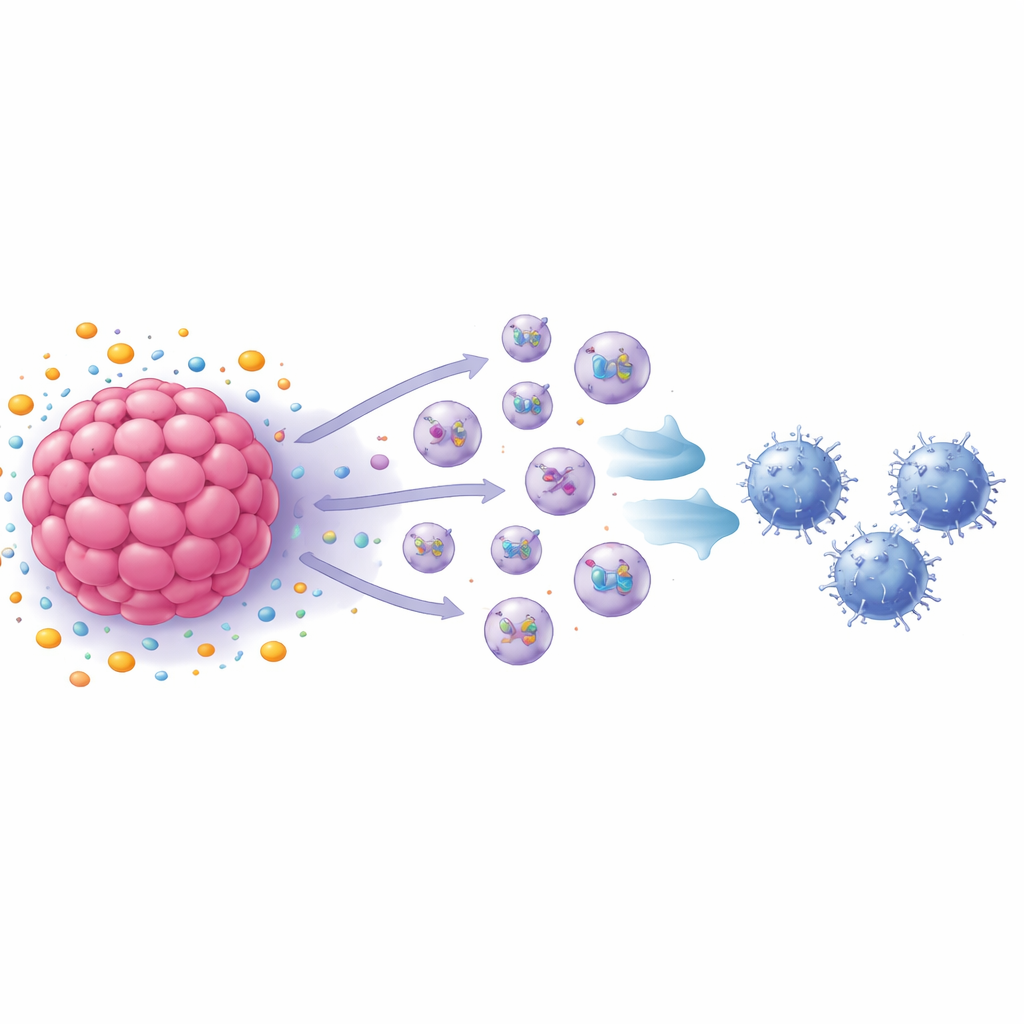
Des vésicules minimes comme messagers de suppression immunitaire
L’équipe s’est ensuite intéressée aux exosomes — des vésicules de l’ordre du nanomètre émises par les cellules et qui transportent des protéines et d’autres molécules vers des cibles distantes. Bloquer la production d’exosomes a en grande partie restauré la prolifération des lymphocytes T CD8, et les analyses ont montré que les cellules cancéreuses traitées au S1P libéraient beaucoup plus d’exosomes que les cellules non traitées. Lorsque ces exosomes ont été ajoutés directement à des lymphocytes T CD8 activés, ces derniers ont ralenti leur prolifération et ont commencé à afficher des signes d’épuisement, y compris plusieurs marqueurs de surface et intracellulaires associés à des cellules immunitaires affaiblies. Dans des expériences animales, les exosomes provenant de cellules mammaires de souris traitées au S1P ont accéléré la croissance tumorale et augmenté la proportion de lymphocytes T CD8 épuisés au sein des tumeurs, tandis que les exosomes issus de cellules dépourvues d’un récepteur clé avaient l’effet inverse.
Un récepteur chargé dans les exosomes cause les dommages
Pour comprendre pourquoi ces exosomes étaient si nocifs, les scientifiques ont examiné les protéines liées à l’immunité enrichies dans leur contenu. Ils ont découvert qu’une protéine, le récepteur du facteur de croissance transformant bêta 2 (TGFBR2), était fortement augmentée sur les exosomes après traitement au S1P, alors qu’une autre protéine de point de contrôle bien connue, PD-L1, ne l’était pas. Les exosomes fusionnaient avec les lymphocytes T CD8 et transféraient TGFBR2 à la surface des T, équipant de fait ces cellules d’une copie supplémentaire d’un récepteur qui active des programmes d’épuisement intracellulaires. Lorsque l’équipe a bloqué TGFBR2 sur les exosomes avec un anticorps ou réduit son niveau dans les cellules cancéreuses, les exosomes n’ont plus pu supprimer l’activité des T ni induire les marqueurs d’épuisement, et les lymphocytes T CD8 ont retrouvé leur capacité à produire des molécules effectrices essentielles.
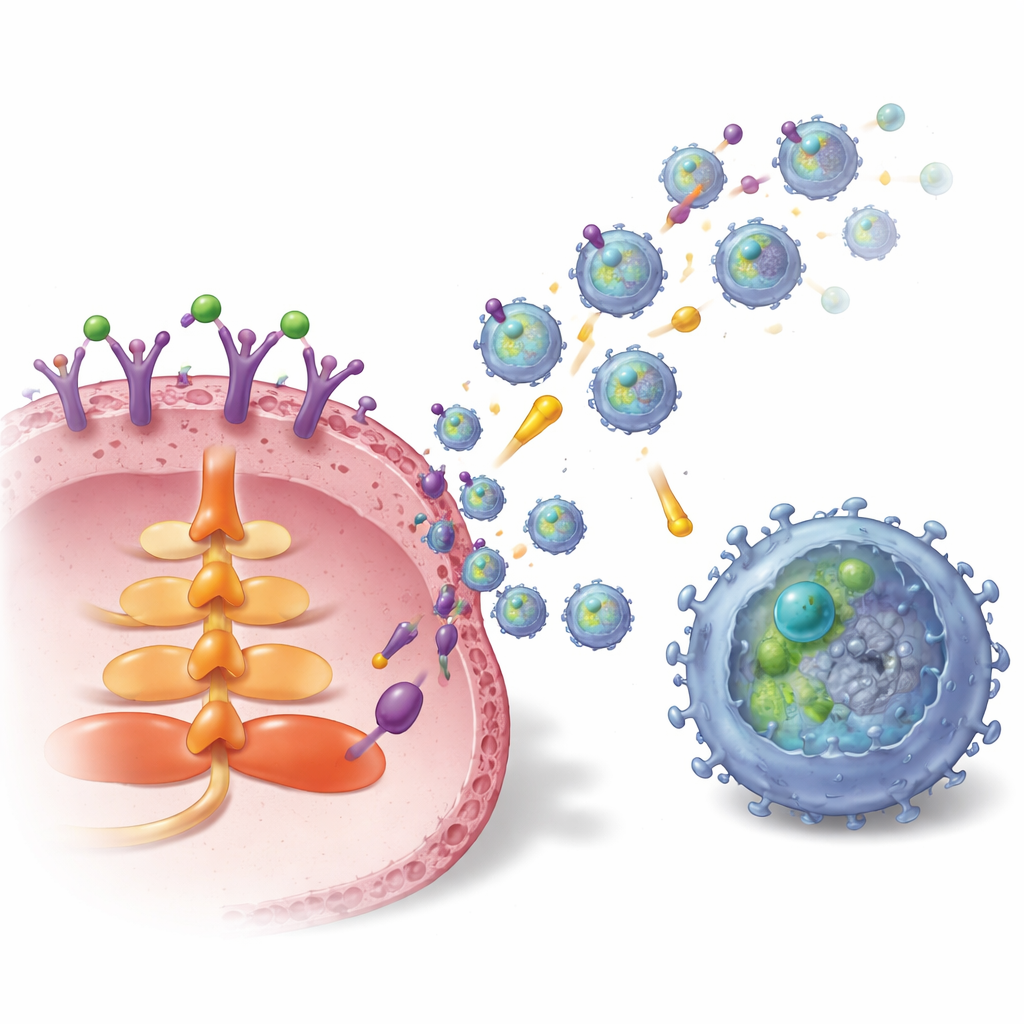
Comment la tumeur fabrique et expédie ces vésicules
L’étude a ensuite cartographié le câblage interne reliant le S1P à la production d’exosomes et au chargement en TGFBR2. L’activation d’un récepteur spécifique du S1P sur les cellules tumorales mammaires, appelé S1P1, a activé la voie de signalisation AKT et une protéine de trafic nommée Rab27a, toutes deux cruciales pour la libération d’exosomes. Parallèlement, S1P1 augmentait la quantité et la stabilité de TGFBR2 dans les cellules cancéreuses. Cela se faisait de deux manières : d’une part en activant un facteur de transcription, LEF1, qui stimule l’expression du gène TGFBR2, et d’autre part en augmentant les niveaux d’une désubiquitinase, USP8, via une voie ERK–CREB1. USP8 ralentit la dégradation de TGFBR2, permettant à plus de récepteur de s’accumuler et d’être empaqueté dans les exosomes. Dans des échantillons de tumeurs mammaires de patientes, S1P1 et TGFBR2 étaient présents à des niveaux plus élevés dans le tissu tumoral et dans les exosomes d’origine tumorale que dans le tissu normal adjacent, et un taux élevé de TGFBR2 sur les exosomes corrélait avec davantage de lymphocytes T CD8 épuisés.
Que cela signifie pour les patientes
Pour un non-spécialiste, le message central est que certains cancers du sein créent un environnement chimique riche en S1P qui ordonne aux cellules tumorales de sécréter de petites vésicules chargées d’un récepteur, TGFBR2, qui désactive les lymphocytes T CD8. Ces vésicules agissent comme des colis furtifs qui reprogramment les cellules tueuses voisines pour les rendre léthargiques et tolérantes à la tumeur. En identifiant la chaîne d’événements S1P–S1P1–TGFBR2, y compris les interrupteurs internes qui contrôlent la libération des exosomes et l’accumulation du récepteur, ce travail suggère plusieurs nouvelles cibles médicamenteuses. Inhiber la signalisation du S1P, bloquer S1P1 ou empêcher TGFBR2 d’atteindre ou de se stabiliser sur les exosomes pourrait réduire l’épuisement des lymphocytes T CD8 et rendre les immunothérapies existantes plus efficaces pour les patientes atteintes de cancer du sein.
Citation: Bhoumick, A., Ghosh, A., Singh, A. et al. Sphingosine-1-phosphate promotes CD8 T cell exhaustion in breast cancer via exosomal transfer of TGFBR2. Cell Death Dis 17, 278 (2026). https://doi.org/10.1038/s41419-026-08523-5
Mots-clés: immunothérapie du cancer du sein, épuisement des lymphocytes T CD8, sphingosine-1-phosphate, exosomes, signalisation TGFBR2