Clear Sky Science · zh
β-连环蛋白突变通过转录激活OXCT1,重编程酮体代谢以驱动肝细胞癌转移并抵抗生酮疗法
这对癌症与饮食有何意义
生酮饮食以高脂肪、极低碳水为特色,正被研究用来通过改变机体燃料来源来“饿死”肿瘤。该研究显示,对于一类重要的肝癌亚群,常见的基因改变使肿瘤细胞劫持酮体作为能量和生长来源。与其因生酮饮食而受损,这些癌症反而可能变得更难治疗并更易转移,这突出了基于饮食的癌症疗法必须与每个肿瘤的生物学特性相匹配。
深入了解肝癌与关键突变
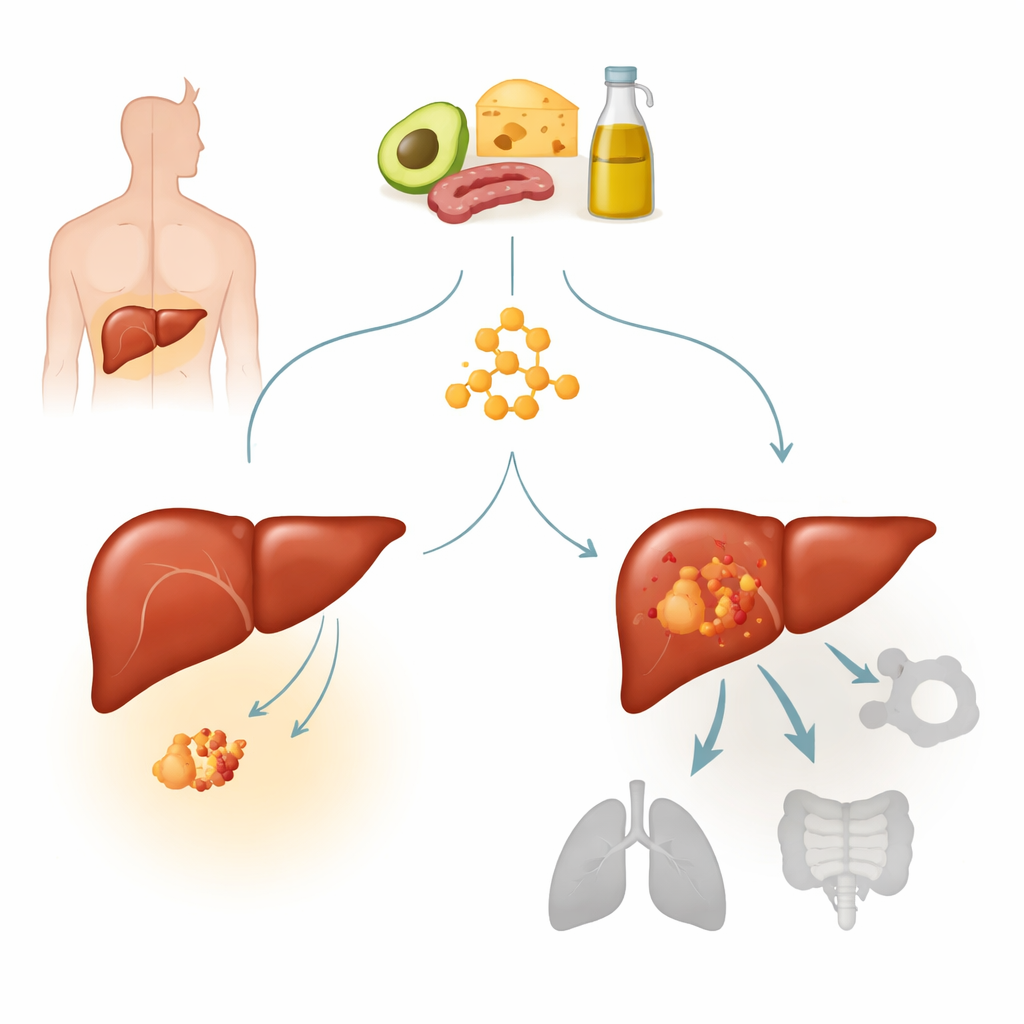
肝细胞癌是最常见的肝癌类型,也是全球主要的癌症死亡原因之一。许多此类肿瘤携带称为β-连环蛋白(beta-catenin)的基因激活性突变,该基因通常参与调控细胞生长与信号响应。一个热点突变S33Y会使β-连环蛋白通路持续激活,并定义出一种独特的肝癌亚型。作者此前发现具有强烈酮体代谢的肿瘤对生酮饮食似乎反应较差。本研究聚焦β-连环蛋白突变肿瘤,探究该突变是否使肝癌对生酮疗法本质上具有抗性,以及可能的机制。
“低糖”饮食为什么无法抑制肿瘤
研究者在小鼠体内比较了携带或不携带S33Y β-连环蛋白突变的人源肝癌细胞,在普通饮食或生酮饮食下的表现。在未携带突变的肿瘤中,生酮饮食明显减缓了肿瘤生长:肿瘤更小、更轻,尽管动物体重维持且血酮上升、血糖下降符合预期。鲜明对比的是,由β-连环蛋白突变驱动的肿瘤在两种饮食下均具有侵袭性生长,且未从生酮方案中获益。研究组在病人来源的肝肿瘤移植模型中观察到类似模式:生酮喂养缩小了β-连环蛋白正常的肿瘤,但并未抑制β-连环蛋白突变肿瘤的生长,表明这是真正的耐受性而非模型特异性效应。
癌细胞如何将酮体转化为生长燃料
为了解释这种耐受性,作者研究了突变β-连环蛋白如何重塑癌细胞内的酮体处理。他们聚焦于OXCT1——细胞分解酮体的主要酶,而在健康肝组织中这一过程通常很少见。β-连环蛋白突变细胞显著提高了OXCT1及其他酮体相关酶的表达,用标记酮体的代谢追踪显示这些细胞能高效地将酮体转化为谷氨酸,后者既是重要的构建模块也是能量来源。深入的分子实验揭示,突变的β-连环蛋白与其伙伴蛋白LEF1合作,结合OXCT1基因的调控区并激活其表达。在突变肿瘤中阻断OXCT1可降低谷氨酸生成并消除它们对生酮饮食的耐受性,表明该酶是关键的代谢“开关”。
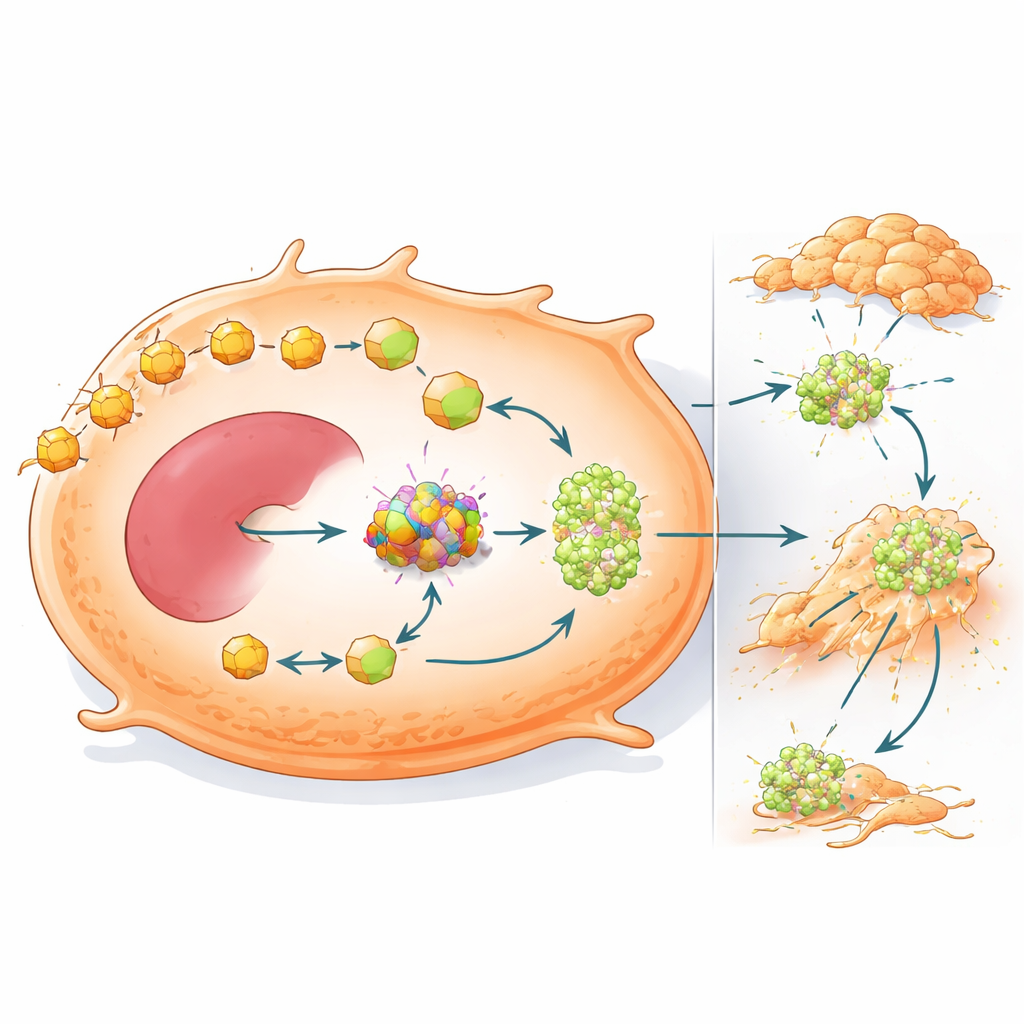
重编程的燃料利用也驱动癌症转移
研究进一步表明,OXCT1不仅帮助肿瘤在低碳环境中存活——它还使肿瘤更易发生转移。当在肝癌细胞中提高OXCT1表达时,这些细胞在体外实验中迁移和侵袭性增强,并在小鼠肝脏中形成更多的转移结节。基因分析将高OXCT1与信号蛋白STAT3的激活及上皮—间质转化程序(细胞松动连接并获得更具移动性与侵袭性的状态)联系起来。在动物实验中,β-连环蛋白突变肿瘤表现出强烈的STAT3激活和广泛的转移,但敲低OXCT1在很大程度上逆转了这些改变并减少了肝脏和肺部的菌落形成(colonization)。
这对生酮疗法意味着什么
通俗地说,这项工作表明携带常见β-连环蛋白突变的某些肝癌能将生酮疗法的初衷颠倒过来。这类肿瘤并非在碳水稀缺时被剥夺燃料,而是通过激活OXCT1燃烧酮体,将其转化为支持生长的分子,并启动有利于转移的通路。因此,仅靠生酮饮食对这一肿瘤亚型的患者可能既有风险又无效。研究结果建议对肿瘤进行β-连环蛋白与OXCT1状态检测,并开发阻断OXCT1的药物,以便通过阻止肿瘤将预期的治疗变为自身优势,来使基于饮食的策略更安全、更有效。
引用: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
关键词: 生酮饮食, 肝癌, β-连环蛋白突变, 肿瘤代谢, OXCT1