Clear Sky Science · es
La mutación de β-catenina reprograma el metabolismo de los cuerpos cetónicos para impulsar la metástasis del carcinoma hepatocelular y la resistencia a la terapia cetogénica mediante la activación transcripcional de OXCT1
Por qué importa esto para el cáncer y la dieta
Las dietas cetogénicas, ricas en grasas y muy bajas en carbohidratos, se están estudiando como una forma de “matar de hambre” a los tumores modificando el combustible que usa el cuerpo. Este estudio muestra que, en un subgrupo importante de cáncer de hígado, un cambio genético común permite que las células tumorales secuestren los cuerpos cetónicos como fuente de energía y de crecimiento. En lugar de debilitarse con una dieta cetogénica, estos cánceres pueden volverse más difíciles de tratar y más propensos a diseminarse, lo que subraya por qué las terapias basadas en la dieta deben ajustarse a la biología de cada tumor.
Una mirada más cercana al cáncer de hígado y a una mutación clave
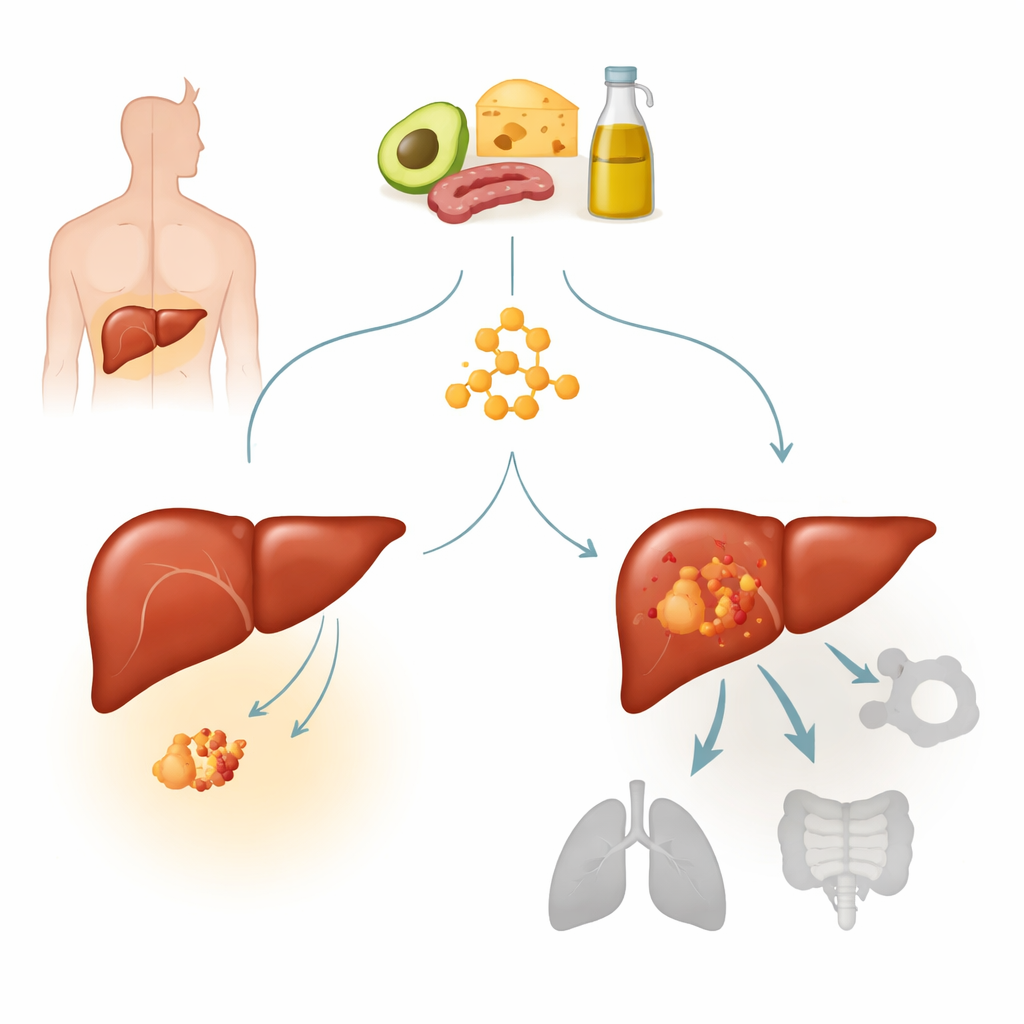
El carcinoma hepatocelular es la forma más común de cáncer de hígado y una de las principales causas de muerte por cáncer en todo el mundo. Muchos de estos tumores presentan mutaciones activadoras en un gen llamado beta-catenina, que normalmente ayuda a controlar cómo crecen las células y cómo responden a señales. Una mutación frecuente, denominada S33Y, mantiene la vía de beta-catenina encendida de forma permanente y define un subtipo distinto de cáncer de hígado. Los autores habían observado anteriormente que los tumores con metabolismo fuerte de cuerpos cetónicos parecían menos sensibles a las dietas cetogénicas. Aquí se centraron en los tumores con mutación en beta-catenina para preguntar si dicha mutación hace que los cánceres de hígado sean intrínsecamente resistentes a la terapia cetogénica y, en caso afirmativo, por qué.
Cuando una dieta “baja en azúcares” no logra frenar los tumores
Usando células humanas de cáncer de hígado implantadas en ratones, los investigadores compararon tumores con y sin la mutación S33Y en beta-catenina bajo una dieta normal o una dieta cetogénica. En tumores sin la mutación, la dieta cetogénica ralentizó claramente el crecimiento: los tumores fueron más pequeños y ligeros, aunque los animales mantuvieron el peso corporal y mostraron el aumento esperado de cetonas en sangre y la caída de glucosa. En marcado contraste, los tumores impulsados por la mutación de beta-catenina crecieron de forma agresiva con ambas dietas y no mostraron beneficio del régimen cetogénico. El equipo observó un patrón similar en injertos tumorales derivados de pacientes: la alimentación cetogénica redujo los tumores con beta-catenina normal, pero no frenó el crecimiento de los tumores con mutación en beta-catenina, lo que indica una resistencia verdadera y no un efecto específico del modelo.
Cómo las células cancerosas convierten las cetonas en combustible para el crecimiento
Para entender esta resistencia, los autores examinaron cómo la beta-catenina mutada remodela el manejo de las cetonas dentro de las células cancerosas. Se centraron en OXCT1, la enzima principal que permite a las células degradar los cuerpos cetónicos —un proceso que normalmente es mínimo en el tejido hepático sano. Las células con mutación en beta-catenina aumentaron fuertemente los niveles de OXCT1 y de otras enzimas relacionadas con las cetonas, y el trazado metabólico con cetonas marcadas mostró que estas células convirtieron eficientemente las cetonas en glutamato, un componente clave para la síntesis y fuente de energía. Experimentos moleculares detallados revelaron que la beta-catenina mutada se asocia con una proteína compañera, LEF1, para unirse a la región de control del gen OXCT1 y activarlo. Bloquear OXCT1 en tumores mutantes redujo la producción de glutamato y eliminó su resistencia a la dieta cetogénica, lo que indica que esta enzima es un “interruptor” metabólico crítico.
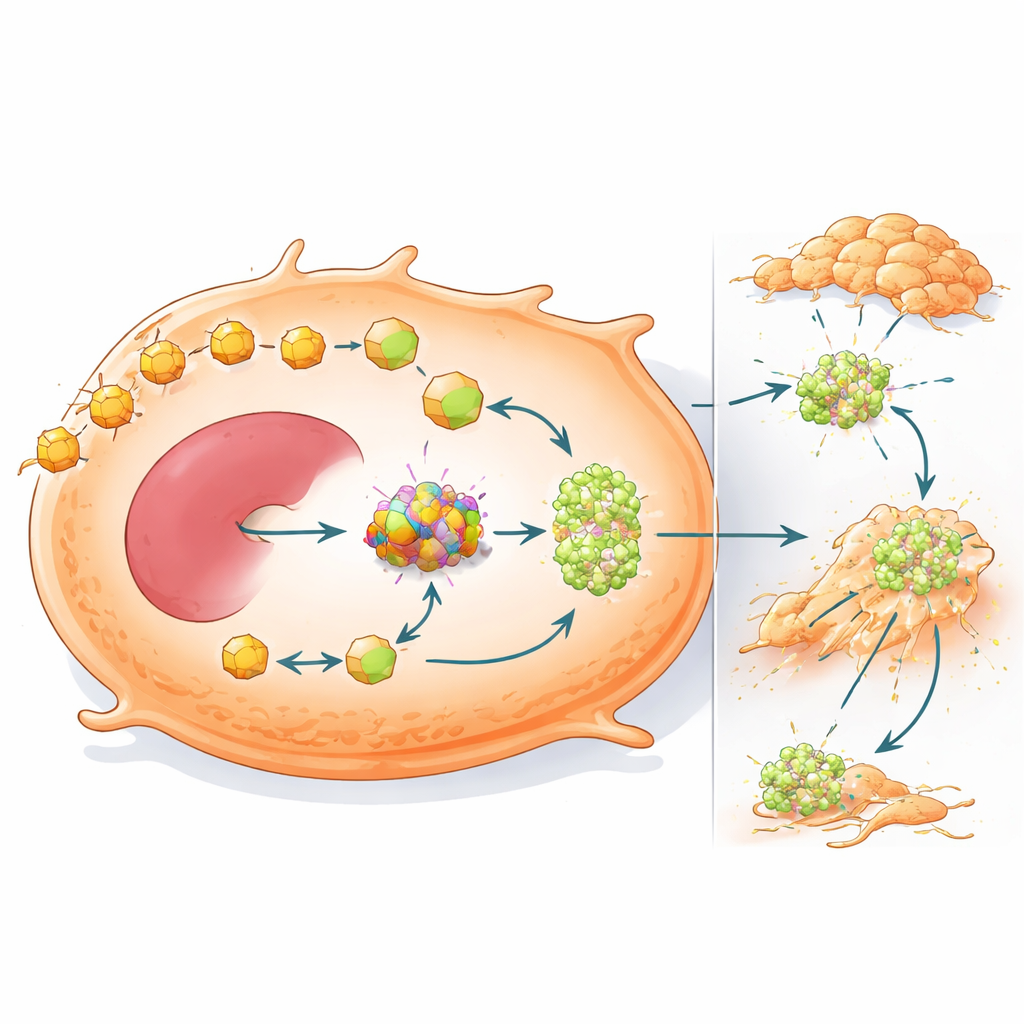
El consumo de combustible reprogramado también impulsa la diseminación
El estudio muestra además que OXCT1 hace más que ayudar a los tumores a sobrevivir en un entorno bajo en carbohidratos: también los vuelve más propensos a diseminarse. Cuando OXCT1 se elevó en células de cáncer de hígado, estas migraron e invadieron el tejido circundante con más agresividad en pruebas de laboratorio y formaron más nódulos metastásicos en los hígados de ratones. Los análisis genéticos vincularon un alto OXCT1 con la activación de una proteína de señalización llamada STAT3 y con un programa de transición epitelio-mesénquima, en el que las células aflojan sus adhesiones y adquieren un estado más móvil e invasivo. En animales, los tumores con mutación en beta-catenina mostraron fuerte activación de STAT3 y metástasis extensa, pero la reducción de OXCT1 revirtió en gran medida estos cambios y disminuyó la colonización tanto hepática como pulmonar.
Qué implica esto para la terapia cetogénica
En términos cotidianos, este trabajo muestra que algunos cánceres de hígado con una mutación común en beta-catenina pueden darle la vuelta a la terapia cetogénica. En lugar de quedarse sin combustible cuando escasean los carbohidratos, estos tumores activan OXCT1 para quemar cuerpos cetónicos, convertirlos en moléculas que sostienen el crecimiento y activar vías que facilitan la diseminación. Como resultado, las dietas cetogénicas por sí solas pueden ser arriesgadas o ineficaces para pacientes con este subtipo tumoral. Los hallazgos sugieren que analizar los tumores para conocer el estado de beta-catenina y OXCT1, y desarrollar fármacos que bloqueen OXCT1, podría hacer que las estrategias basadas en la dieta sean más seguras y eficaces al impedir que los cánceres conviertan una terapia prevista en una ventaja.
Cita: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Palabras clave: dieta cetogénica, cáncer de hígado, mutación de beta-catenina, metabolismo tumoral, OXCT1