Clear Sky Science · pl
Mutacja β-kateniny przeprogramowuje metabolizm ciał ketonowych, napędzając przerzuty raka wątrobowokomórkowego i oporność na terapię ketogeniczną poprzez aktywację transkrypcyjną OXCT1
Dlaczego to ma znaczenie dla raka i diety
Diety ketogeniczne, bogate w tłuszcz i bardzo ubogie w węglowodany, są badane jako sposób na „zagłodzenie” nowotworów poprzez zmianę źródła paliwa wykorzystywanego przez organizm. Badanie to pokazuje, że w istotnej podgrupie raka wątroby powszechna zmiana genetyczna umożliwia komórkom nowotworowym wykorzystanie ciał ketonowych jako źródła energii i wzrostu. Zamiast osłabienia przez dietę ketogeniczną, nowotwory te mogą stać się trudniejsze do leczenia i bardziej skłonne do rozprzestrzeniania się, co podkreśla konieczność dopasowania terapii dietetycznych do biologii konkretnego guza.
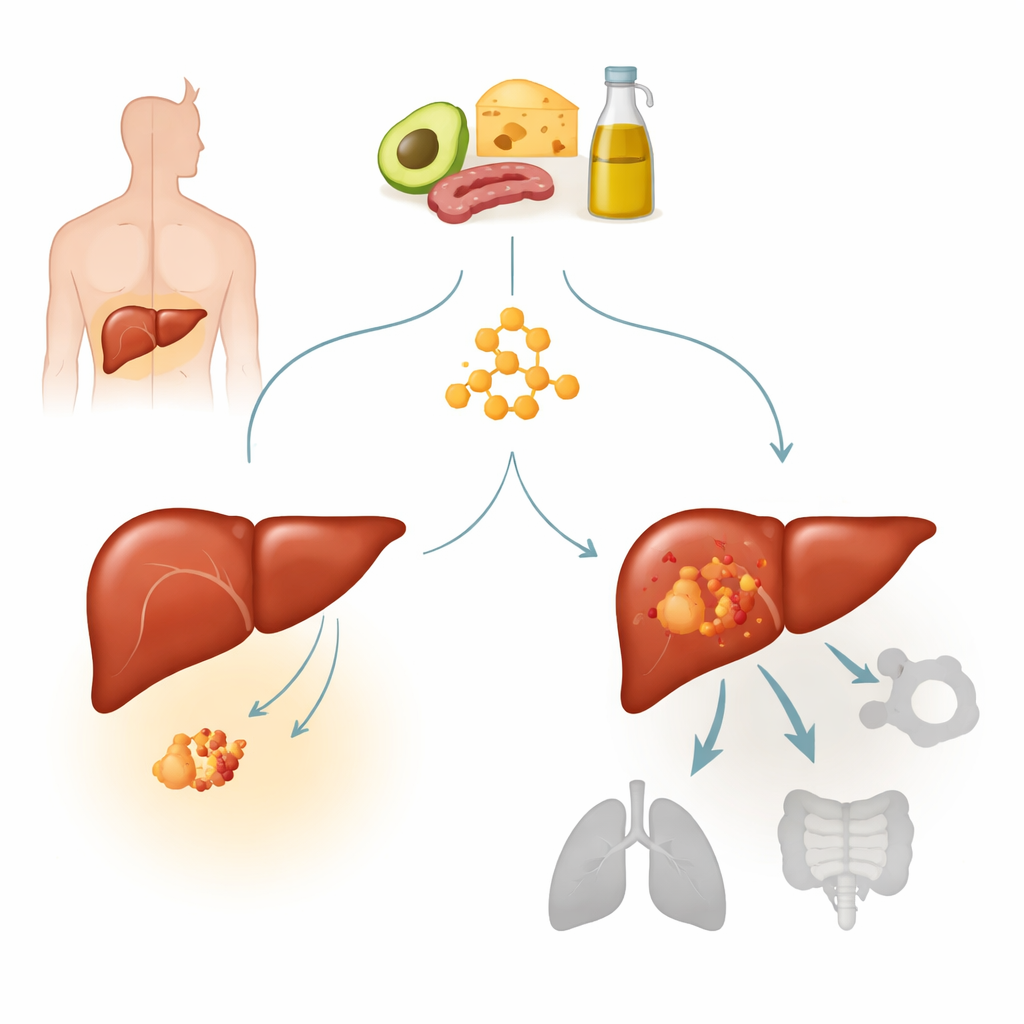
Bliższe spojrzenie na raka wątroby i kluczową mutację
Rak wątrobowokomórkowy jest najczęstszą postacią raka wątroby i jednym z głównych powodów zgonów z powodu nowotworów na świecie. Wiele z tych guzów nosi aktywujące mutacje w genie zwanym beta-kateniną, który normalnie pomaga kontrolować wzrost komórek i ich odpowiedzi na sygnały. Jedna z mutacji hotspot, nazwana S33Y, utrzymuje szlak beta-kateniny trwale włączony i definiuje odrębną podkategorię raka wątroby. Autorzy wcześniej zauważyli, że nowotwory o silnym metabolizmie ketonowym wydawały się mniej wrażliwe na diety ketogeniczne. W tym badaniu skupili się na guzach z mutacją beta-kateniny, aby sprawdzić, czy ta mutacja czyni raki wątroby z natury opornymi na terapię ketogeniczną i jeśli tak — w jaki sposób.
Gdy „niska zawartość cukru” nie spowalnia guzów
Badacze użyli ludzkich komórek raka wątroby hodowanych w myszach i porównali guzy z mutacją S33Y beta-kateniny oraz bez niej przy diecie normalnej lub ketogenicznej. W guzach bez mutacji dieta ketogeniczna wyraźnie spowalniała wzrost: guzy były mniejsze i lżejsze, mimo że zwierzęta utrzymywały masę ciała i wykazywały oczekiwany wzrost ketonów we krwi oraz spadek glukozy. W ostrym kontraście guzy napędzane mutacją beta-kateniny rosły agresywnie przy obu dietach i nie czerpały korzyści z reżimu ketogenicznego. Podobny wzorzec zaobserwowano w przeszczepach guzów pochodzących od pacjentów: żywienie ketogeniczne zmniejszało guzy z normalną beta-kateniną, lecz nie hamowało wzrostu guzów z mutacją beta-kateniny, co wskazuje na prawdziwą oporność, a nie efekt specyficzny dla modelu.
Jak komórki nowotworowe przekształcają ketony w paliwo wzrostu
Aby zrozumieć tę oporność, autorzy zbadali, jak zmutowana beta-katenina przekształca obsługę ketonów wewnątrz komórek nowotworowych. Skoncentrowali się na OXCT1, głównym enzymie umożliwiającym rozkład ciał ketonowych — procesie normalnie minimalnym w zdrowej tkance wątroby. Komórki z mutacją beta-kateniny silnie zwiększały poziomy OXCT1 i innych enzymów związanych z ketonami, a śledzenie metaboliczne z wykorzystaniem znakowanych ciał ketonowych wykazało, że te komórki wydajnie przekształcały ketony w glutaminian, kluczowy element budulcowy i źródło energii. Szczegółowe eksperymenty molekularne ujawniły, że zmutowana beta-katenina współpracuje z białkiem partnerem LEF1, by wiązać się z regionem regulatorowym genu OXCT1 i go włączać. Zablokowanie OXCT1 w guzach z mutacją zmniejszało produkcję glutaminianu i usuwało ich oporność na dietę ketogeniczną, co wskazuje, że enzym ten jest krytycznym metabolicznym „przełącznikiem”.
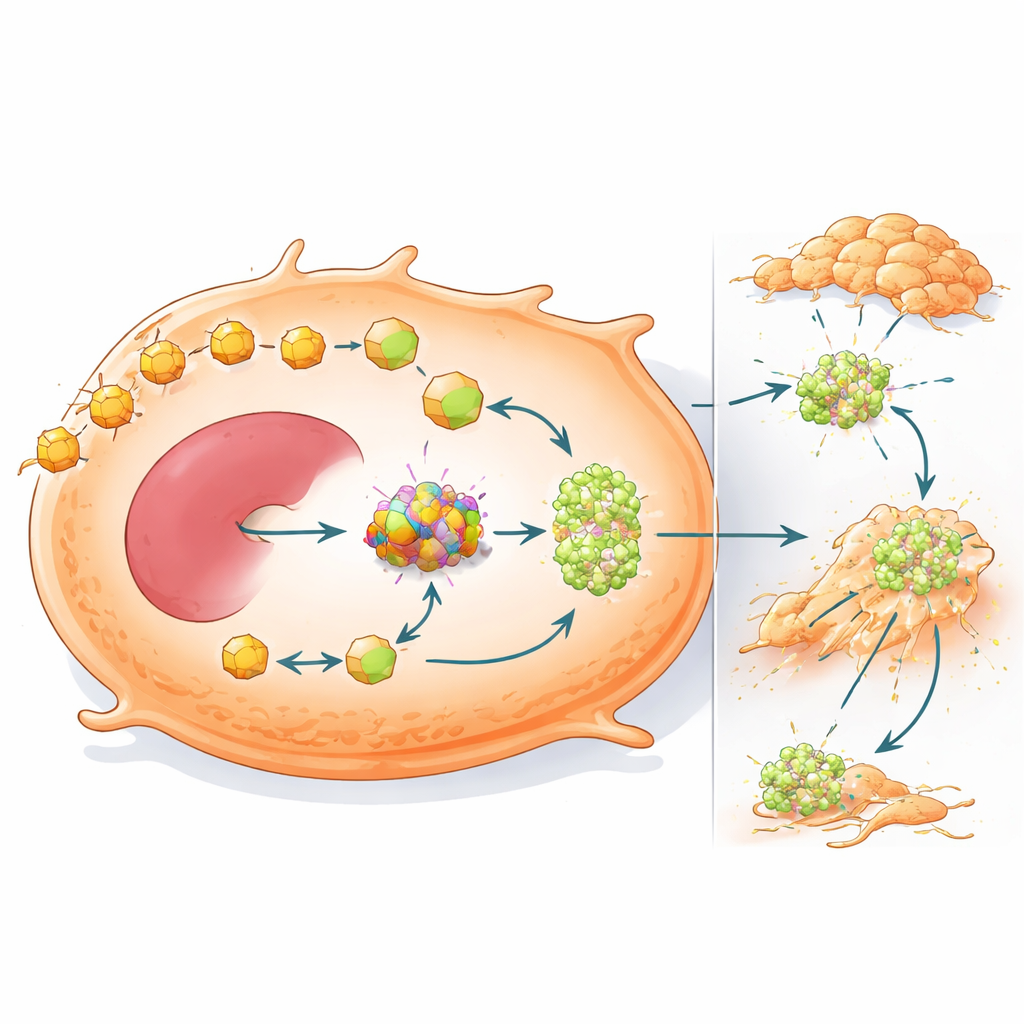
Przeprogramowane wykorzystanie paliwa napędza także rozprzestrzenianie się raka
Badanie dodatkowo pokazuje, że OXCT1 robi więcej niż pomaga guzom przetrwać w środowisku o niskiej zawartości węglowodanów — sprawia też, że są bardziej skłonne do rozsiewu. Gdy OXCT1 był podwyższony w komórkach raka wątroby, w testach laboratoryjnych wykazywały one silniejszą migrację i inwazję otaczających tkanek oraz tworzyły więcej przerzutowych guzków w wątrbach myszy. Analizy genowe powiązały wysoki poziom OXCT1 z aktywacją białka sygnałowego STAT3 oraz z programem przejścia nabłonkowo-mezenchymalnego, w którym komórki osłabiają połączenia między sobą i zyskują bardziej ruchliwy, inwazyjny stan. U zwierząt guzy z mutacją beta-kateniny wykazywały silną aktywację STAT3 i rozległe przerzuty, ale zmniejszenie ekspresji OXCT1 w dużej mierze odwracało te zmiany i redukowało kolonizację wątroby i płuc.
Co to oznacza dla terapii ketogenicznej
Mówiąc prostymi słowami, praca ta pokazuje, że niektóre raki wątroby niosące powszechną mutację beta-kateniny mogą odwrócić działanie terapii ketogenicznej. Zamiast być pozbawione paliwa przy niedoborze węglowodanów, guzy te aktywują OXCT1, spalają ciała ketonowe, przekształcają je w molekuły wspierające wzrost i uruchamiają szlaki sprzyjające rozsiewowi. W efekcie same diety ketogeniczne mogą być ryzykowne lub nieskuteczne dla pacjentów z tym podtypem guza. Wyniki sugerują, że badanie guzów pod kątem statusu beta-kateniny i OXCT1 oraz opracowanie leków blokujących OXCT1 mogłoby uczynić strategie oparte na diecie bezpieczniejszymi i skuteczniejszymi, zapobiegając sytuacji, w której zamierzona terapia staje się przewagą dla nowotworu.
Cytowanie: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Słowa kluczowe: dieta ketogeniczna, rak wątroby, mutacja beta-kateniny, metabolizm guza, OXCT1