Clear Sky Science · he
מוטציה ב‑β‑catenin משכתבת את חילוף החומרים של גופי קטון ומניעה גרורות וסיבול לטיפול קטוגני באמצעות הפעלה תעתיקית של OXCT1
מדוע זה חשוב לסרטן ותזונה
דיאטות קטוגניות, עתירות שומן ודלות מאוד בפחמימות, נחקרות כאמצעי "להרעיב" גידולים על ידי שינוי הדלק שהגוף משתמש בו. המחקר הזה מראה שעבור תת‑קבוצה חשובה של סרטן הכבד, שינוי גנטי נפוץ מאפשר לתאי הגידול לפרוץ ולנצל גופי קטון כמקור אנרגיה וצמיחה. במקום להיחלש על ידי דיאטה קטוגנית, סרטן זה עשוי להפוך לקשה יותר לטיפול ובעל נטייה גבוהה יותר להתפשט — מה שממחיש שגישות טיפול תזונתיות חייבות להיות מותאמות לביולוגיה הספציפית של כל גידול.
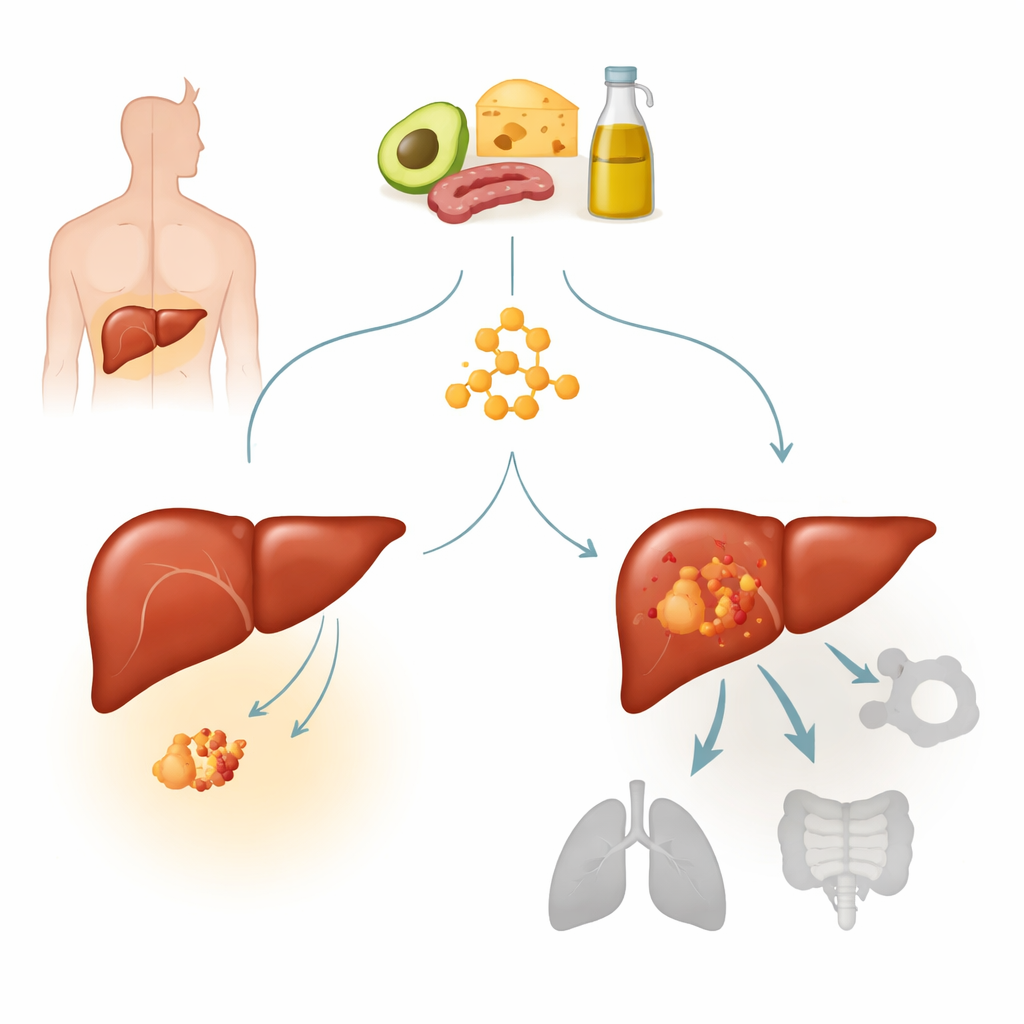
מבט קרוב יותר על סרטן הכבד ומוטציה מרכזית
קרצינומת תאי הכבד (HCC) היא הצורה הנפוצה ביותר של סרטן הכבד וסיבה מובילה לתמותה מסרטן ברחבי העולם. רבים מהגידולים הללו נושאים מוטציות מגרות בגן שנקרא בטא‑קטנין, שתפקידו רגיל לפקח על גדילה ותשובות תאיות לאותות. מוטציה ב"חם‑נקודה" אחת, שנקראת S33Y, משאירה את מסלול הבטא‑קטנין פעיל באופן קבוע ומגדירה תת‑סוג מובחן של סרטן הכבד. החוקרים גילו בעבר כי גידולים עם חילוף חומרים חזק של גופי קטון נראו פחות רגישים לדיאטות קטוגניות. כאן הם התמקדו בגידולים עם מוטציות בבטא‑קטנין כדי לשאול האם מוטציה זו עושה את סרטן הכבד בעמיד מטבולית כלפי טיפול קטוגני, ואם כן — כיצד.
מתי "דיאטה דלת סוכר" נכשלת בהאטת גידולים
באמצעות תאי סרטן כבד אנושיים שגודלו בעכברים, החוקרים השוו גידולים עם ובלי מוטציית S33Y בבטא‑קטנין תחת דיאטה רגילה או דיאטה קטוגנית. בגידולים ללא המוטציה, הדיאטה הקטוגנית האטה בבירור את הגדילה: הגידולים היו קטנים וקלים יותר, למרות שהחיות שמרו על משקל גוף וחלו העלייה הצפויה ברמת קטונים בדם והירידה בסוכר בדם. בניגוד חמור לכך, גידולים שמונעו על ידי מוטציית הבטא‑קטנין צמחו באגרסיביות תחת שתי הדיאטות ולא הראו תועלת מהמשטר הקטוגני. הצוות ראה דפוס דומה בהשתלות גידול ממטופלים: מזון קטוגני הקטין גידולים עם בטא‑קטנין תקין אך לא עצר את גדילתם של גידולים עם מוטנט בבטא‑קטנין, מה שמעיד על עמידות אמתית ולא על אפקט תלוי‑מודל.
כיצד תאי סרטן הופכים קטונים לדלק לצמיחה
כדי להבין את העמידות הזו, המחברים בחנו כיצד הבטא‑קטנין המוטנט משכתב את מנגנון הטיפול בקטונים בתוך תאי הסרטן. הם התמקדו ב‑OXCT1, האנזים המרכזי שמאפשר לתאים לפרק גופי קטון — תהליך שבמצב רגיל מצומצם ברקמת כבד בריאה. תאי בטא‑קטנין‑מוטנט הגדילו בעוצמה את רמות OXCT1 ואנזימים קשורים לקטון אחרים, ומחקר מטבולי עם קטונים מסומנים הראה שתאים אלה ממירים ביעילות קטונים לגלוטמט, אבני בניין ומקור אנרגיה מרכזי. ניסויים מולקולריים מפורטים חשפו שבטא‑קטנין המוטנט משתף פעולה עם חלבון שותף, LEF1, כדי להיקשר לאזור הבקרה של גן OXCT1 ולהפעילו. חסימת OXCT1 בגידולים מוטנטיים הקטינה את ייצור הגלוטמט וביטלה את העמידות שלהם לדיאטה הקטוגנית, מה שמצביע על כך שהאנזים הזה הוא "מתג" מטבולי קריטי.
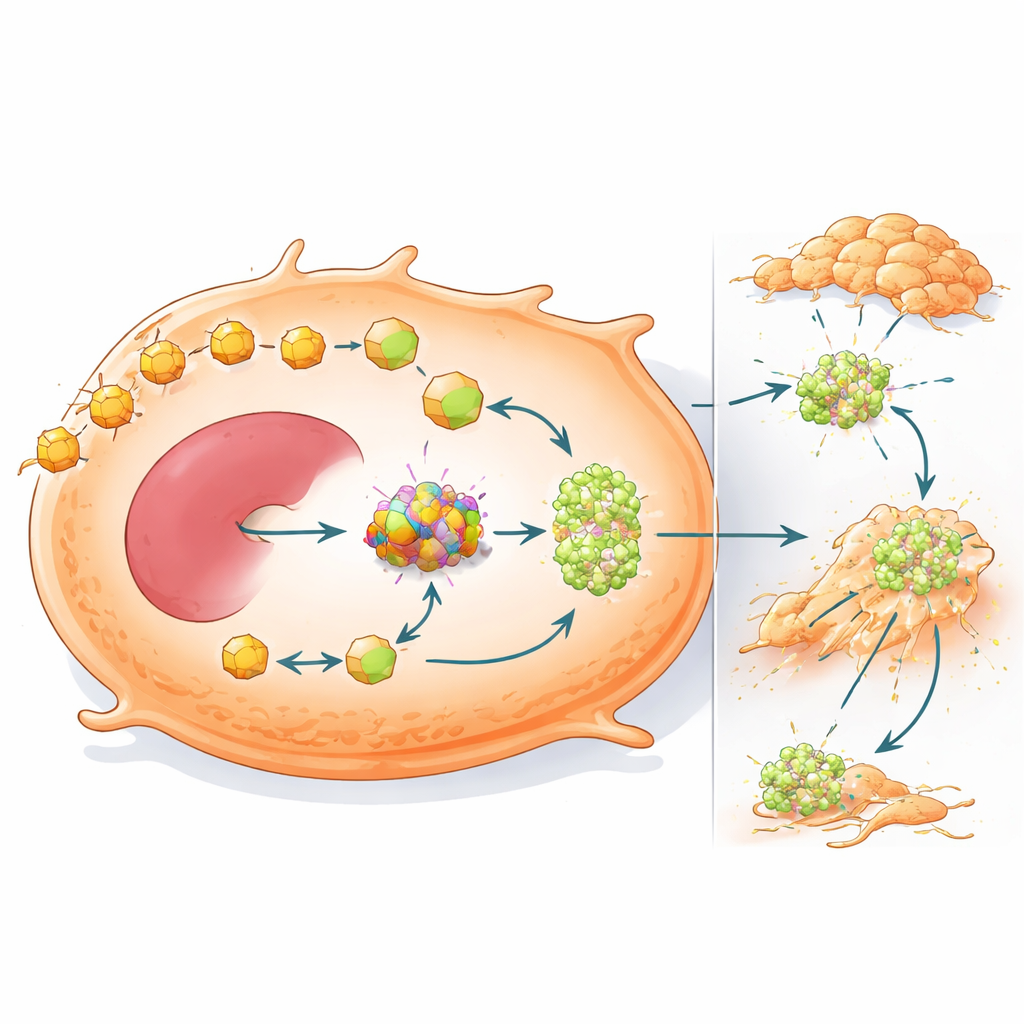
שימוש דלקי מחדש שמניע גם התפשטות סרטן
המחקר מראה עוד ש‑OXCT1 עושה יותר מסייעת הישרדות בסביבה דלת‑פחמימות — הוא גם מגדיל את הנטייה של הגידול להתפשט. כאשר OXCT1 הוגבר בתאי סרטן כבד, הם נדדו ופלשו לרקמות סמוכות ביתר אגרסיביות במבחני מעבדה ויצרו יותר נודולים גרורתיים בכבד העכברים. ניתוחי גנים קישרו רמות גבוהות של OXCT1 להפעלה של חלבון איתות שנקרא STAT3 ולתוכנית היפוך אפיתל‑מזנכימלית (EMT), שבה התאים משחררים את הקשרים שלהם ורוכשים מצב נייד ופולשני יותר. בחיות, לגידולים מוטנטיים בבטא‑קטנין הייתה הפעלת STAT3 חזקה ומטאסטזות נרחבות, אך דיכוי OXCT1 היפך ברובו שינויים אלו והקטין הן קולוניזציה בכבד והן בריאות.
מה המשמעות לטיפול קטוגני
במונחים פשוטים, עבודה זו מראה כי חלק מסרטני הכבד הנושאים מוטציה נפוצה בבטא‑קטנין יכולים להפוך את הטיפול הקטוגני נגדם. במקום להיחשף למחסור בדלק כאשר פחמימות נדירות, גידולים אלה מפעילים את OXCT1 כדי לשרוף גופי קטון, להפוך אותם למולקולות התומכות בצמיחה ולהפעיל מסלולים שמסייעים להתפשטות. כתוצאה מכך, דיאטות קטוגניות בבדן עלולות להיות מסוכנות או חסרות יעילות עבור חולים עם תת‑הסוג הזה של הגידול. הממצאים מציעים כי בדיקה של מצב הבטא‑קטנין ו‑OXCT1 בגידולים, ופיתוח תרופות החוסמות OXCT1, עשויים להפוך אסטרטגיות מבוססות תזונה לבטוחות ויעילות יותר על ידי מניעת ניצול הטיפול לטובת הגידול.
ציטוט: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
מילות מפתח: דיאטה קטוגנית, סרטן הכבד, מוטציה ב‑בטא‑קטנין, חילוף חומרים בגידול, OXCT1