Clear Sky Science · de
β-Catenin-Mutation programmiert den Ketonkörperstoffwechsel um, treibt Metastasierung des hepatozellulären Karzinoms und Resistenz gegen ketogene Therapie durch transkriptionelle Aktivierung von OXCT1 voran
Warum das für Krebs und Ernährung wichtig ist
Ketogene Diäten, die reich an Fett und sehr arm an Kohlenhydraten sind, werden als mögliche Strategie untersucht, Tumoren durch Änderung der Brennstoffquelle des Körpers „auszuhungern“. Diese Studie zeigt, dass bei einer wichtigen Untergruppe von Leberkrebs eine häufige genetische Veränderung Tumorzellen befähigt, Ketonkörper als Energie- und Wachstumsquelle zu kapern. Anstatt durch eine ketogene Diät geschwächt zu werden, können diese Krebsarten dadurch tatsächlich schwerer zu behandeln sein und eher streuen, was verdeutlicht, dass diätbasierte Krebstherapien an die Biologie des jeweiligen Tumors angepasst werden müssen.
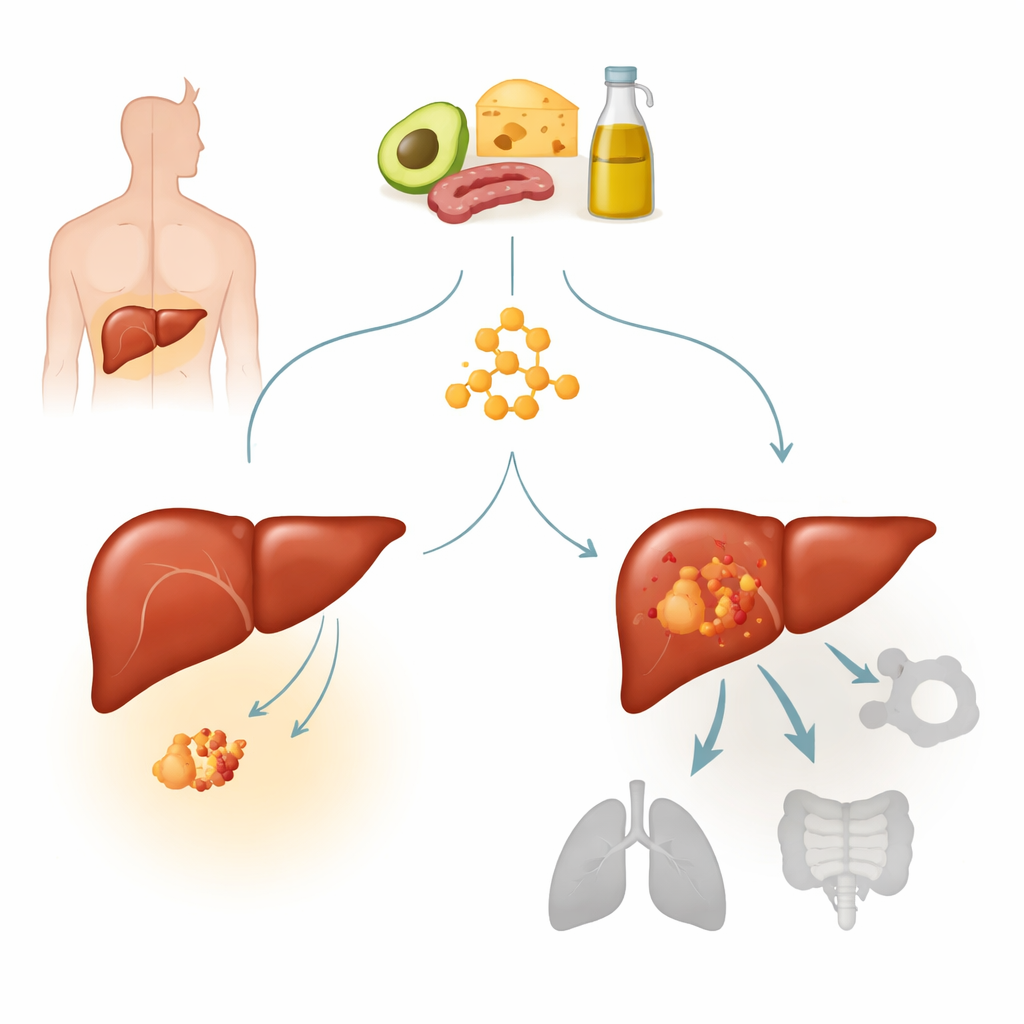
Ein genauerer Blick auf Leberkrebs und eine Schlüsselmuta tion
Das hepatozelluläre Karzinom ist die häufigste Form von Leberkrebs und eine führende Krebstodesursache weltweit. Viele dieser Tumoren tragen aktivierende Mutationen in einem Gen namens β‑Catenin, das normalerweise die Zellwachstumskontrolle und Signalantworten steuert. Eine Hotspot‑Mutation, bezeichnet als S33Y, hält den β‑Catenin‑Signalweg dauerhaft aktiviert und definiert einen eigenen Subtyp von Leberkrebs. Die Autorinnen und Autoren hatten zuvor festgestellt, dass Tumoren mit ausgeprägtem Ketonkörperstoffwechsel weniger auf ketogene Diäten ansprachen. Hier konzentrierten sie sich auf β‑Catenin‑mutierte Tumoren, um zu klären, ob diese Mutation Leberkrebse intrinsisch resistent gegen ketogene Therapie macht und, falls ja, wie.
Wenn eine „zuckerarme“ Diät Tumoren nicht verlangsamt
An Humanleberkrebszellen, die in Mäusen wuchsen, verglichen die Forschenden Tumoren mit und ohne die S33Y‑β‑Catenin‑Mutation unter normaler bzw. ketogener Diät. Bei Tumoren ohne Mutation verlangsamte die ketogene Diät deutlich das Wachstum: Die Tumoren waren kleiner und leichter, obwohl die Tiere ihr Körpergewicht hielten und wie erwartet ein Anstieg der Blutketone und ein Abfall des Blutzuckers zu beobachten war. Ganz im Gegensatz dazu wuchsen von der β‑Catenin‑Mutation getriebene Tumoren unter beiden Diäten aggressiv und zeigten keinen Nutzen von der ketogenen Ernährung. Ein ähnliches Muster beobachtete das Team in patientenabgeleiteten Tumortransplantaten: Ketogene Ernährung verkleinerte β‑Catenin‑normale Tumoren, bremste jedoch nicht das Wachstum von β‑Catenin‑mutierten Tumoren, was auf echte Resistenz statt auf ein modellabhängiges Phänomen hinweist.
Wie Krebszellen Ketone in Wachstumsbrennstoff verwandeln
Um diese Resistenz zu verstehen, untersuchten die Autorinnen und Autoren, wie mutiertes β‑Catenin die Ketoneverwertung in Krebszellen umgestaltet. Sie fokussierten auf OXCT1, das Schlüsselenzym, das Zellen den Abbau von Ketonkörpern ermöglicht — ein Prozess, der im gesunden Lebergewebe normalerweise minimal ist. β‑Catenin‑mutierte Zellen erhöhten OXCT1‑Level und andere ketonassoziierte Enzyme stark, und metabolische Verfolgung mit markierten Ketonkörpern zeigte, dass diese Zellen Ketone effizient in Glutamat umwandelten, einen wichtigen Baustein und Energiespender. Detaillierte molekulare Experimente zeigten, dass mutiertes β‑Catenin mit einem Partnerprotein, LEF1, zusammenarbeitet, um an die Kontrollregion des OXCT1‑Gens zu binden und dessen Expression zu aktivieren. Die Blockade von OXCT1 in mutierten Tumoren verringerte die Glutamatproduktion und hob ihre Resistenz gegenüber der ketogenen Diät auf, was darauf hindeutet, dass dieses Enzym einen kritischen metabolischen „Schalter“ darstellt.
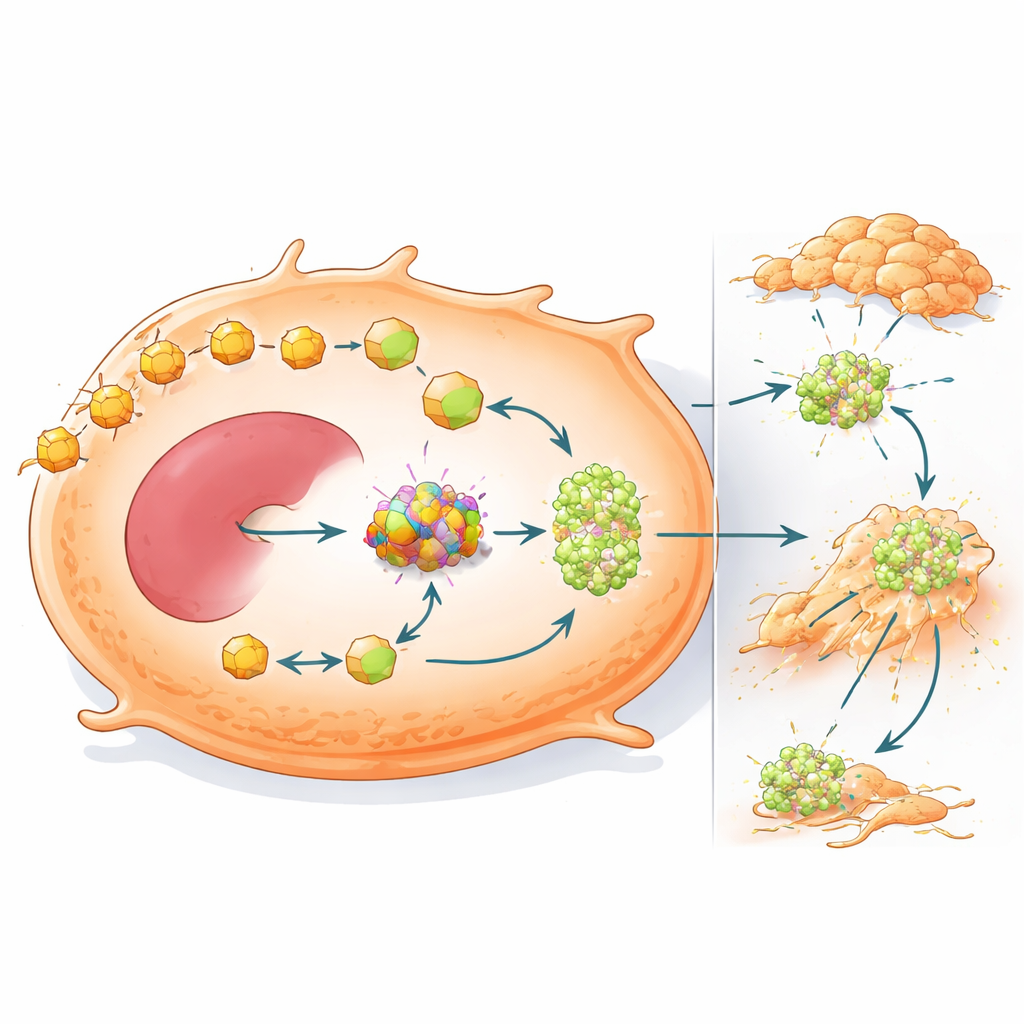
Umgeschaltete Brennstoffnutzung treibt auch die Metastasierung voran
Die Studie zeigt außerdem, dass OXCT1 mehr leistet als Tumoren das Überleben in kohlenhydratarmen Umgebungen zu ermöglichen — es macht sie auch metastasenfreudiger. Wenn OXCT1 in Leberkrebszellen erhöht wurde, migrierten und invasierten sie im Laborversuch aggressiver und bildeten in den Lebern von Mäusen mehr metastatische Herde. Genanalysen verbanden hohe OXCT1‑Werte mit Aktivierung eines Signalmoleküls namens STAT3 und mit einem epithelial‑mesenchymalen Übergangsprogramm, bei dem Zellen ihre Haftung lockern und einen mobileren, invasiveren Zustand erlangen. In Tieren wiesen β‑Catenin‑mutierte Tumoren starke STAT3‑Aktivierung und umfangreiche Metastasierung auf, doch die Herunterregulierung von OXCT1 kehrte diese Veränderungen weitgehend um und reduzierte sowohl Leber‑ als auch Lungenbesiedlung.
Was das für ketogene Therapie bedeutet
Einfach gesagt zeigt diese Arbeit, dass einige Leberkrebse mit einer häufigen β‑Catenin‑Mutation ketogene Therapie ins Gegenteil verkehren können. Anstatt ihnen bei Kohlenhydratmangel den Brennstoff zu entziehen, aktivieren diese Tumoren OXCT1, verbrennen Ketonkörper, wandeln sie in wachstumsfördernde Moleküle um und schalten Signalwege an, die das Streuen begünstigen. Folglich können ketogene Diäten allein für Patientinnen und Patienten mit diesem Tumorsubtyp riskant oder unwirksam sein. Die Ergebnisse legen nahe, Tumoren auf β‑Catenin‑ und OXCT1‑Status zu testen und Medikamente zu entwickeln, die OXCT1 blockieren, um diätbasierte Strategien sicherer und effektiver zu machen, indem verhindert wird, dass Tumoren eine beabsichtigte Therapie zu ihrem Vorteil nutzen.
Zitation: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Schlüsselwörter: ketogene Diät, Leberkrebs, β‑Catenin‑Mutation, Tumorstoffwechsel, OXCT1