Clear Sky Science · fr
La mutation de β-caténine reprogramme le métabolisme des corps cétoniques pour favoriser la métastase du carcinome hépatocellulaire et la résistance à la thérapie cétogène via l’activation transcriptionnelle d’OXCT1
Pourquoi cela compte pour le cancer et l’alimentation
Les régimes cétogènes, riches en graisses et très pauvres en glucides, sont étudiés comme moyen de « priver » les tumeurs en modifiant le carburant utilisé par l’organisme. Cette étude montre que, pour un sous‑groupe important de cancers du foie, une altération génétique courante permet aux cellules tumorales de détourner les corps cétoniques pour en faire une source d’énergie et de croissance. Plutôt que d’être affaiblies par un régime cétogène, ces tumeurs peuvent devenir plus difficiles à traiter et plus susceptibles de se propager, soulignant la nécessité d’adapter les approches alimentaires à la biologie de chaque tumeur.
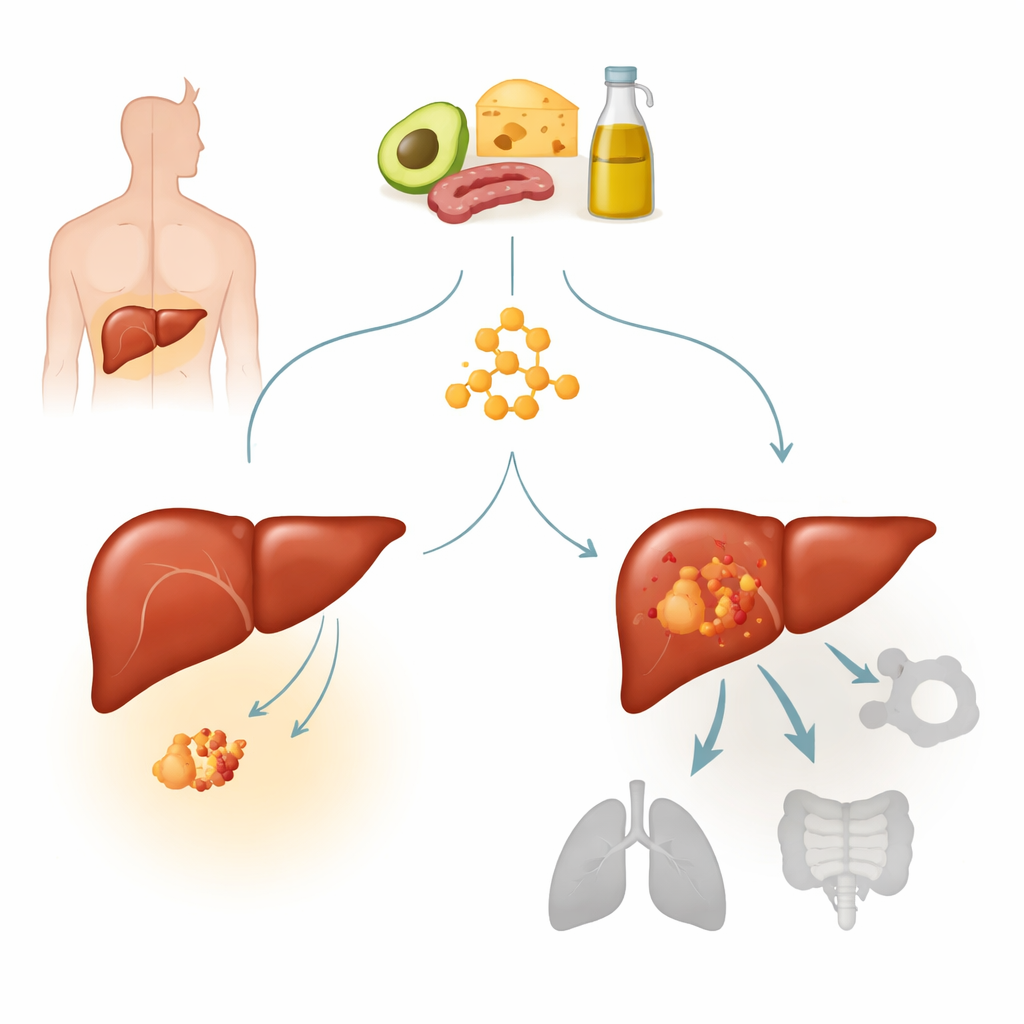
Un examen approfondi du cancer du foie et d’une mutation clé
Le carcinome hépatocellulaire est la forme la plus fréquente de cancer du foie et une cause majeure de décès par cancer dans le monde. Beaucoup de ces tumeurs portent des mutations activatrices dans un gène appelé bêta‑caténine, qui régule normalement la croissance cellulaire et la réponse aux signaux. Une mutation récurrente, nommée S33Y, maintient la voie de la bêta‑caténine constamment activée et définit un sous‑type distinct de cancer du foie. Les auteurs avaient précédemment observé que les tumeurs présentant un métabolisme des corps cétoniques élevé semblaient moins sensibles aux régimes cétogènes. Ici, ils se sont concentrés sur les tumeurs porteuses de la mutation de la bêta‑caténine pour déterminer si cette mutation rend intrinsèquement ces cancers résistants à la thérapie cétogène et, le cas échéant, par quels mécanismes.
Quand un régime « pauvre en sucre » n’arrête pas les tumeurs
En utilisant des cellules humaines de cancer du foie implantées chez la souris, les chercheurs ont comparé des tumeurs avec et sans la mutation S33Y de la bêta‑caténine sous un régime normal ou un régime cétogène. Dans les tumeurs sans la mutation, le régime cétogène ralentissait clairement la croissance : les tumeurs étaient plus petites et plus légères, bien que les animaux aient maintenu leur poids et présenté l’augmentation attendue des cétones sanguines et la baisse de la glycémie. En net contraste, les tumeurs porteuses de la mutation de la bêta‑caténine croissaient de manière agressive sous les deux régimes et ne tiraient aucun bénéfice du protocole cétogène. Les auteurs ont observé un schéma similaire dans des greffes tumorales dérivées de patients : l’alimentation cétogène réduisait les tumeurs sans mutation de la bêta‑caténine mais n’entravait pas la croissance des tumeurs mutées, indiquant une résistance réelle plutôt qu’un artefact lié au modèle.
Comment les cellules cancéreuses transforment les cétones en carburant de croissance
Pour comprendre cette résistance, les auteurs ont examiné comment la bêta‑caténine mutée modifie la gestion des cétones à l’intérieur des cellules tumorales. Ils se sont concentrés sur OXCT1, l’enzyme principale permettant la dégradation des corps cétoniques — un processus normalement faible dans le tissu hépatique sain. Les cellules mutées pour la bêta‑caténine augmentaient fortement les niveaux d’OXCT1 et d’autres enzymes liées aux cétones, et le suivi métabolique avec des cétones marquées a montré que ces cellules convertissaient efficacement les cétones en glutamate, un élément clé de construction et une source d’énergie. Des expériences moléculaires détaillées ont révélé que la bêta‑caténine mutante s’associe à une protéine partenaire, LEF1, pour se lier à la région régulatrice du gène OXCT1 et l’activer. Bloquer OXCT1 dans les tumeurs mutantes a réduit la production de glutamate et levé leur résistance au régime cétogène, indiquant que cette enzyme constitue un « interrupteur » métabolique critique.
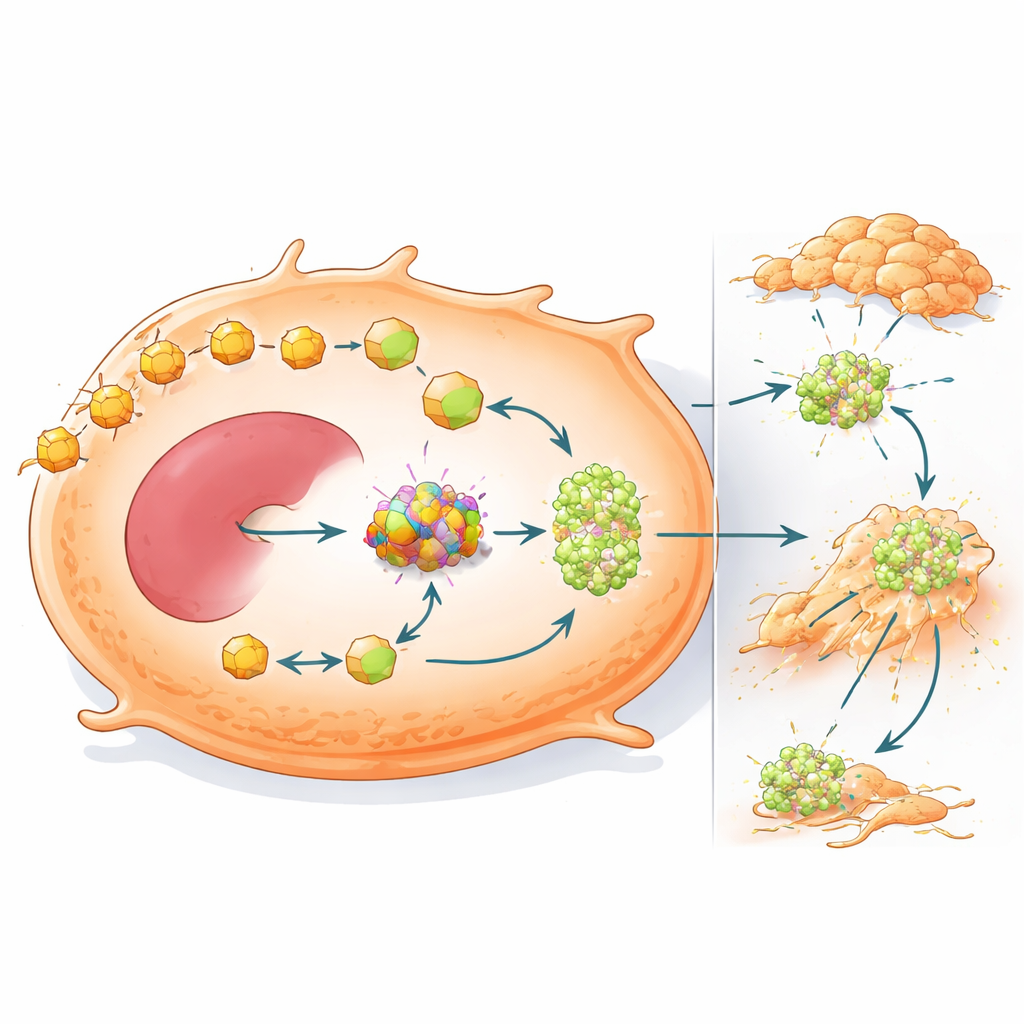
La réorientation du carburant favorise aussi la dissémination tumorale
L’étude montre en outre qu’OXCT1 fait plus que permettre aux tumeurs de survivre en faible consommation de glucides : il les rend aussi plus aptes à se propager. Lorsque OXCT1 était surexprimé dans des cellules de cancer du foie, elles migraient et envahissaient les tissus environnants de manière plus agressive lors d’essais in vitro et formaient davantage de nodules métastatiques dans le foie des souris. Les analyses génomiques ont relié un niveau élevé d’OXCT1 à l’activation d’une protéine de signalisation, STAT3, et à un programme d’épithélio‑mésenchymal transition (EMT), dans lequel les cellules perdent leurs attachements et acquièrent un état plus mobile et invasif. Chez l’animal, les tumeurs porteuses de la mutation de la bêta‑caténine présentaient une forte activation de STAT3 et des métastases étendues, mais l’inhibition d’OXCT1 a largement inversé ces changements et réduit la colonisation du foie et des poumons.
Ce que cela implique pour la thérapie cétogène
En termes pratiques, ce travail montre que certains cancers du foie porteurs d’une mutation fréquente de la bêta‑caténine peuvent retourner la thérapie cétogène contre le patient. Au lieu d’être privés de carburant lorsque les glucides se raréfient, ces tumeurs activent OXCT1 pour brûler les corps cétoniques, les convertir en molécules favorables à la croissance et activer des voies qui facilitent la dissémination. Par conséquent, les régimes cétogènes seuls peuvent être risqués ou inefficaces pour les patients atteints de ce sous‑type tumoral. Ces résultats suggèrent que le typage des tumeurs pour la bêta‑caténine et OXCT1, ainsi que le développement de médicaments bloquant OXCT1, pourraient rendre les stratégies basées sur l’alimentation plus sûres et plus efficaces en empêchant les cancers de transformer une thérapie prévue en avantage.»}
Citation: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Mots-clés: régime cétogène, cancer du foie, mutation de la bêta-caténine, métabolisme tumoral, OXCT1