Clear Sky Science · it
La mutazione di β-catenina riprogramma il metabolismo dei corpi chetonici per guidare la metastasi dell’epatocarcinoma e la resistenza alla terapia chetogenica tramite l’attivazione trascrizionale di OXCT1
Perché è importante per cancro e dieta
Le diete chetogeniche, ricche di grassi e molto povere di carboidrati, vengono esplorate come modo per “affamare” i tumori modificando il combustibile che l’organismo utilizza. Questo studio mostra che, per un sottogruppo importante di tumori epatici, una comune alterazione genetica permette alle cellule tumorali di dirottare i corpi chetonici come fonte di energia e di crescita. Invece di essere indeboliti da una dieta chetogenica, questi tumori possono diventare più difficili da trattare e più inclini a diffondersi, sottolineando perché le terapie oncologiche basate sulla dieta devono essere adattate alla biologia specifica di ogni tumore.
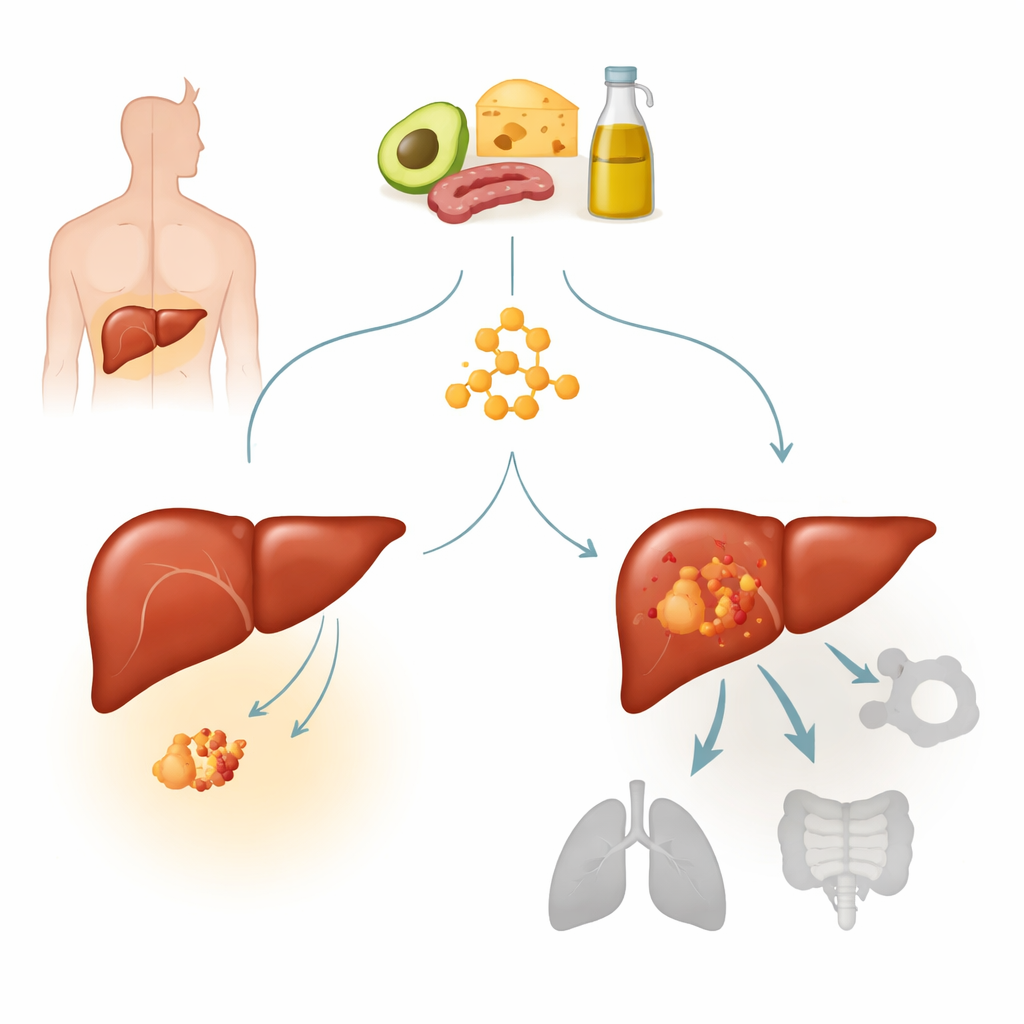
Uno sguardo più ravvicinato al cancro al fegato e a una mutazione chiave
L’epatocarcinoma è la forma più comune di cancro al fegato ed è una delle principali cause di morte per cancro nel mondo. Molti di questi tumori presentano mutazioni attivanti in un gene chiamato beta-catenina, che normalmente contribuisce a controllare la crescita cellulare e la risposta ai segnali. Una mutazione hotspot, denominata S33Y, mantiene il percorso della beta-catenina acceso in modo permanente e definisce un sottotipo distinto di tumore epatico. Gli autori avevano precedentemente osservato che i tumori con forte metabolismo dei corpi chetonici sembravano meno sensibili alle diete chetogeniche. In questo lavoro si sono concentrati sui tumori con mutazione di beta-catenina per chiedersi se tale mutazione renda intrinsecamente resistenti i carcinomi epatici alla terapia chetogenica e, in caso affermativo, in che modo.
Quando una dieta “a basso contenuto di zuccheri” non arresta i tumori
Utilizzando cellule umane di cancro al fegato coltivate in topi, i ricercatori hanno confrontato tumori con e senza la mutazione S33Y della beta-catenina sotto una dieta normale o una dieta chetogenica. Nei tumori privi della mutazione, la dieta chetogenica ha chiaramente rallentato la crescita: i tumori erano più piccoli e pesavano meno, nonostante gli animali mantenessero il peso corporeo e mostrassero il previsto aumento dei chetoni nel sangue e la riduzione della glicemia. In netto contrasto, i tumori guidati dalla mutazione di beta-catenina crescevano in modo aggressivo con entrambe le diete e non hanno tratto beneficio dalla dieta chetogenica. Il gruppo ha osservato un pattern simile nei trapianti di tumore epatico derivati da pazienti: l’alimentazione chetogenica riduceva i tumori con beta-catenina normale ma non frenava la crescita dei tumori con beta-catenina mutata, indicando una vera resistenza piuttosto che un effetto specifico del modello sperimentale.
Come le cellule tumorali trasformano i chetoni in combustibile per la crescita
Per comprendere questa resistenza, gli autori hanno esaminato come la beta-catenina mutata rimodelli la gestione dei chetoni nelle cellule tumorali. Si sono concentrati su OXCT1, l’enzima principale che consente alle cellule di degradare i corpi chetonici—un processo normalmente minimo nel tessuto epatico sano. Le cellule con beta-catenina mutata hanno aumentato fortemente i livelli di OXCT1 e di altri enzimi legati ai chetoni, e il tracciamento metabolico con corpi chetonici marcati ha mostrato che queste cellule convertivano in modo efficiente i chetoni in glutammato, un importante mattoncino e fonte di energia. Esperimenti molecolari dettagliati hanno rivelato che la beta-catenina mutata si allea con una proteina partner, LEF1, per legarsi alla regione di controllo del gene OXCT1 e attivarla. Bloccare OXCT1 nei tumori mutati ha ridotto la produzione di glutammato e ha eliminato la loro resistenza alla dieta chetogenica, indicando che questo enzima è un “interruttore” metabolico critico.
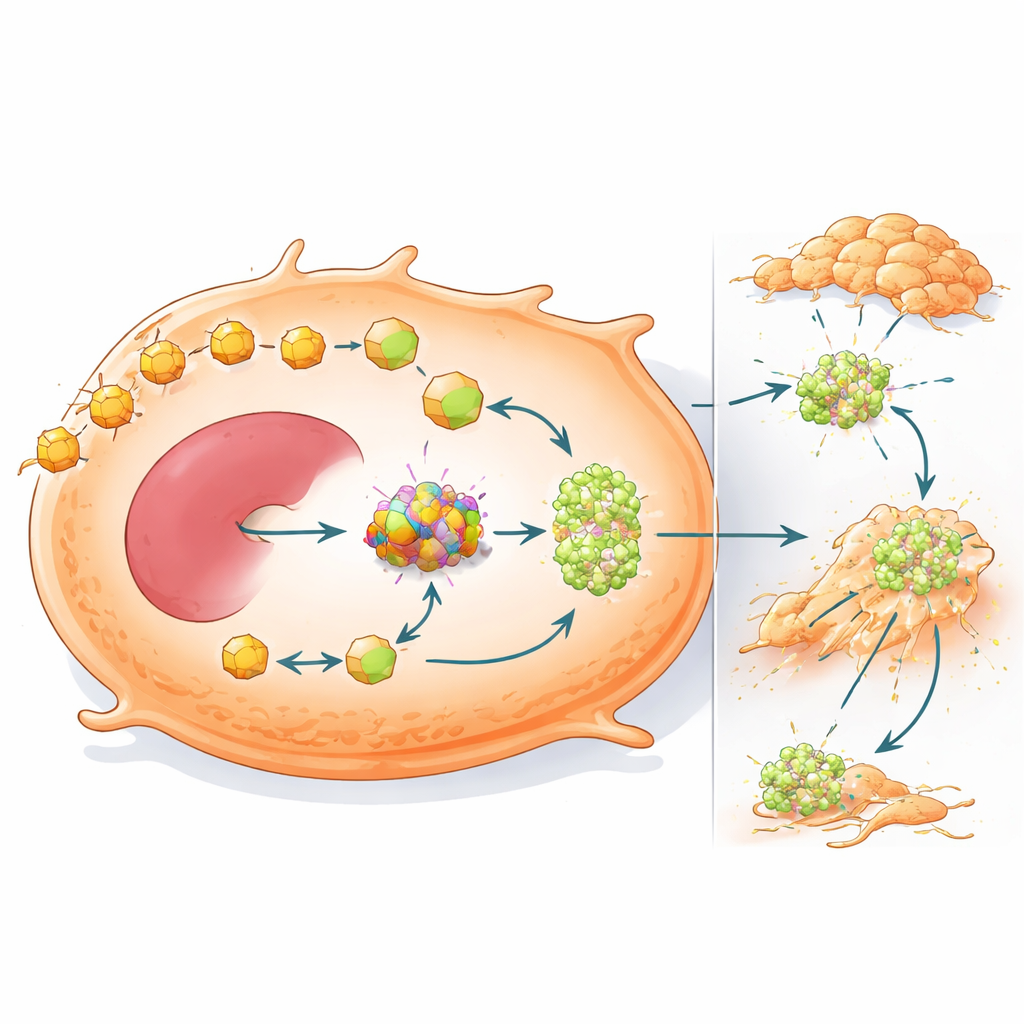
L’uso riprogrammato del combustibile favorisce anche la diffusione del cancro
Lo studio mostra inoltre che OXCT1 fa più che aiutare i tumori a sopravvivere in un ambiente povero di carboidrati—li rende anche più propensi a metastatizzare. Quando OXCT1 è stato aumentato nelle cellule di cancro al fegato, queste migravano e invadevano il tessuto circostante in modo più aggressivo nei test in vitro e hanno formato più noduli metastatici nei fegati dei topi. Analisi geniche hanno collegato livelli elevati di OXCT1 all’attivazione di una proteina di segnalazione chiamata STAT3 e a un programma di transizione epiteliale–mesenchimale, nel quale le cellule allentano le loro adesioni e acquisiscono uno stato più mobile e invasivo. Negli animali, i tumori con beta-catenina mutata mostravano forte attivazione di STAT3 ed estese metastasi, ma l’abbassamento di OXCT1 ha in gran parte invertito questi cambiamenti e ridotto sia la colonizzazione epatica sia quella polmonare.
Implicazioni per la terapia chetogenica
In termini pratici, questo lavoro mostra che alcuni tumori epatici portatori di una comune mutazione di beta-catenina possono ribaltare l’effetto atteso della terapia chetogenica. Invece di essere privati di combustibile quando i carboidrati scarseggiano, questi tumori attivano OXCT1 per bruciare i corpi chetonici, trasformarli in molecole che favoriscono la crescita e attivare vie che ne facilitano la diffusione. Di conseguenza, le diete chetogeniche da sole possono essere rischiose o inefficaci per i pazienti con questo sottotipo tumorale. I risultati suggeriscono che testare i tumori per lo stato di beta-catenina e OXCT1, e sviluppare farmaci che blocchino OXCT1, potrebbe rendere le strategie basate sulla dieta più sicure ed efficaci impedendo ai tumori di trasformare una terapia prevista in un vantaggio.
Citazione: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Parole chiave: dieta chetogenica, cancro al fegato, mutazione di beta-catenina, metabolismo tumorale, OXCT1