Clear Sky Science · tr
β-katenin mutasyonu, OXCT1’in transkripsiyonel aktivasyonu yoluyla keton cisimciği metabolizmasını yeniden programlayarak hepatosellüler karsinom metastazını ve ketojenik tedaviye direnci tetikliyor
Kanser ve diyet açısından neden önemli
Yağ açısından yüksek ve karbonhidrat açısından çok düşük olan ketojenik diyetler, vücudun kullandığı yakıtı değiştirerek tümörleri “aç bırakma” yolu olarak araştırılıyor. Bu çalışma, önemli bir karaciğer kanseri alt grubu için yaygın bir genetik değişikliğin tümör hücrelerinin keton cisimlerini enerji ve büyüme kaynağı olarak kullanmasını sağladığını gösteriyor. Ketojenik diyetle zayıflamak yerine, bu kanserler tedaviye daha dirençli ve yayılmaya daha yatkın hale gelebilir; bu da diyet temelli kanser terapilerinin her tümörün biyolojisine göre eşleştirilmesi gerektiğini vurguluyor.
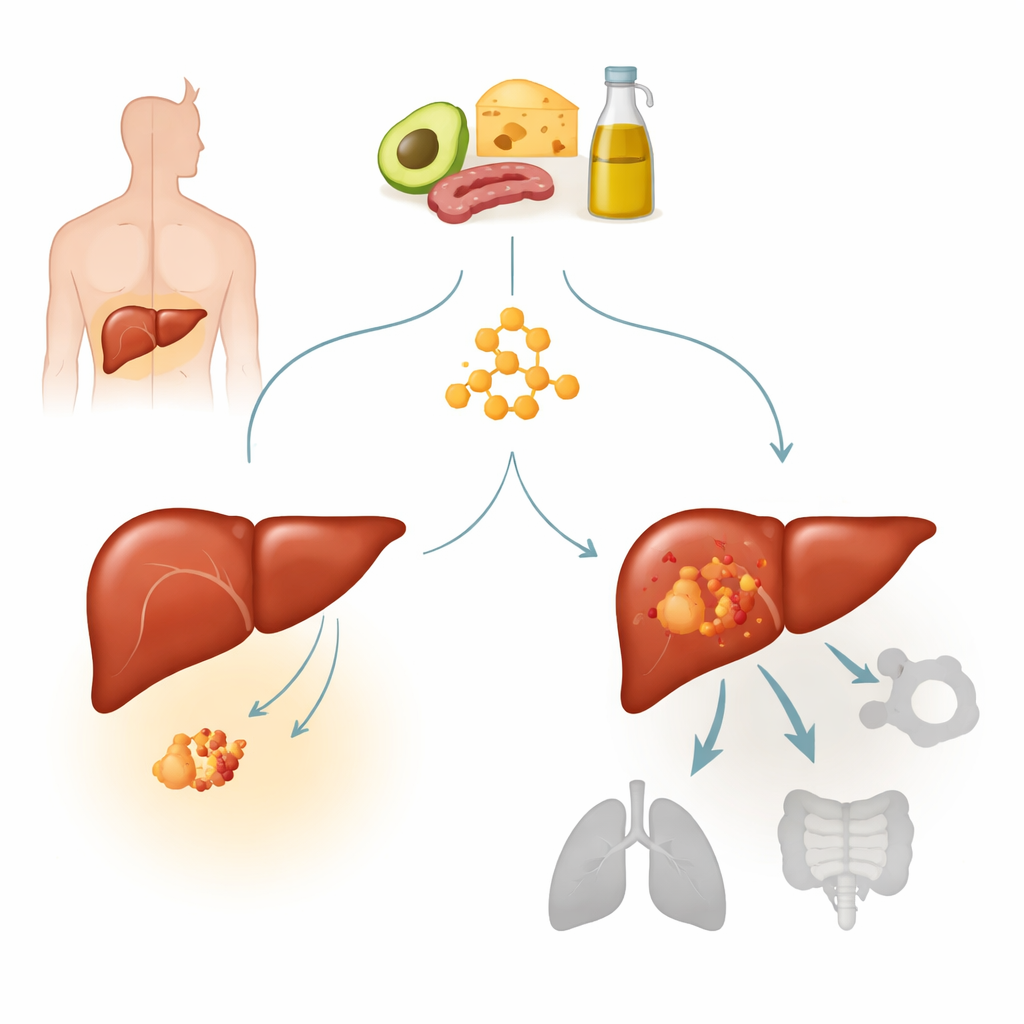
Karaciğer kanseri ve kilit bir mutasyona daha yakından bakış
Hepatosellüler karsinom, karaciğer kanserinin en yaygın formu olup dünya genelinde kanser ölümlerinin önde gelen nedenlerinden biridir. Bu tümörlerin birçoğu, hücrelerin nasıl büyüdüğünü ve sinyallere nasıl yanıt verdiğini normalde düzenlemeye yardımcı olan beta-katenin adlı bir gende aktifleştirici mutasyonlar taşır. S33Y olarak adlandırılan bir hotspot mutasyon, beta-katenin yolunu kalıcı olarak açık tutar ve belirgin bir karaciğer kanseri alt tipini tanımlar. Yazarlar daha önce güçlü keton cisimciği metabolizmasına sahip tümörlerin ketojenik diyetlere daha az yanıt verdiğini bulmuşlardı. Burada, beta-katenin mutant tümörlerin bu mutasyonun karaciğer kanserlerini ketojenik tedaviye doğuştan dirençli kılıp kılmadığını ve eğer öyleyse bunun nasıl olduğunu sorguladılar.
“Düşük şeker” diyetinin tümörleri yavaşlatmada başarısız olduğu durum
Araştırmacılar, farelerde büyütülen insan karaciğer kanseri hücrelerini kullanarak S33Y beta-katenin mutasyonuna sahip ve olmayan tümörleri normal diyet veya ketojenik diyet altında karşılaştırdı. Mutasyonu olmayan tümörlerde ketojenik diyet belirgin şekilde büyümeyi yavaşlattı: tümörler daha küçük ve daha hafifti; hayvanlar vücut ağırlığını korurken kanda beklenen keton yükselmesi ve kan şekeri düşüşü görüldü. Keskin bir tezat olarak, beta-katenin mutasyonu tarafından yönlendirilen tümörler her iki diyet altında da agresifçe büyüdü ve ketojenik rejimden hiçbir yarar görmedi. Araştırma ekibi, hasta kaynaklı karaciğer tümör greftlerinde benzer bir desen gözlemledi: ketojenik beslenme beta-katenin normal tümörlerini küçülttü ancak beta-katenin mutant tümörlerin büyümesini engellemedi; bu durum model-özgü bir etki değil, gerçek bir direnç olduğunu gösteriyor.
Kanser hücreleri ketonları nasıl büyüme yakıtına çevirir
Bu direnci anlamak için yazarlar, mutasyona uğramış beta-kateninin kanser hücreleri içinde keton işleyişini nasıl yeniden şekillendirdiğini inceledi. Sağlıklı karaciğer dokusunda normalde minimal olan keton cisimciği yıkımını sağlayan ana enzim OXCT1’e odaklandılar. Beta-katenin mutant hücreler OXCT1 düzeylerini ve diğer ketonla ilişkili enzimleri güçlü şekilde artırdı; etiketli keton cisimcikleriyle yapılan metabolik izlemeler bu hücrelerin ketonları verimli biçimde glutamata çevirdiğini gösterdi; glutamat hem temel bir yapı taşı hem de enerji kaynağıdır. Ayrıntılı moleküler deneyler, mutant beta-kateninin bir ortak protein olan LEF1 ile işbirliği yapıp OXCT1 geninin kontrol bölgesine bağlanarak onu açtığını ortaya koydu. Mutant tümörlerde OXCT1’i engellemek glutamat üretimini azalttı ve ketojenik diyete karşı dirençlerini ortadan kaldırdı; bu da bu enzimin kritik bir metabolik “anahtar” olduğunu gösteriyor.
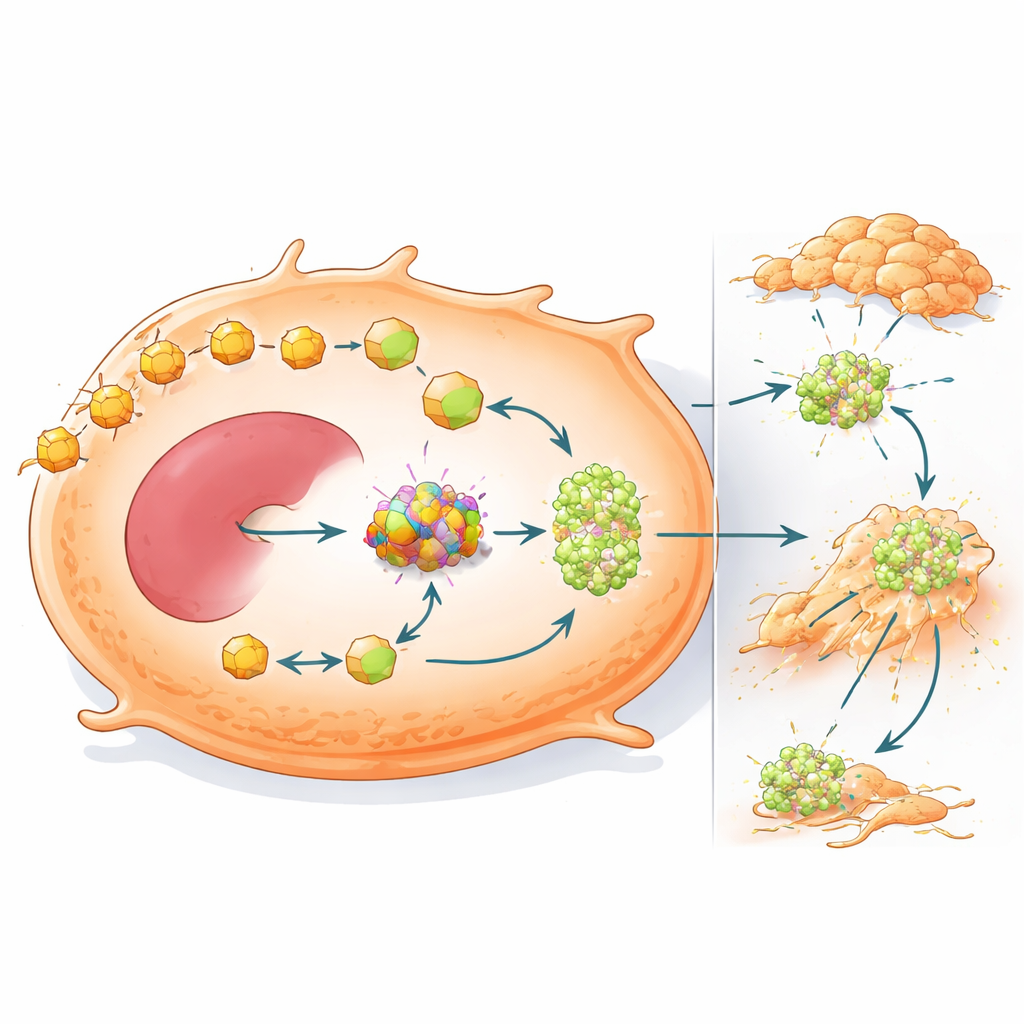
Yeniden kablolanmış yakıt kullanımı aynı zamanda kanserin yayılmasını da tetikliyor
Çalışma ayrıca OXCT1’in sadece düşük karbonhidrat ortamında tümörlerin hayatta kalmasına yardımcı olmakla kalmayıp aynı zamanda bunların daha kolay yayılmasını da sağladığını gösteriyor. OXCT1 karaciğer kanseri hücrelerinde yükseltildiğinde, bu hücreler laboratuvar testlerinde çevre dokuları daha agresifce göç edip istila etti ve farelerin karaciğerlerinde daha fazla metastatik nodül oluşturdu. Gen analizleri yüksek OXCT1’i STAT3 adlı bir sinyal proteininin aktivasyonu ve hücrelerin bağlantılarını gevşetip daha hareketli, invaziv bir durumda olmalarını sağlayan epitel–mezenkimal geçiş programıyla ilişkilendirdi. Hayvanlarda beta-katenin mutant tümörler güçlü STAT3 aktivasyonu ve yaygın metastaz gösterdi; fakat OXCT1’in baskılanması bu değişiklikleri büyük ölçüde tersine çevirdi ve hem karaciğer hem de akciğer kolonizasyonunu azalttı.
Ketojenik terapi için ne anlama geliyor
Günlük ifadeyle, bu çalışma bazı karaciğer kanserlerinin yaygın bir beta-katenin mutasyonunu taşıması halinde ketojenik terapinin beklenen etkisini tersine çevirebileceğini gösteriyor. Karbonhidratlar kıt olduğunda yakıtı kesilmiş olmak yerine, bu tümörler OXCT1’i aktive ederek keton cisimciklerini yakar, onları büyümeyi destekleyen moleküllere dönüştürür ve yayılmalarına yardımcı olan yolakları devreye sokar. Sonuç olarak, ketojenik diyetler tek başına bu tümör alt tipi olan hastalar için riskli veya etkisiz olabilir. Bulgular, tümörlerin beta-katenin ve OXCT1 durumunun test edilmesini ve OXCT1’i hedef alan ilaçların geliştirilmesini öneriyor; bu yaklaşım, diyet temelli stratejilerin kanserlerin niyet edilen bir terapiyi avantaja çevirmesini önleyerek daha güvenli ve etkili olmasını sağlayabilir.
Atıf: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Anahtar kelimeler: ketojenik diyet, karaciğer kanseri, beta-katenin mutasyonu, tümör metabolizması, OXCT1