Clear Sky Science · nl
β-catenine-mutatie herprogrammeert ketonlichaatmetabolisme om hepatocellulair carcinoom‑uitzaaiing en resistentie tegen ketogene therapie aan te jagen via transcriptie‑activatie van OXCT1
Waarom dit belangrijk is voor kanker en voeding
Ketogene diëten, die rijk zijn aan vet en zeer arm aan koolhydraten, worden onderzocht als manier om tumoren als het ware te "verhongeren" door te veranderen welke brandstof het lichaam gebruikt. Deze studie toont aan dat voor een belangrijke subgroep van leverkanker een veelvoorkomende genetische verandering tumorcellen in staat stelt ketonlichamen te kapen als energie‑ en groeibron. In plaats van verzwakt te worden door een ketogeen dieet, kunnen deze kankers juist moeilijker te behandelen zijn en eerder uitzaaien, wat benadrukt dat dieetgebaseerde kankertherapieën afgestemd moeten zijn op de biologie van elk afzonderlijk tumortype.
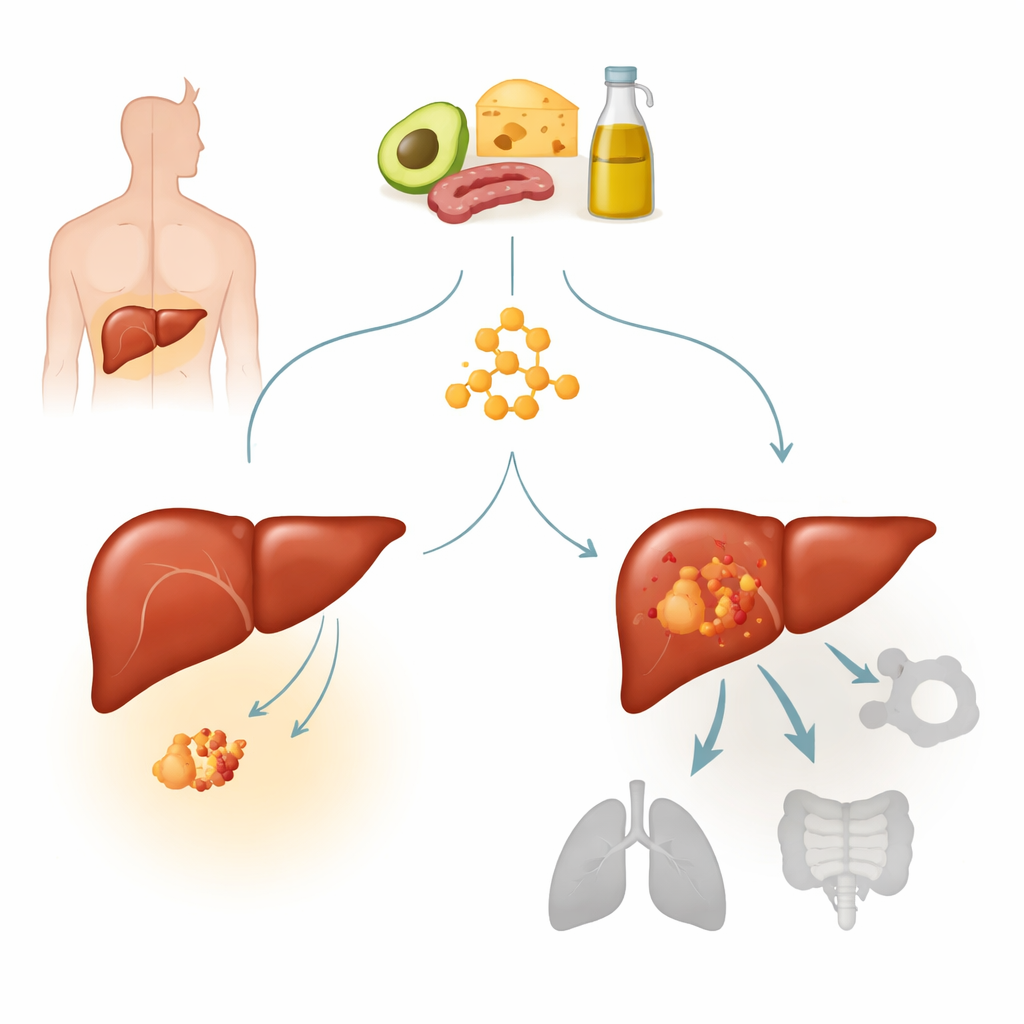
Een nadere blik op leverkanker en een sleutelmutatie
Hepatocellulair carcinoom is de meest voorkomende vorm van leverkanker en een belangrijke oorzaak van sterfte door kanker wereldwijd. Veel van deze tumoren dragen activerende mutaties in een gen dat beta‑catenine heet, dat normaal helpt bij het regelen van celgroei en respons op signalen. Eén veelvoorkomende hotspotmutatie, S33Y genoemd, houdt het beta‑cateninepad permanent ingeschakeld en definieert een distinct subtype van leverkanker. De auteurs hadden eerder gevonden dat tumoren met sterk ketonlichaatmetabolisme minder responsief leken op ketogene diëten. Hier concentreerden ze zich op beta‑catenine‑gemuteerde tumoren om te onderzoeken of deze mutatie leverkankers intrinsiek resistent maakt tegen ketogene behandeling en, zo ja, hoe dat werkt.
Wanneer een "laag‑suiker" dieet tumoren niet vertraagt
Met behulp van menselijke leverkankercellen die in muizen werden gekweekt, vergeleken de onderzoekers tumoren met en zonder de S33Y beta‑cateninemutatie onder ofwel een normaal dieet ofwel een ketogeen dieet. Bij tumoren zonder de mutatie vertraagde het ketogene dieet duidelijk de groei: tumoren waren kleiner en lichter, hoewel de dieren hun lichaamsgewicht behielden en de verwachte stijging van bloedketonen en daling van bloedsuiker lieten zien. In scherp contrast groeiden tumoren aangedreven door de beta‑cateninemutatie agressief onder beide diëten en vertoonden geen voordeel van het ketogene regime. Het team zag een vergelijkbaar patroon in patiëntafgeleide levertumortransplantaten: ketogene voeding verkleinde beta‑catenine‑normale tumoren maar remde de groei van beta‑catenine‑gemuteerde tumoren niet, wat wijst op echte resistentie in plaats van een model‑specifiek effect.
Hoe kankercellen ketonen veranderen in groeibrandstof
Om deze resistentie te begrijpen, onderzochten de auteurs hoe gemuteerd beta‑catenine het ketonbeheer binnen kankercellen herinricht. Ze richtten zich op OXCT1, het belangrijkste enzym waarmee cellen ketonlichamen afbreken—een proces dat normaal gesproken minimaal is in gezond leverweefsel. Beta‑catenine‑gemuteerde cellen verhoogden sterk OXCT1‑niveaus en andere ketongerelateerde enzymen, en metabolische tracering met gelabelde ketonlichamen toonde aan dat deze cellen ketonen efficiënt omzetten in glutamaat, een belangrijke bouwsteen en energiebron. Gedetailleerde moleculaire experimenten lieten zien dat gemuteerd beta‑catenine samenwerkt met een partnerproteïne, LEF1, om te binden aan het regelgebied van het OXCT1‑gen en het aan te zetten. Het blokkeren van OXCT1 in gemuteerde tumoren verminderde de glutamaatproductie en hief hun resistentie tegen het ketogene dieet op, wat aangeeft dat dit enzym een cruciale metabole "schakelaar" is.
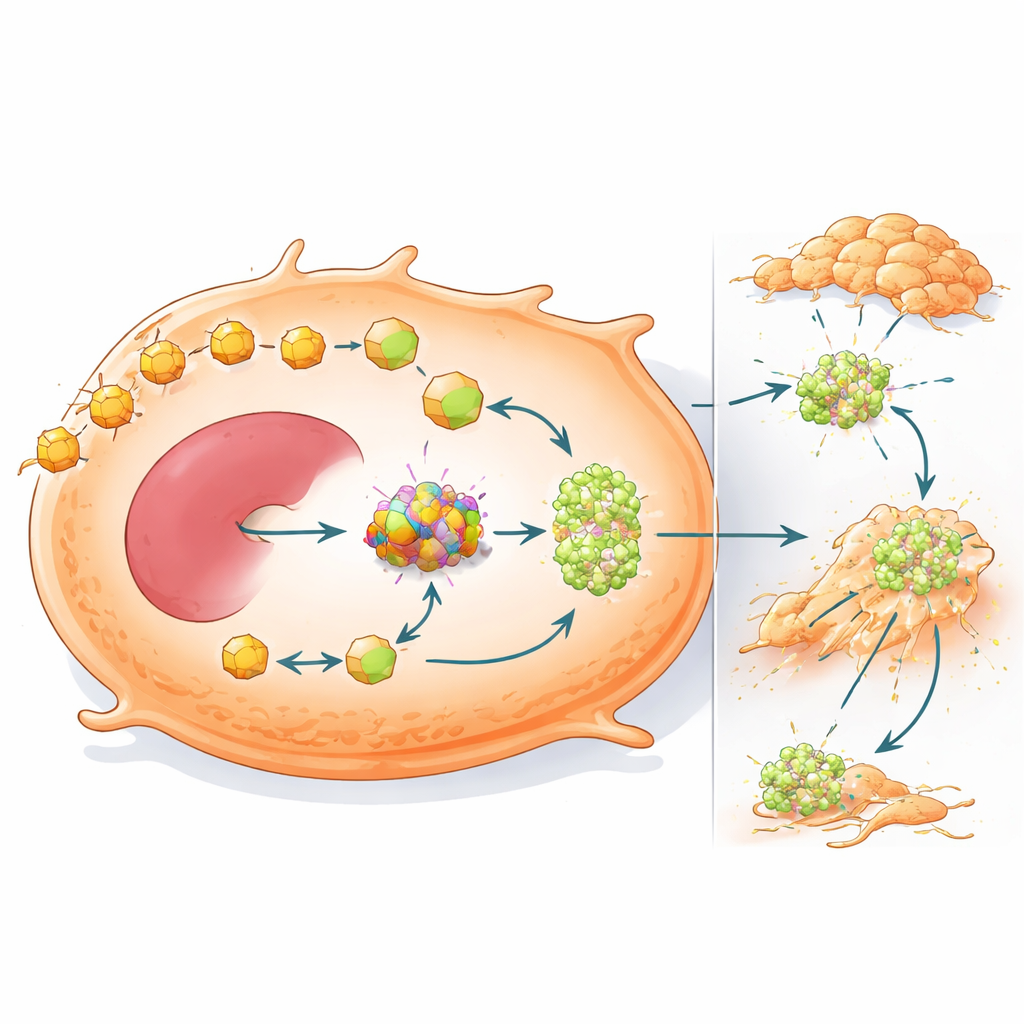
Hernieuwd brandstofgebruik bevordert ook kankerspreiding
De studie toont verder aan dat OXCT1 meer doet dan tumoren helpen overleven in een koolhydraatarme omgeving—het maakt ze ook gevoeliger voor uitzaaiing. Wanneer OXCT1 verhoogd werd in leverkankercellen, migreerden en infiltreerden ze omliggend weefsel agressiever in laboratoriumtesten en vormden ze meer metastatische noduli in de lever van muizen. Genanalyses koppelden hoge OXCT1 aan activatie van een signaalproteïne dat STAT3 heet en aan een epitheel‑mesenchymale overgangsroute, waarbij cellen hun hechting verzwakken en een mobieler, invasiever karakter krijgen. In dieren vertoonden beta‑catenine‑gemuteerde tumoren sterke STAT3‑activatie en uitgebreide metastasering, maar het onderdrukken van OXCT1 keerde deze veranderingen grotendeels om en verminderde zowel lever‑ als longkolonisatie.
Wat dit betekent voor ketogene therapie
In gewone bewoordingen toont dit werk aan dat sommige leverkankers met een veelvoorkomende beta‑cateninemutatie ketogene therapie kunnen omkeren. In plaats van brandstof te missen wanneer koolhydraten schaars zijn, schakelen deze tumoren OXCT1 aan om ketonlichamen te verbranden, ze om te zetten in groeiondersteunende moleculen en routes te activeren die hen helpen uit te zaaien. Daardoor kunnen ketogene diëten op zichzelf risicovol of ineffectief zijn voor patiënten met dit tumortype. De bevindingen suggereren dat het testen van tumoren op beta‑catenine‑ en OXCT1‑status, en het ontwikkelen van geneesmiddelen die OXCT1 blokkeren, dieetgebaseerde strategieën veiliger en effectiever zou kunnen maken door te voorkomen dat tumoren een bedoelde therapie in een voordeel veranderen.
Bronvermelding: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Trefwoorden: ketogeen dieet, leverkanker, beta‑cateninemutatie, tumormetabolisme, OXCT1