Clear Sky Science · ar
طفرة β‑catenin تُعيد برمجة أيض أجسام الكيتون لدفع نقيلة سرطان الكبد ومقاومة العلاج الكيتوني عبر تنشيط نسخي لـ OXCT1
لماذا يهم هذا بالنسبة للسرطان والنظام الغذائي
تُدرَس الحميات الكيتونية، الغنية بالدهون والمنخفضة جداً بالكربوهيدرات، كوسيلة لـ "تجويع" الأورام عبر تغيير الوقود الذي يستخدمه الجسم. تُظهر هذه الدراسة أن مجموعة مهمة من سرطانات الكبد تحمل تغيراً جينياً شائعاً يسمح لخلايا الورم بالاستيلاء على أجسام الكيتون كمصدر للطاقة والنمو. بدلاً من أن تضعف بفعل الحمية الكيتونية، قد تصبح هذه السرطانات في الواقع أصعب علاجاً وأكثر ميلاً للانتشار، ما يبرز سبب ضرورة موائمة العلاجات الغذائية مع بَيولوجيا كل ورم.
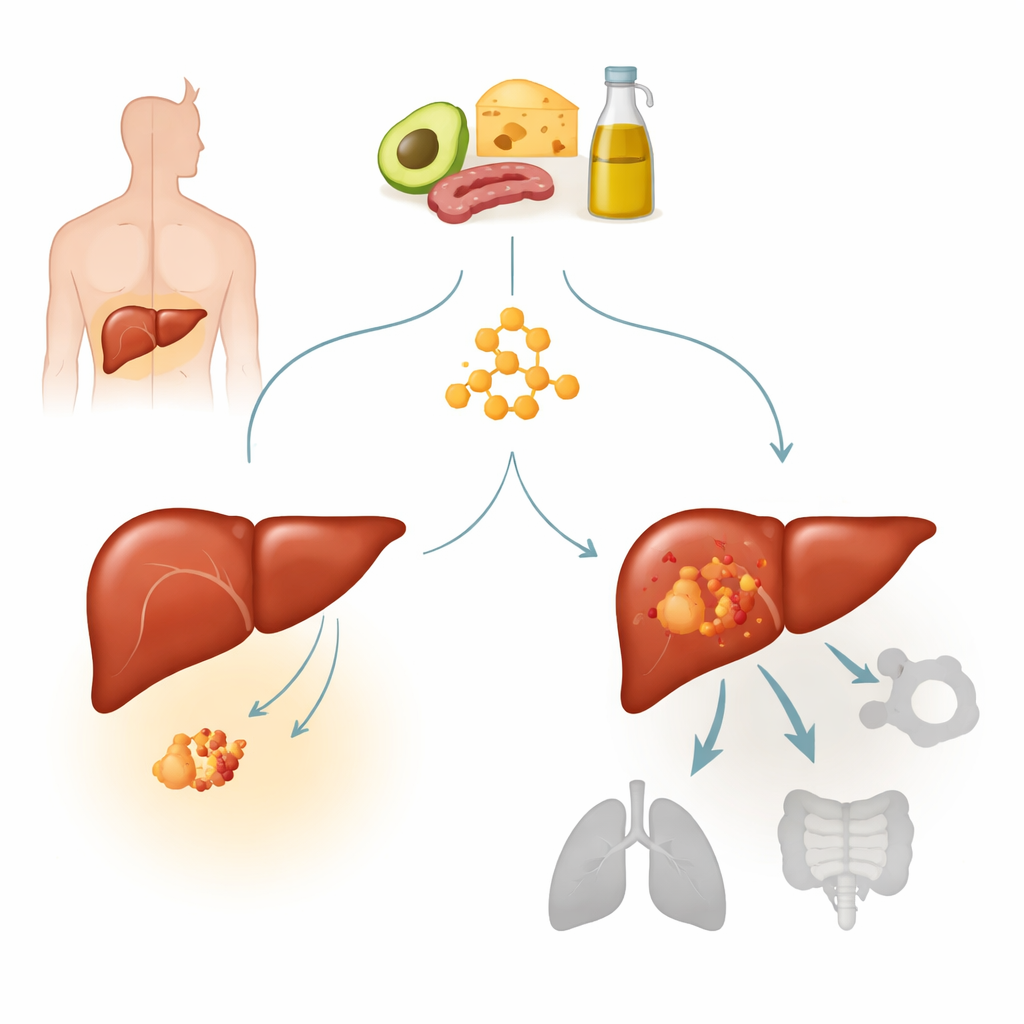
نظرة أقرب إلى سرطان الكبد وطفرة رئيسية
سرطان الخلايا الكبدية هو الشكل الأكثر شيوعاً لسرطان الكبد وسبب رئيسي للوفاة بالسرطان عالمياً. يحمل العديد من هذه الأورام طفرات منشِطة في جين يُدعى بيتا‑كاتينين، الذي يساعد عادة في التحكم في نمو الخلايا واستجابتها للإشارات. تحوّر رئيسي واحد، يسمى S33Y، يبقي مسار بيتا‑كاتينين مُنشّطاً بشكل دائم ويحدد نوعاً فرعياً مميزاً من سرطان الكبد. كان الباحثون قد وجدوا سابقاً أن الأورام ذات أيض أجسام الكيتون القوي بدت أقل استجابة للأنظمة الكيتونية. هنا، ركزوا على الأورام الحاملة لطيبة بيتا‑كاتينين ليسألوا ما إذا كانت هذه الطفرة تجعل سرطانات الكبد مقاومة بطبيعتها للعلاج الكيتوني وإذا كان الأمر كذلك، كيف يحدث ذلك.
عندما يفشل "النظام منخفض السكر" في إبطاء الأورام
باستخدام خلايا سرطان كبد بشري نمت في فئران، قارن الباحثون الأورام الحاملة وغير الحاملة لطفرة S33Y في بيتا‑كاتينين تحت حمية عادية أو حمية كيتونية. في الأورام من دون الطفرة، أبطأت الحمية الكيتونية النمو بوضوح: كانت الأورام أصغر وأخف وزناً، بالرغم من أن الحيوانات حافظت على وزن الجسم وأظهرت الارتفاع المتوقع في أجسام الكيتون وانخفاض السكر في الدم. على النقيض الحاد، نمت الأورام المدفوعة بطفرة بيتا‑كاتينين بشكل عدواني تحت كلا النظامين الغذائيين ولم تظهر أي استفادة من النظام الكيتوني. لوحظ نمط مماثل في زراعات أورام مأخوذة من مرضى: غذاء كيتوني قلّص أورام بيتا‑كاتينين الطبيعية لكنه لم يوقف نمو أورام بيتا‑كاتينين المتحولة، مما يشير إلى مقاومة حقيقية بدلاً من تأثير خاص بالنموذج التجريبي.
كيف تحول خلايا السرطان الكيتونات إلى وقود للنمو
لفهم هذه المقاومة، فحص المؤلفون كيف تعيد بيتا‑كاتينين المتحولة تشكيل تعامل الخلايا السرطانية مع الكيتونات. ركزوا على OXCT1، الإنزيم الرئيسي الذي يسمح للخلايا بتفكيك أجسام الكيتون—وهي عملية عادة ما تكون ضئيلة في نسيج الكبد السليم. زادت خلايا بيتا‑كاتينين المتحولة بشكل كبير مستويات OXCT1 وإنزيمات مرتبطة بالكيتون الأخرى، وأظهرت تجارب تتبع أيضية باستخدام أجسام كيتون معنونة أن هذه الخلايا تحوّل الكيتونات بكفاءة إلى جلوتمات، وهو لبِنَاء أساسي ومصدر طاقة. كشفت تجارب جزيئية مفصّلة أن بيتا‑كاتينين المتحولة تتعاون مع بروتين شريك، LEF1، للارتباط بمنطقة التحكم في جين OXCT1 وتشغيله. منع OXCT1 في الأورام المتحولة خفّض إنتاج الجلوتمات وأزال مقاومتها للنظام الكيتوني، مما يشير إلى أن هذا الإنزيم يعمل كـ "مفتاح" أيضي حاسم.
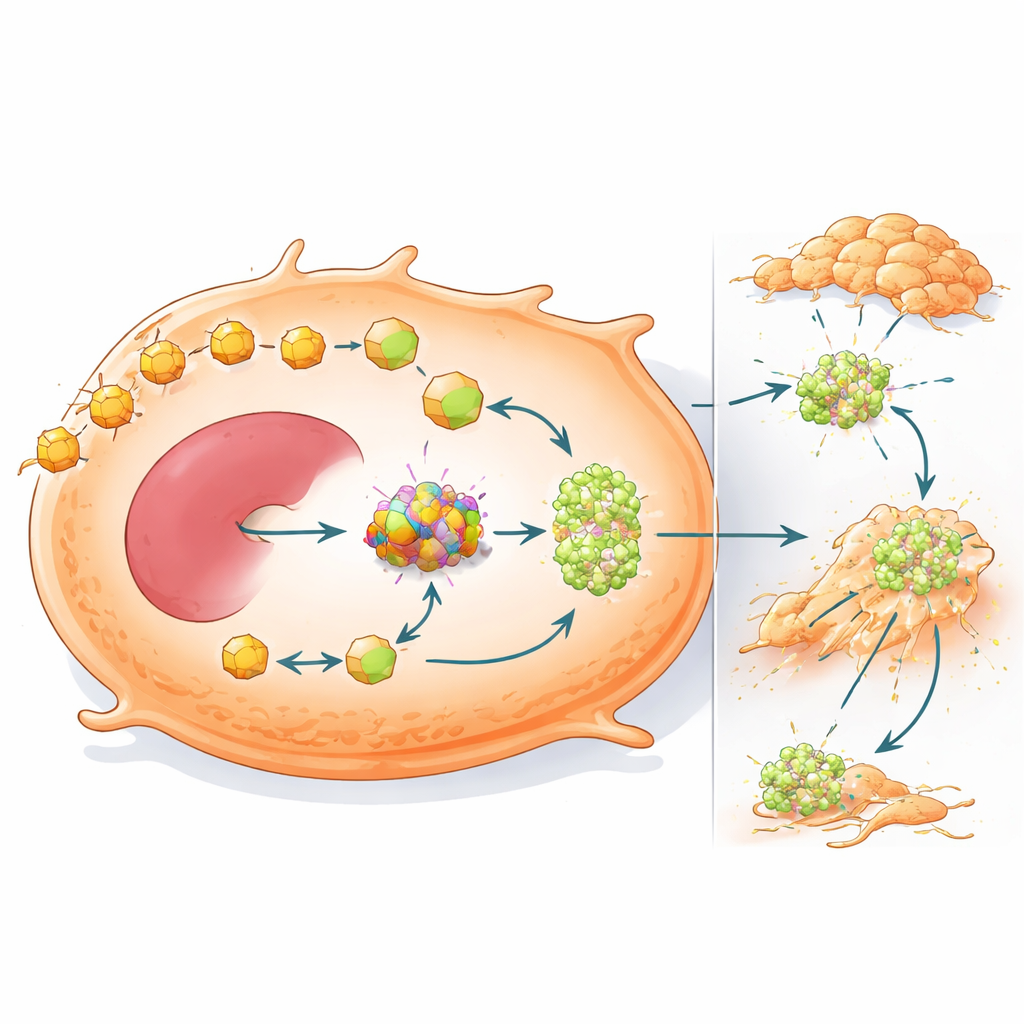
إعادة توصيل استخدام الوقود تدفع أيضاً انتشار السرطان
تُظهر الدراسة أيضاً أن OXCT1 يفعل أكثر من مساعدة الأورام على البقاء في بيئة منخفضة الكربوهيدرات—فهو يجعلها أيضاً أكثر ميلاً للانتشار. عندما ارتفع مستوى OXCT1 في خلايا سرطان الكبد، هاجرت وغزت الأنسجة المحيطة بشكل أكثر عدوانية في اختبارات المختبر وشكلت عقد نقيلية أكثر في أكباد الفئران. ربطت تحليلات الجينات بين ارتفاع OXCT1 وتنشيط بروتين إشارة يُدعى STAT3 وبرنامج الانتقال الظهاري‑اللحمي، حيث تُرخّص الخلايا روابطها وتكتسب حالة أكثر حركة وغزوًا. في الحيوانات، كانت أورام بيتا‑كاتينين المتحولة تظهر تنشيطًا قويًا لـ STAT3 ونقلاً واسع النطاق، لكن خفض OXCT1 عكس هذه التغيرات إلى حد كبير وقلّل من استيطان الكبد والرئتين.
ماذا يعني هذا للعلاج الكيتوني
بعبارات بسيطة، تُظهر هذه الدراسة أن بعض سرطانات الكبد الحاملة لطفرات شائعة في بيتا‑كاتينين يمكن أن تقلب مفعول العلاج الكيتوني رأساً على عقب. بدلاً من أن تُحرم من الوقود عندما تقل الكربوهيدرات، تنشط هذه الأورام OXCT1 لحرق أجسام الكيتون، وتحويلها إلى جزيئات تدعم النمو، وتنشيط مسارات تساعدها على الانتشار. ونتيجة لذلك، قد تكون الحميات الكيتونية وحدها محفوفة بالمخاطر أو غير فعالة للمرضى الحاملين لهذا النوع الفرعي من الأورام. تشير النتائج إلى أن فحص الأورام لحالة بيتا‑كاتينين وOXCT1، وتطوير أدوية تُثبط OXCT1، قد يجعل الاستراتيجيات القائمة على النظام الغذائي أكثر أماناً وفعالية عبر منع الأورام من تحويل علاج مقصود إلى ميزة لها.
الاستشهاد: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
الكلمات المفتاحية: حمية كيتونية, سرطان الكبد, طفرة بيتا‑كاتينين, أيض الورم, OXCT1