Clear Sky Science · ru
Мутация β-катенина перенастраивает метаболизм кетоновых тел, способствуя метастазированию гепатоцеллюлярной карциномы и устойчивости к кето-терапии через транскрипционную активацию OXCT1
Почему это важно для рака и питания
Кетогенные диеты, богатые жирами и крайне бедные углеводами, исследуются как способ «голодания» опухолей через изменение топливных субстратов организма. В этом исследовании показано, что для важной подгруппы рака печени обычное генетическое изменение позволяет опухолевым клеткам использовать кетоновые тела как источник энергии и роста. Вместо ослабления под кето-диетой такие опухоли могут стать труднее поддающимися лечению и более склонными к распространению, что подчеркивает необходимость подбирать диетические подходы к терапии в соответствии с биологией каждой опухоли.
Подробнее о раке печени и ключевой мутации
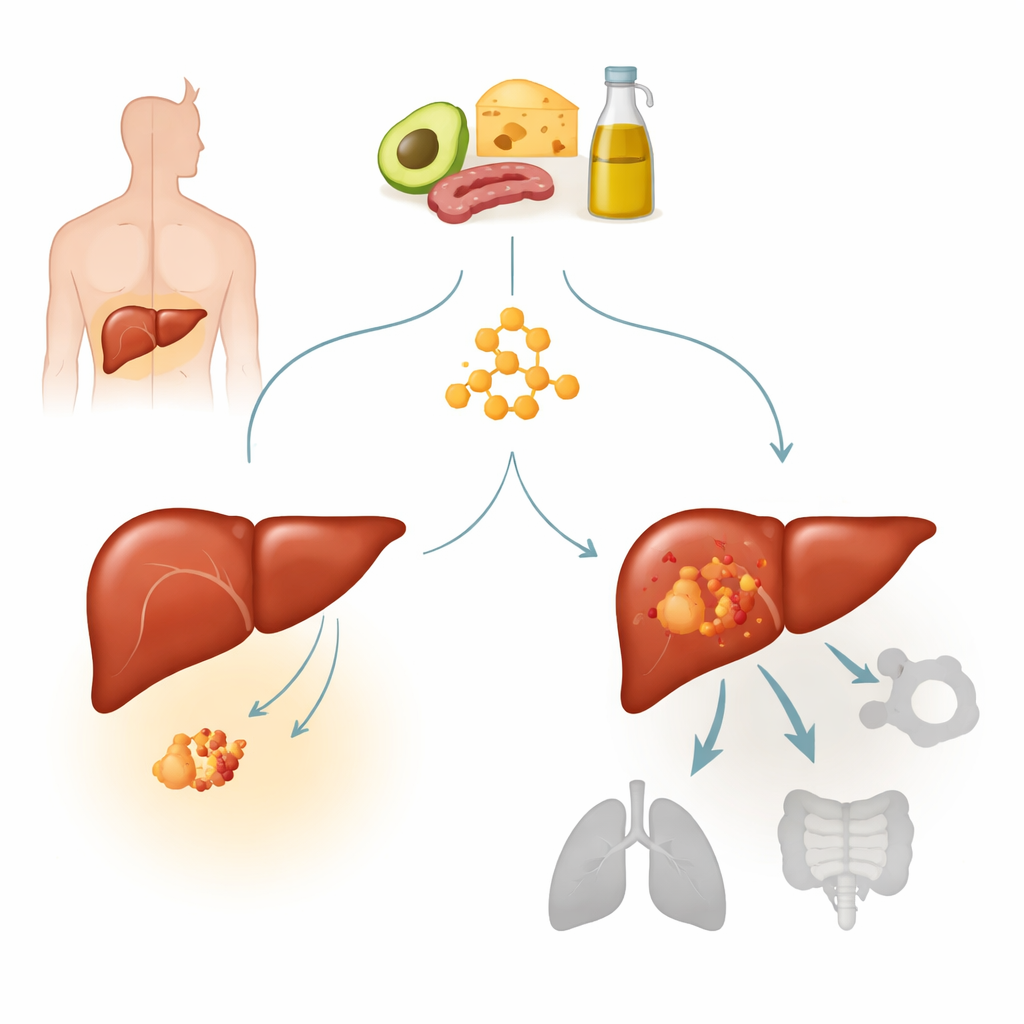
Гепатоцеллюлярная карцинома — наиболее распространенная форма рака печени и одна из ведущих причин смертности от рака в мире. Многие такие опухоли содержат активирующие мутации в гене бета-катенина, который обычно участвует в контроле роста клеток и ответов на сигналы. Одна горячая точка мутаций, называемая S33Y, удерживает путь бета‑катенина постоянно включенным и определяет отдельный подтип рака печени. Ранее авторы обнаружили, что опухоли с выраженным метаболизмом кетоновых тел кажутся менее чувствительными к кетогенной диете. В этой работе они сосредоточились на опухолях с мутантным бета‑катенином, чтобы выяснить, делает ли эта мутация рак печени врожденно устойчивым к кето-терапии и, если да, то каким образом.
Когда «низкоуглеводная» диета не замедляет опухоль
Используя человеческие клетки рака печени, выращенные у мышей, исследователи сравнили опухоли с мутацией S33Y в бета‑катенине и без неё при обычном питании и при кетогенной диете. В опухолях без мутации кетогенная диета явно замедляла рост: опухоли были меньшими и легче, хотя животные сохраняли массу тела и демонстрировали ожидаемый рост уровня кетонов в крови и снижение уровня глюкозы. В резком контрасте опухоли, управляемые мутацией бета‑катенина, агрессивно росли при обеих диетах и не получали пользы от кетогенной схемы. Похожая картина наблюдалась и в трансплантатах опухолей, полученных от пациентов: кормление по кетогенной диете уменьшало размеры опухолей с нормальным бета‑катенином, но не сдерживало рост опухолей с мутантным бета‑катенином, что указывает на истинную устойчивость, а не модельно-специфический эффект.
Как раковые клетки превращают кетоны в топливо для роста
Чтобы понять эту устойчивость, авторы изучили, как мутантный бета‑катенин перестраивает утилизацию кетонов в клетках опухоли. Они сосредоточились на OXCT1 — ключевом ферменте, который позволяет клеткам расщеплять кетоновые тела — процессе, обычно минимальном в здоровой печеночной ткани. Клетки с мутантным бета‑катенином значительно повышали уровни OXCT1 и других ферментов, связанных с кетонами, а метаболическое трассирование мечеными кетоновыми телами показало, что эти клетки эффективно превращают кетоны в глутамат — важный строительный блок и источник энергии. Подробные молекулярные эксперименты выявили, что мутантный бета‑катенин в сотрудничестве с белком‑партнёром LEF1 связывается с регуляторной областью гена OXCT1 и включает его экспрессию. Блокада OXCT1 в мутантных опухолях снижала продукцию глутамата и устраняла их устойчивость к кетогенной диете, что указывает на этот фермент как на критический метаболический «переключатель».
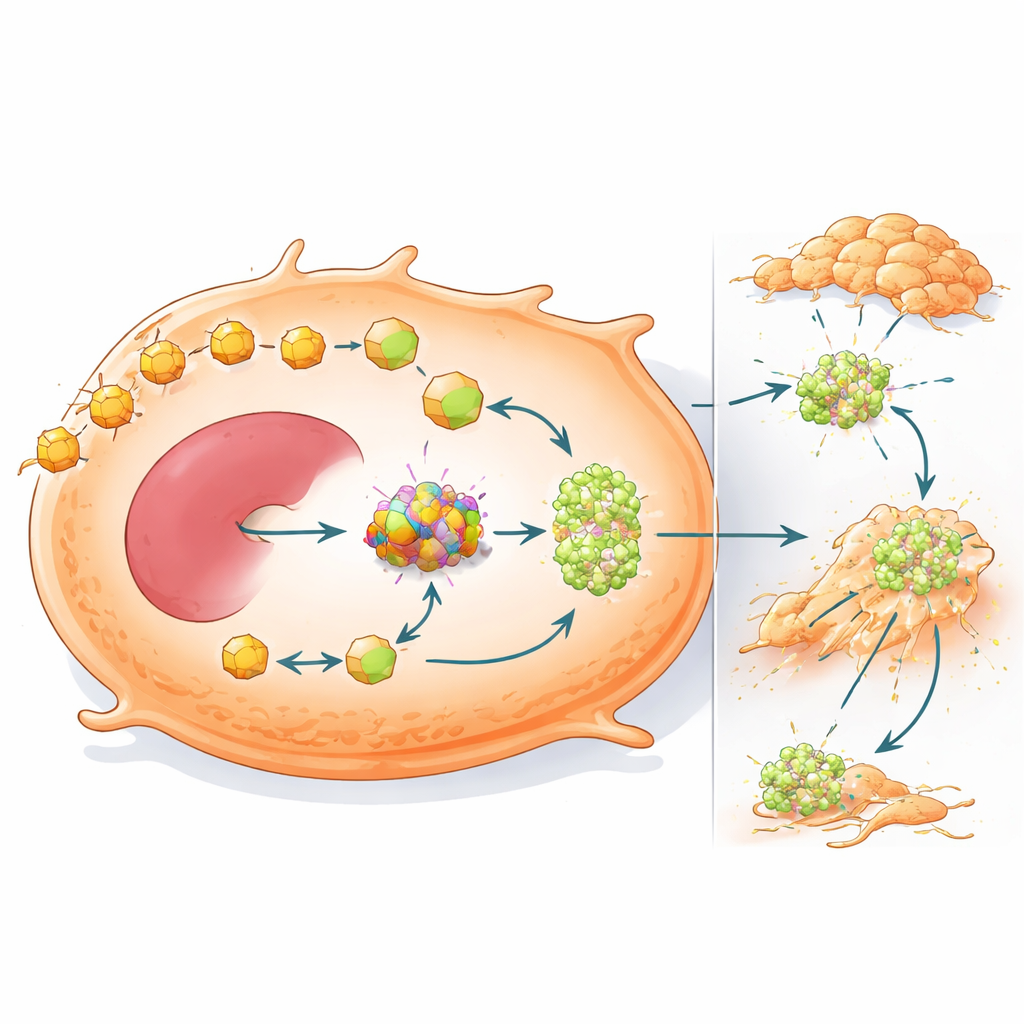
Перестроенное использование топлива также способствует метастазированию
Исследование дополнительно показывает, что OXCT1 делает больше, чем просто помогает опухолям пережить дефицит углеводов — он также повышает их склонность к распространению. При повышении уровня OXCT1 в клетках рака печени они в лабораторных тестах активнее мигрировали и проникали в окружающие ткани и образовывали больше метастатических узелков в печени мышей. Генетические анализы связывали высокий OXCT1 с активацией сигнального белка STAT3 и с программой эпителиально-мезенхимального перехода, при которой клетки ослабляют межклеточные связи и приобретают более подвижное, инвазивное состояние. У животных опухоли с мутантным бета‑катенином имели сильную активацию STAT3 и обширные метастазы, но подавление OXCT1 в значительной степени обращало эти изменения и снижало колонизацию печени и лёгких.
Что это значит для кетогенной терапии
Проще говоря, эта работа показывает, что некоторые раки печени с частой мутацией бета‑катенина могут перевернуть эффект кетогенной терапии с ног на голову. Вместо того чтобы лишаться топлива при недостатке углеводов, эти опухоли активируют OXCT1, сжигают кетоновые тела, превращают их в молекулы, поддерживающие рост, и включают пути, способствующие распространению. В результате кетогенные диеты в одиночку могут быть рискованными или неэффективными для пациентов с этим подтипом опухоли. Полученные данные указывают на необходимость тестирования опухолей на статус бета‑катенина и OXCT1 и на перспективу разработки препаратов, блокирующих OXCT1, чтобы сделать подходы, основанные на диете, безопаснее и эффективнее, предотвращая превращение предполагаемой терапии в преимущество для рака.
Цитирование: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Ключевые слова: кетогенная диета, рак печени, мутация бета-катенина, метаболизм опухоли, OXCT1