Clear Sky Science · pt
Mutação em β-catenina reprograma o metabolismo de corpos cetônicos para impulsionar metástase do carcinoma hepatocelular e resistência à terapia cetogênica via ativação transcricional de OXCT1
Por que isso importa para câncer e dieta
Dietas cetogênicas, ricas em gordura e muito pobres em carboidratos, estão sendo investigadas como forma de “privar” tumores ao alterar o combustível que o corpo utiliza. Este estudo mostra que, para um subgrupo importante de câncer de fígado, uma alteração genética comum permite que as células tumorais sequestram corpos cetônicos como fonte de energia e de crescimento. Em vez de serem enfraquecidos por uma dieta cetogênica, esses cânceres podem, na verdade, tornar-se mais difíceis de tratar e mais propensos a se espalhar, ressaltando por que terapias contra o câncer baseadas em dieta devem ser ajustadas à biologia de cada tumor.
Um olhar mais atento sobre o câncer de fígado e uma mutação chave
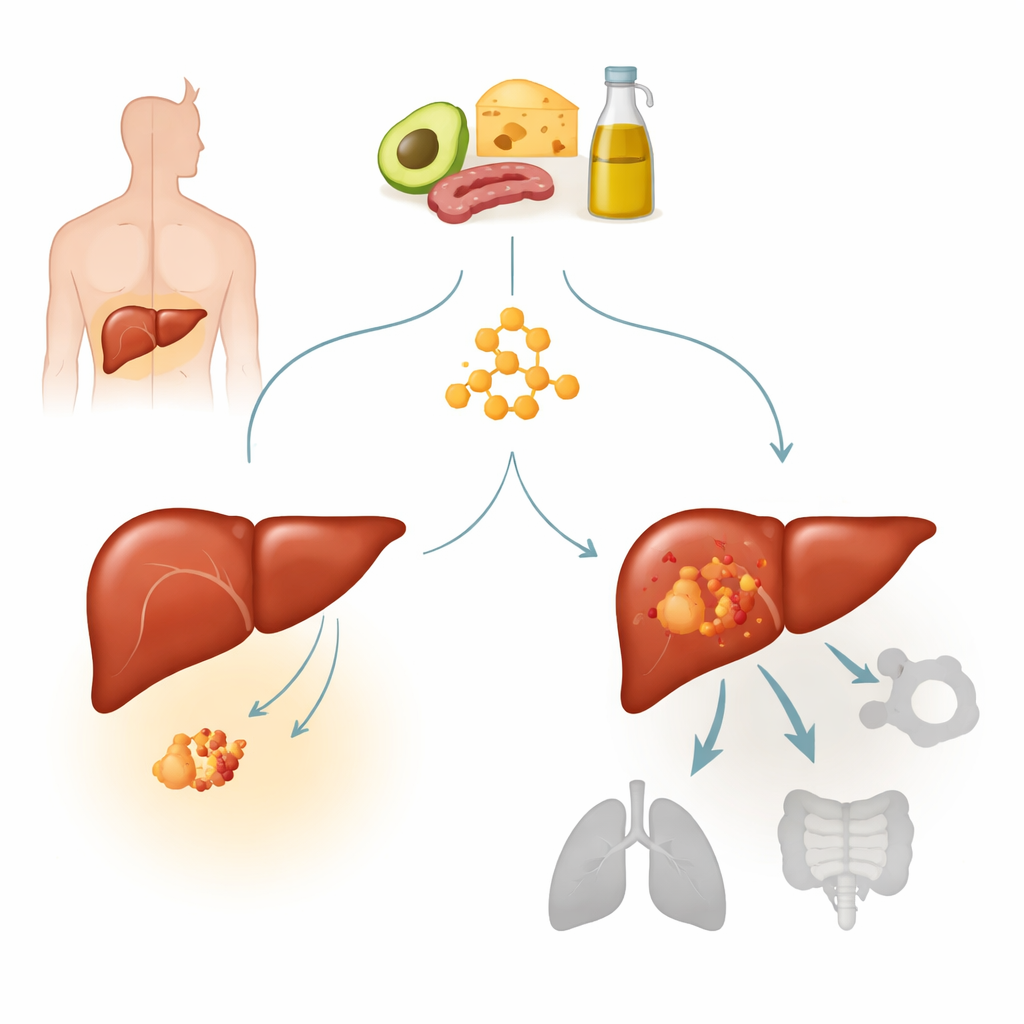
O carcinoma hepatocelular é a forma mais comum de câncer de fígado e uma das principais causas de morte por câncer no mundo. Muitos desses tumores carregam mutações ativadoras em um gene chamado beta-catenina, que normalmente ajuda a controlar como as células crescem e respondem a sinais. Uma mutação em ponto recorrente, chamada S33Y, mantém a via da beta-catenina permanentemente ligada e define um subtipo distinto de câncer de fígado. Os autores já haviam observado anteriormente que tumores com metabolismo ativo de corpos cetônicos pareciam menos responsivos a dietas cetogênicas. Aqui, eles focaram em tumores com mutação na beta-catenina para investigar se essa mutação torna os cânceres de fígado intrinsecamente resistentes à terapia cetogênica e, em caso afirmativo, como.
Quando uma dieta “baixo açúcar” não consegue deter os tumores
Usando células humanas de câncer de fígado cultivadas em camundongos, os pesquisadores compararam tumores com e sem a mutação S33Y na beta-catenina sob dieta normal ou dieta cetogênica. Nos tumores sem a mutação, a dieta cetogênica claramente retardou o crescimento: os tumores eram menores e mais leves, apesar de os animais manterem o peso corporal e apresentarem o aumento esperado de cetonas no sangue e queda da glicemia. Em nítido contraste, tumores impulsionados pela mutação da beta-catenina cresceram agressivamente em ambas as dietas e não mostraram benefício com o regime cetogênico. A equipe observou um padrão similar em enxertos de tumores hepáticos derivados de pacientes: a alimentação cetogênica reduziu tumores com beta-catenina normal, mas não conteve o crescimento de tumores com mutação na beta-catenina, indicando resistência verdadeira em vez de um efeito específico do modelo.
Como as células cancerosas transformam cetonas em combustível para crescer
Para entender essa resistência, os autores examinaram como a beta-catenina mutante remodela o manejo de cetonas dentro das células cancerosas. Eles se concentraram em OXCT1, a principal enzima que permite às células degradar corpos cetônicos — um processo normalmente mínimo no tecido hepático saudável. Células com beta-catenina mutante aumentaram fortemente os níveis de OXCT1 e outras enzimas relacionadas a cetonas, e rastreamento metabólico com corpos cetônicos marcados mostrou que essas células convertem eficientemente cetonas em glutamato, um bloco construtor e fonte de energia chave. Experimentos moleculares detalhados revelaram que a beta-catenina mutante se associa a uma proteína parceira, LEF1, para se ligar à região reguladora do gene OXCT1 e ativá‑lo. Bloquear OXCT1 em tumores mutantes reduziu a produção de glutamato e eliminou sua resistência à dieta cetogênica, indicando que essa enzima é um “interruptor” metabólico crítico.
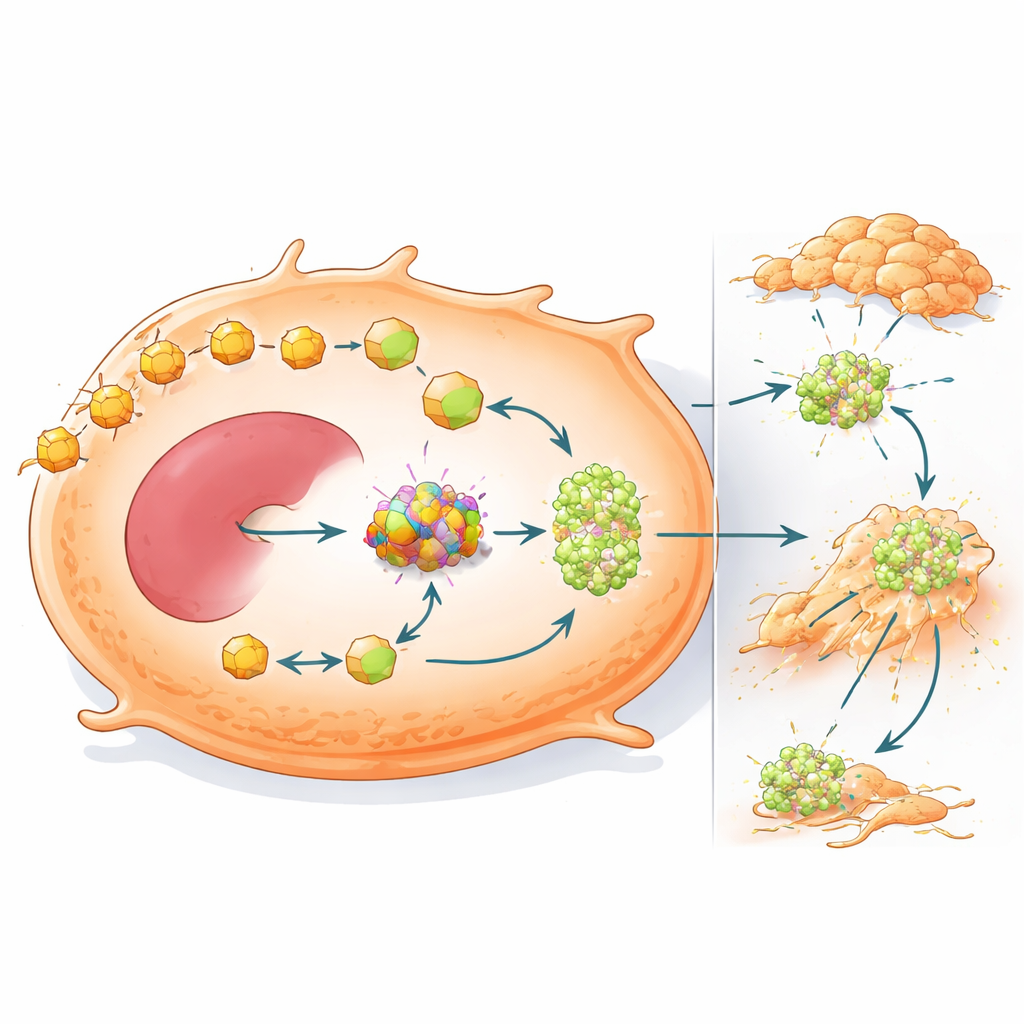
O uso reprogramado de combustível também impulsiona a disseminação do câncer
O estudo ainda mostra que OXCT1 faz mais do que ajudar tumores a sobreviver em um ambiente pobre em carboidratos — ele também os torna mais propensos a metastizar. Quando OXCT1 foi aumentado em células de câncer de fígado, elas migraram e invadiram tecidos circundantes mais agressivamente em testes de laboratório e formaram mais nódulos metastáticos nos fígados de camundongos. Análises genéticas vincularam altos níveis de OXCT1 à ativação de uma proteína de sinalização chamada STAT3 e a um programa de transição epitélio‑mesênquima, no qual as células afrouxam suas conexões e adquirem um estado mais móvel e invasivo. Em animais, tumores com mutação na beta-catenina apresentaram forte ativação de STAT3 e metástase extensa, mas a redução de OXCT1 inverteu amplamente essas alterações e diminuiu a colonização tanto do fígado quanto dos pulmões.
O que isso significa para a terapia cetogênica
Em termos práticos, este trabalho mostra que alguns cânceres de fígado que carregam uma mutação comum na beta-catenina podem inverter o efeito esperado da terapia cetogênica. Em vez de serem privados de combustível quando os carboidratos são escassos, esses tumores ativam OXCT1 para queimar corpos cetônicos, convertê‑los em moléculas que suportam o crescimento e ativar vias que os ajudam a se espalhar. Como resultado, dietas cetogênicas isoladas podem ser arriscadas ou ineficazes para pacientes com esse subtipo tumoral. Os achados sugerem que testar tumores quanto ao status de beta-catenina e OXCT1, e desenvolver fármacos que bloqueiem OXCT1, poderia tornar estratégias baseadas na dieta mais seguras e eficazes ao impedir que os cânceres transformem uma terapia pretendida em vantagem.
Citação: Li, H., Qian, L., Ji, Y. et al. β-catenin mutation reprograms ketone body metabolism to drive hepatocellular carcinoma metastasis and resistance to ketogenic therapy via transcriptional activation of OXCT1. Cell Death Dis 17, 301 (2026). https://doi.org/10.1038/s41419-026-08457-y
Palavras-chave: dieta cetogênica, câncer de fígado, mutação em beta-catenina, metabolismo tumoral, OXCT1