Clear Sky Science · zh
通过基于AmyloLipid纳米囊泡(ALN)鼻内给药系统输送亚麻醉剂量氯胺酮对PTSD动物模型生物行为反应的影响
帮助大脑从创伤中自愈
创伤后应激障碍(PTSD)可能持续多年,使人陷入恐惧、焦虑和侵入性记忆的循环。许多现有治疗只部分有效或见效缓慢。本研究探讨了一种通过鼻腔将一种已知药物氯胺酮直接输送到大脑的新方法,使用微小的脂质与淀粉复合囊泡。期望是增强疗效、减少副作用,并更好地支持大脑在创伤后自我适应和恢复的能力。
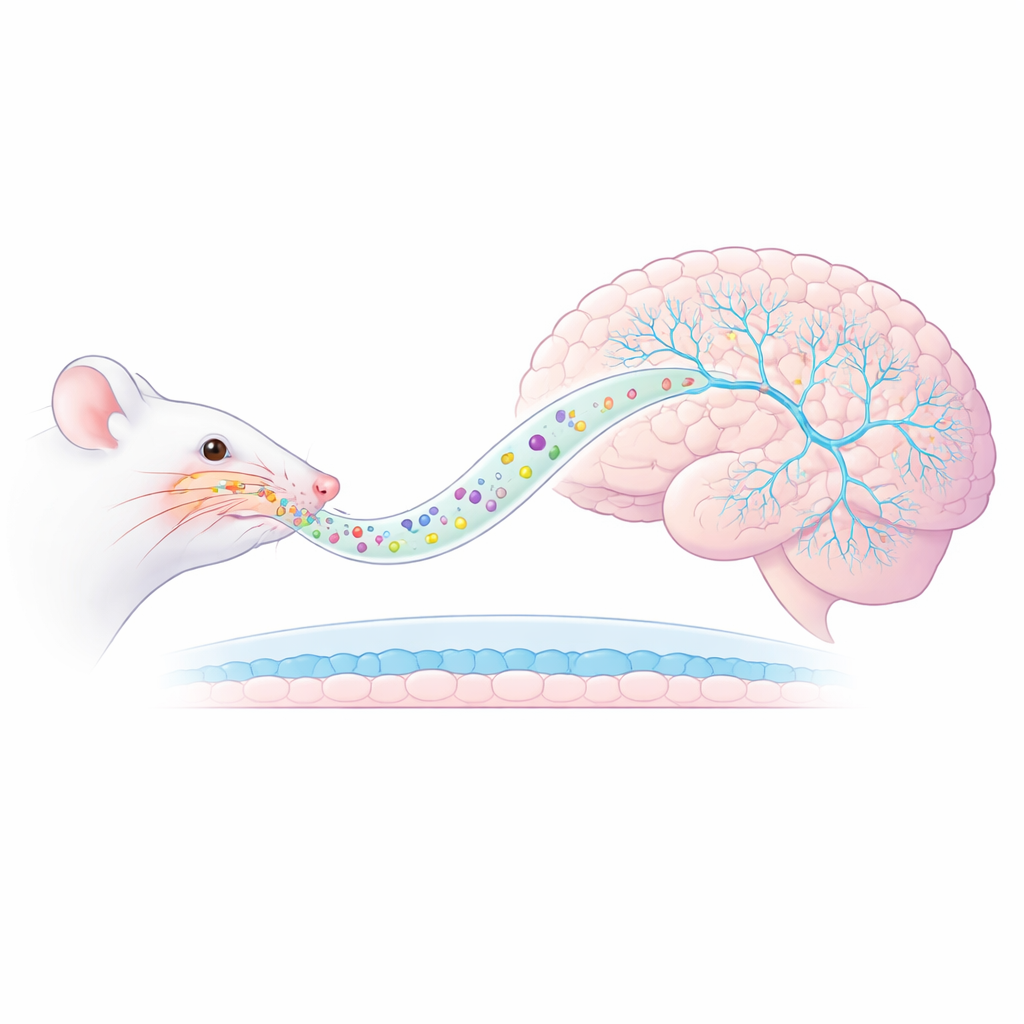
一种新的鼻到脑通路
研究者使用一种大鼠PTSD模型,动物暴露于捕食者气味,诱发持久的焦虑和对威胁暗示的过度反应。研究不是通过注射给药,而是将氯胺酮封装在AmyloLipid纳米囊泡中——这些纳米级小滴具有脂质核心并包裹以改性淀粉外壳。喷入鼻腔后,这些颗粒被设计为沿神经通路直接进入大脑,绕过通常限制药物进入的大脑血–脑屏障。早期测量显示,这种方法显著提高了脑组织中的氯胺酮水平,同时保持血液中浓度较低,提示更有针对性的递送并可能减少全身性副作用。
检测应激、恐惧与惊跳反应
在创伤暴露后,大鼠接受为期两周、每周三次的鼻内处理:不同剂量的装载氯胺酮的纳米囊泡、空纳米囊泡、普通氯胺酮溶液或生理盐水。研究组随后测量了动物在高架迷宫中的焦虑样表现、对响亮声音的惊跳强度,以及在再次暴露于无害的捕食者气味提示时的冻结程度。他们还将个体大鼠分为表现出极端、部分或很小干扰的组,模拟人类对创伤反应的差异。低剂量纳米囊泡中的氯胺酮——尤其是0.6毫克/千克——表现突出:它降低了类焦虑行为、减弱了过度的惊跳反应,并将表现出强烈PTSD样反应的动物比例相比空载颗粒组几乎减少了一半。相比之下,最高剂量则增加了冻结和焦虑,强调用药并非越多越好。
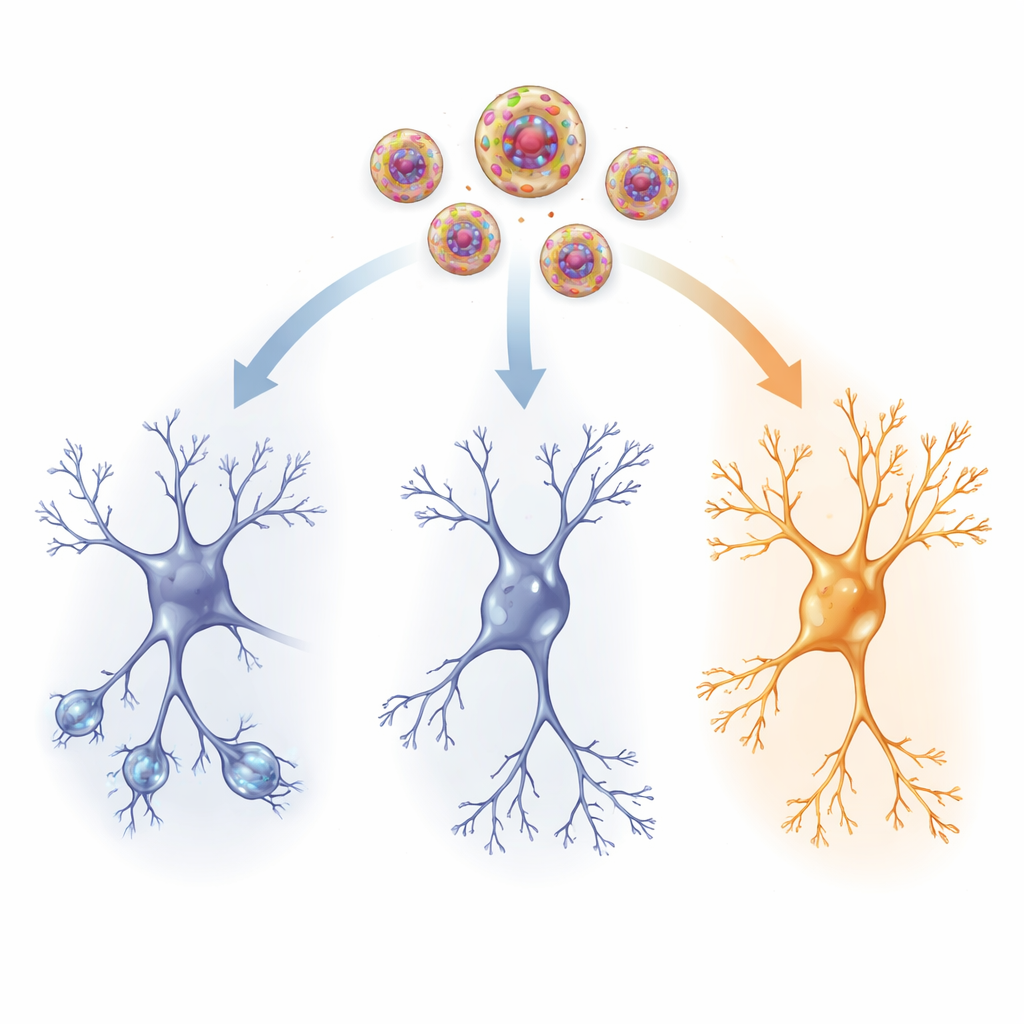
大脑回路内的变化
为了观察物理层面的改变,研究者检查了一个关键的记忆区域海马体以及一个应激控制中心——下丘脑室旁核。在未接受活性药物的受创大鼠中,海马神经元枝条更少且更短,构成突触的小棘突也减少——这是连接减弱的迹象。脑源性神经营养因子(BDNF)这种支持生长的蛋白和与应激恢复力相关的神经肽Y(NPY)的水平也下降。同时,HCN1通道(位于细胞膜上、影响神经元兴奋阈值的蛋白)增加。综合来看,这些变化表明创伤后大脑网络的可塑性和反应性下降。
在神经元中恢复平衡
通过纳米囊泡给药的低剂量氯胺酮逆转了许多上述损伤迹象。接受处理的大鼠神经元恢复了更长且更复杂的树突分支和更多棘突,尤其是在海马最上层——远端输入到达之处。BDNF和NPY在海马和应激控制区的水平回升至接近正常,表明对细胞存活、成长与韧性的支持恢复。同时,异常升高的HCN1通道减少,有助于恢复健康的电生理反应性。这些结构和化学变化与行为学改善密切对应,暗示有针对性的氯胺酮递送有助于受创大脑以更适应性的方式重新连线。
为何剂量与给药方式至关重要
将基于纳米囊泡的氯胺酮与普通氯胺酮溶液比较,凸显了给药方式与剂量的重要性。在低剂量时,鼻到脑系统在缓解类焦虑行为、惊跳和冻结方面优于标准氯胺酮。然而在最高剂量下,纳米囊泡中的氯胺酮似乎加剧了应激反应,可能是因为更多药物逃逸进入血液,被转化为有活性的代谢产物,并通过不那么靶向的途径到达大脑。这一模式表明存在一个狭窄的“最佳区间”,在该区间内低剂量的直接脑部递送最大化有益效果并最小化不良反应。
这对未来治疗的意义
简言之,这项工作表明,将少量氯胺酮温和地从鼻腔直接送入大脑,可使受创动物变得更平静、更有韧性,同时帮助其脑细胞重新建立连接并恢复健康的活动。尽管研究在大鼠中进行,但它指向一种治疗PTSD的策略:使用智能载体和精细剂量控制,而不是依赖更高药量。通过调节HCN1通道并提升BDNF和NPY等促进生长与恢复力的分子,AmyloLipid纳米囊泡中的鼻内氯胺酮或许有朝一日能提供一种更精准、持久且更安全的方式,帮助大脑从严重应激中恢复。
引用: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
关键词: PTSD, 氯胺酮, 鼻内给药, 纳米颗粒, 神经可塑性