Clear Sky Science · he
השפעת קטמין תת-אנסטטי הניתן באמצעות ננו-וזיקולות מבוססות AmyloLipid (ALN) במערכת אינטרנזאלית על תגובות ביוהביורליות במודל חייתי של PTSD
עזרה למוח להחלים מהטראומה
הפרעת דחק פוסט-טראומטית (PTSD) יכולה להתקיים שנים רבות, כשהאנשים סובלים ממחזורים של פחד, חרדה וזיכרונות פולשניים. טיפולים רבים כיום פועלים רק חלקית או באיטיות רבה. המחקר הזה בוחן שיטת מתן חדשה לתרופה ידועה, קטמין, ישירות למוח דרך האף באמצעות בועיות זעירות של שומן ועמילן. התקווה היא להגביר את התועלת, לצמצם תופעות לוואי, ולתמוך טוב יותר ביכולת הטבעית של המוח להסתגל ולהחלים לאחר טראומה.
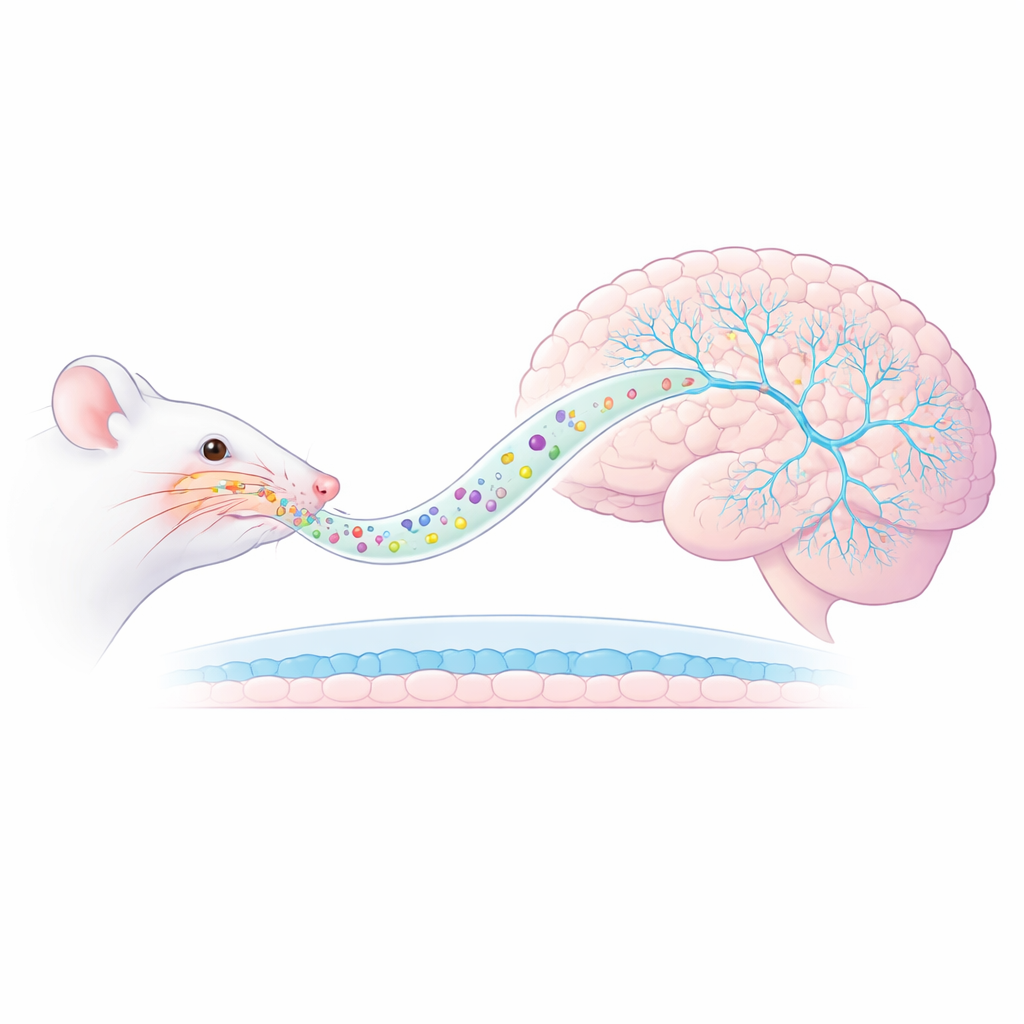
נתיב חדש מהאף אל המוח
החוקרים התמקדו במודל עכברים של PTSD שבו בעלי החיים נחשפים לריח טורף, מה שמפעיל חרדה ממושכת ותגובות מוגזמות לרמזים על האיום. במקום לתת את הקטמין בהזרקה, ארזו אותו בתוך ננו-וזיקולות AmyloLipid — טיפות בקנה מידה ננומטרי עם ליבת שומן עטופה במעטפת עמילן שעברה שינוי. כשהתמיסה נשאפת לאף, החלקיקים הללו מיועדים לנוע לאורך מסלולי עצב ישירות למוח, ולעקוף את מחסום הדם-מוח הרגיל שמגביל כניסת תרופות. מדידות מוקדמות הראו שגישה זו הגבירה במידה ניכרת את רמות הקטמין ברקמת המוח תוך שמירה על רמות דם נמוכות, דבר שמצביע על מתן ממוקד יותר ופחות תופעות לוואי מערכתיות אפשריות.
בדיקת סטרס, פחד והיפראקטיביות להפתעה
לאחר החשיפה לטראומה, העכברים קיבלו טיפולים אינטרנזאליים שלוש פעמים בשבוע במשך שבועיים: מינונים שונים של ננו-וזיקולות טעונות קטמין, ננו-וזיקולות ריקות, תמיסת קטמין רגילה או סליין. הצוות מדד אז עד כמה בעלי החיים נראו לחוצים במבוך מוגבה, כמה הם קפאו או הופתעו מקולות חזקים וכמה הם קפאו בעת חשיפה מחודשת לרמז חסר-פגיעה של ריח הטורף. הם גם מיינו את העכברים לפי פרופילים שגלו הפרעות קיצוניות, חלקיות או מינימליות, המדמים את השונות האנושית בתגובות לטראומה. קטמין במינון נמוך בננו-וזיקולות — במיוחד 0.6 מיליגרם לקילוגרם — בלט: הוא הוריד התנהגויות דמויות-חרדה, הקטין תגובות היפראקטיביות להפתעה וצמצם כמעט בחצי את החלק היחסי של בעלי החיים שהראו תגובות חזקות בדומה ל-PTSD לעומת אלה שקיבלו חלקיקים ריקים. לעומת זאת, המינון הגבוה ביותר הגדיל הקפאות וחרדה, מה שמדגיש שלעתים יותר תרופה אינה בהכרח טובה יותר.
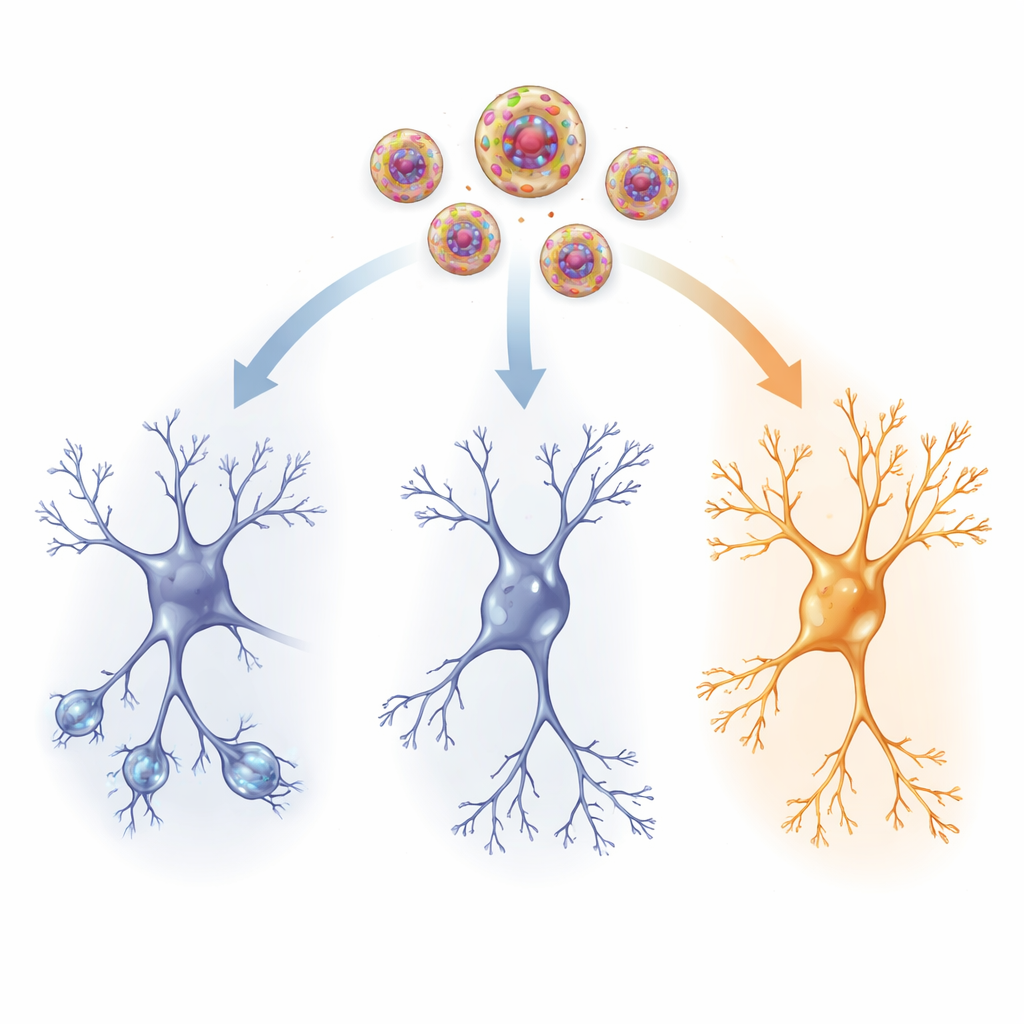
פנימה בחוטי התקשורת של המוח
כדי לראות מה משתנה פיזית, החוקרים בדקו איזור זיכרון מרכזי — ההיפוקמפוס — וגרעין פרה-וונטיקולרי בהיפותלמוס, שהוא מרכז לבקרת סטרס. בעכברים ששרדו טראומה ולא קיבלו תרופה פעילה, תאי העצב בהיפוקמפוס היו עם תת-התפוצות של ענפים קצרים ופחות חריצים זעירים שאליהם מתקיימות סינפסות — סימנים לחיבורים מוחלשים. גם רמות גורם הצמיחה BDNF ורמות הנוירופפטיד NPY, מולקולה המקושרת לעמידות מול סטרס, ירדו. במקביל נצפה גידול בתעלות HCN1, חלבונים בממברנת התא שמעצבים את רמות ההתרגשות הנוירונלית. ביחד התזוזות האלה מצביעות על רשת מוחית פחות גמישה ופחות תגובתית לאחר טראומה.
השבת איזון בתאי העצב
קטמין במינון נמוך שניתן באמצעות ננו-וזיקולות הפך רבים מסימני הנזק הללו. תאי העצב בעכברים המטופלים החזירו ענפים ארוכים ומורכבים יותר ושלמות של יותר חריצים, במיוחד בשכבה העליונה של ההיפוקמפוס שבה מגיעים קלטים מרוחקים. רמות BDNF ו-NPY שבו ועלהו לכיוון הנורמה הן בהיפוקמפוס והן באזור בקרה על הסטרס, דבר שמרמז על חידוש תמיכה בהישרדות תאים, בצמיחה ובעמידות. במקביל, הגאות הבלתי תקינה בתעלות HCN1 פחתה, וסייעה להשיב רמת תגובתיות חשמלית בריאה. השינויים המבניים והכימיים האלה התאימו בצמוד לשיפורי ההתנהגות, מה שמרמז כי מתן קטמין ממוקד מסייע למוח הפגוע להתחבר מחדש בצורה מותאמת יותר.
למה מינון ושיטת מתן חשובים
השוואת קטמין בננו-וזיקולות מול תמיסת קטמין רגילה הדגישה את חשיבות האופן והכמות שבה התרופה ניתנת. במינונים נמוכים, המערכת מהאף אל המוח עלתה על קטמין סטנדרטי בהקלה על התנהגויות דמוי-חרדה, תגובות הפתעה והקפאה. עם זאת, במינון הגבוה ביותר נראה כי קטמין בננו-וזיקולות החמיר תגובות סטרס, ככל הנראה מכיוון שכמות גדולה יותר של תרופה נשאבה אל מערכת הדם, עברה להפחתה לאפיקים פעילים והגיעה למוח בדרכים פחות ממוקדות. דפוס זה מצביע על כך שקיים "חלון" צר של מינון אידיאלי שבו מתן ישיר למוח במינון נמוך ממקסם את ההשפעות הטובות וממזער את הלא רצויות.
מה המשמעות לטיפול בעתיד
במילים פשוטות, עבודה זו מראה ששליחה עדינה של כמויות קטנות של קטמין מהאף ישירות אל המוח יכולה להפוך בעלי חיים מוטרדים לשקטים ועמידים יותר, תוך סיוע לתאי המוח לשקם חיבורים ולשוב לפעילות בריאה. למרות שהמחקר נעשה בעכברים, הוא מצביע על אסטרטגיה לטיפול ב-PTSD המשתמשת בנושאים חכמים ומינון מדוד במקום הגדלת כמות התרופה בלבד. על ידי כיוונון תעלות HCN1 והגברת מולקולות תמיכה וצמיחה כמו BDNF ו-NPY, קטמין אינטרנזלי בננו-וזיקולות AmyloLipid עשוי יום אחד להציע דרך מדויקת, ממושכת ובטוחה יותר לעזור למוח להחלים מלחץ חמור.
ציטוט: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
מילות מפתח: הפרעת דחק פוסט-טראומטית, קטמין, מתן אינטרנזלי, ננוחלקיקים, נוירופלסטיות