Clear Sky Science · pl
Wpływ subanestetycznego ketaminy podawanego za pomocą donosowego systemu opartego na nanowezikach AmyloLipid (ALN) na odpowiedzi biobehawioralne w modelu zwierzęcym PTSD
Pomoc mózgowi w regeneracji po traumie
Zaburzenie stresowe pourazowe (PTSD) może utrzymywać się przez lata, pozostawiając osoby uwięzione w cyklach lęku, niepokoju i natrętnych wspomnień. Wiele obecnych terapii działa jedynie częściowo lub bardzo wolno. W tym badaniu zbadano nowy sposób dostarczania dobrze znanego leku — ketaminy — bezpośrednio do mózgu przez nos, wykorzystując maleńkie pęcherzyki tłuszczu i skrobi. Celem jest zwiększenie korzyści, ograniczenie skutków ubocznych i lepsze wsparcie zdolności mózgu do adaptacji i regeneracji po urazie.
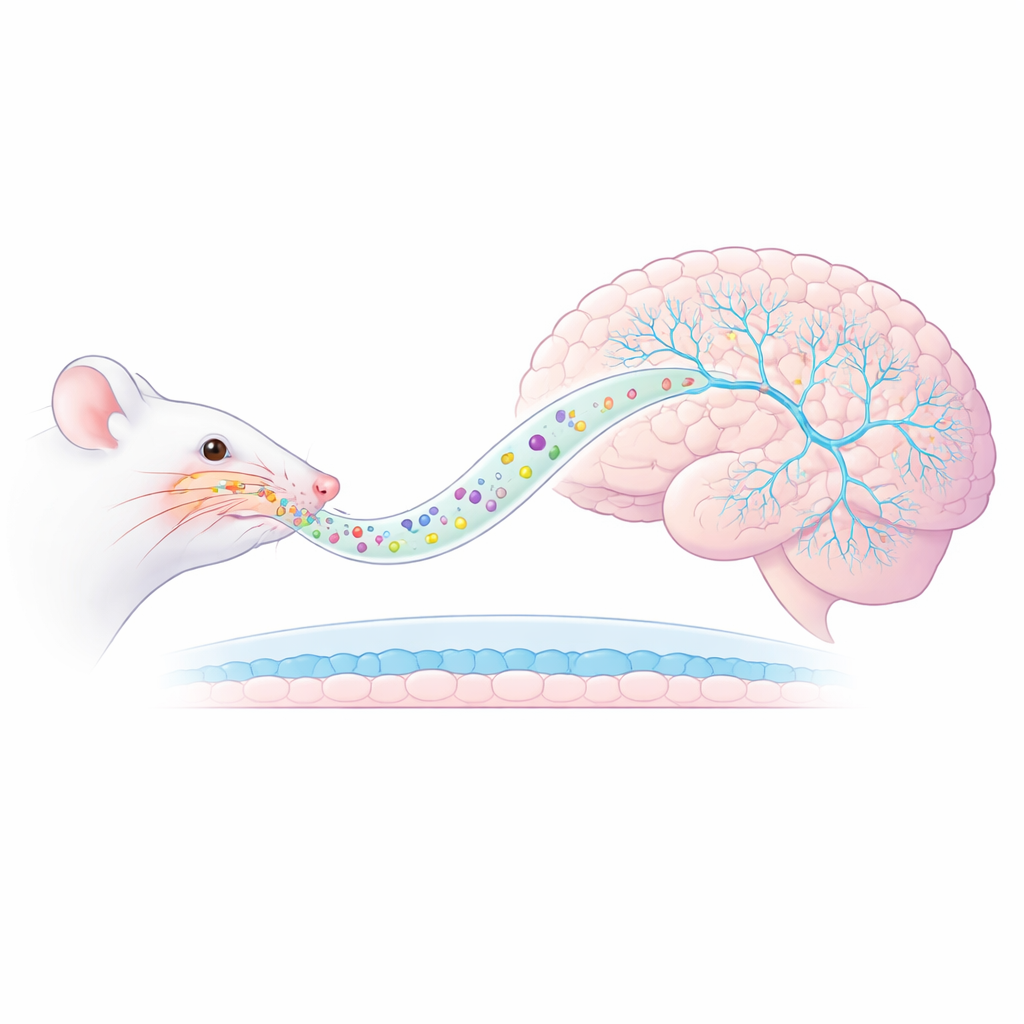
Nowa droga od nosa do mózgu
Naukowcy skupili się na modelu PTSD u szczurów, w którym zwierzęta są narażone na zapach drapieżnika, co wywołuje długotrwały lęk i nasilone reakcje na przypomnienia zagrożenia. Zamiast podawać ketaminę w zastrzyku, zamknęli ją wewnątrz nanowezików AmyloLipid — kropelek o rozmiarach nanometrów z tłustym jądrem otoczonym zmodyfikowaną powłoką skrobiową. Po zastosowaniu donosowym cząstki te mają przemieszczać się wzdłuż dróg nerwowych bezpośrednio do mózgu, omijając zwykłą barierę krew–mózg, która ogranicza przenikanie leków. Wcześniejsze pomiary wykazały, że podejście to znacząco zwiększa poziomy ketaminy w tkance mózgowej, przy jednocześnie niskich stężeniach we krwi, co sugeruje bardziej ukierunkowane dostarczanie i potencjalnie mniejsze ogólnoustrojowe skutki uboczne.
Badanie stresu, lęku i odruchu wystraszenia
Po ekspozycji traumatycznej szczury otrzymywały donosowe leczenie trzy razy w tygodniu przez dwa tygodnie: różne dawki nanowezików z ketaminą, puste nanoweziki, roztwór ketaminy lub sól fizjologiczną. Zespół mierzył następnie, jak bardzo zwierzęta wydawały się lękliwe w podwyższonym labiryncie, jak silnie reagowały na głośne dźwięki oraz jak długo zastygały w bezruchu po ponownym wystawieniu na nieszkodliwe przypomnienie zapachu drapieżnika. Przyporządkowano też poszczególne szczury do grup wykazujących skrajne, częściowe lub minimalne zaburzenia, naśladując zróżnicowanie reakcji ludzi na traumę. Ketamina w nanowezikach w niskiej dawce — zwłaszcza 0,6 mg/kg — wyróżniała się: zmniejszała zachowania podobne do lęku, łagodziła nasilony odruch wystraszenia i zmniejszała odsetek zwierząt z silnymi reakcjami przypominającymi PTSD niemal o połowę w porównaniu z grupą otrzymującą puste cząstki. Natomiast najwyższa dawka zwiększała zastyganie i lęk, podkreślając, że większa ilość leku nie zawsze daje lepsze efekty.
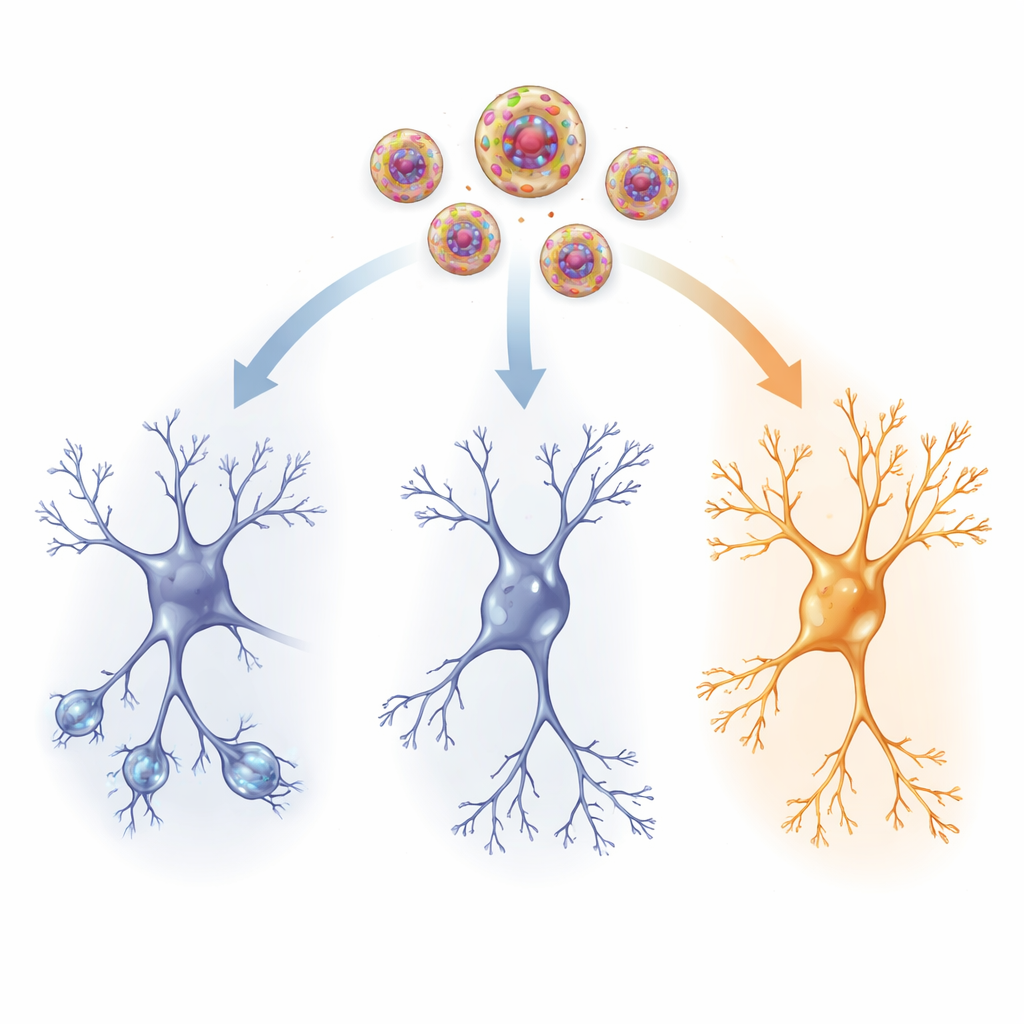
Wnętrze okablowania mózgu
Aby zobaczyć, co ulegało zmianie fizycznie, badacze zbadali kluczowy region pamięci — hipokamp — oraz ośrodek kontroli stresu, jądro przykomorowe podwzgórza. U przerażonych szczurów, które nie otrzymały aktywnego leku, komórki nerwowe w hipokampie miały mniej i krótsze rozgałęzienia oraz mniej drobnych kolców synaptycznych — oznaki osłabionych połączeń. Poziomy czynnika neurotroficznego pochodzenia mózgowego (BDNF), białka wspierającego wzrost, oraz neuropeptydu Y (NPY), związku z odpornością na stres, były również zmniejszone. Jednocześnie zaobserwowano wzrost kanałów HCN1, białek w błonie komórkowej kształtujących łatwość wyładowań neuronów. Te zmiany razem wskazują na sieć mózgową mniej plastyczną i mniej responsywną po traumie.
Przywracanie równowagi w komórkach nerwowych
Niskodawkowa ketamina podana za pomocą nanowezików odwróciła wiele z tych oznak uszkodzenia. Neurony u leczonych zwierząt odzyskały dłuższe i bardziej złożone rozgałęzienia oraz więcej kolców, szczególnie w najbardziej powierzchownej warstwie hipokampa, gdzie docierają odległe wejścia. Poziomy BDNF i NPY wróciły w kierunku normy zarówno w hipokampie, jak i w ośrodku kontroli stresu, sugerując odnowione wsparcie dla przeżycia komórek, wzrostu i odporności. Jednocześnie ustąpił nieprawidłowy wzrost kanałów HCN1, co pomogło przywrócić zdrowy poziom reaktywności elektrycznej. Te strukturalne i chemiczne zmiany ściśle korelowały z poprawą zachowania, co sugeruje, że celowane dostarczanie ketaminy pomaga traumatyzowanemu mózgowi przebudować się w bardziej adaptacyjny sposób.
Dlaczego dawka i droga podania mają znaczenie
Porównanie ketaminy w nanowezikach z zwykłym roztworem ketaminy uwypukliło istotę sposobu i ilości podawanego leku. Przy niskich dawkach system od nosa do mózgu przewyższał standardową ketaminę w łagodzeniu zachowań lękowych, odruchu wystraszenia i zastygania. Jednak przy najwyższej dawce ketamina w nanowezikach wyglądała na pogarszającą reakcje na stres, prawdopodobnie dlatego, że więcej leku przedostało się do krwiobiegu, zostało przekształcone w aktywne produkty rozpadu i dotarło do mózgu mniej ukierunkowanymi drogami. Ten wzorzec sugeruje istnienie wąskiego „punktu optymalnego”, w którym bezpośrednie dostarczanie do mózgu przy niskiej dawce maksymalizuje korzyści przy jednoczesnym minimalizowaniu niepożądanych efektów.
Co to może oznaczać dla przyszłej opieki
Mówiąc prościej, praca ta pokazuje, że delikatne podawanie małych ilości ketaminy bezpośrednio z nosa do mózgu może uczynić traumatyzowane zwierzęta spokojniejszymi i bardziej odpornymi, a jednocześnie pomóc ich komórkom mózgowym odbudować połączenia i odzyskać zdrową aktywność. Chociaż badanie przeprowadzono na szczurach, wskazuje ono na strategię leczenia PTSD wykorzystującą inteligentne nośniki i staranne dawkowanie, zamiast po prostu większych dawek leku. Poprzez modulację kanałów HCN1 i zwiększanie poziomów cząsteczek wspierających wzrost i odporność, takich jak BDNF i NPY, donosowa ketamina w nanowezikach AmyloLipid może pewnego dnia zaoferować bardziej precyzyjny, dłużej działający i bezpieczniejszy sposób wspierania regeneracji mózgu po ciężkim stresie.
Cytowanie: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Słowa kluczowe: PTSD, ketamina, podawanie donosowe, nanocząstki, neuroplastyczność