Clear Sky Science · ru
Влияние субанестетической кетамина, доставляемого через носовую систему на основе нановезикул AmyloLipid (ALN), на биоповеденческие реакции в модели ПТСР у животных
Помощь мозгу в восстановлении после травмы
Посттравматическое стрессовое расстройство (ПТСР) может сохраняться годами, заставляя людей жить в циклах страха, тревоги и навязчивых воспоминаний. Многие существующие методы лечения работают лишь частично или медленно. В этом исследовании изучается новый способ доставить хорошо известный препарат — кетамин — прямо в мозг через нос, используя крошечные пузырьки жира и крахмала. Цель — усилить полезный эффект, сократить побочные явления и лучше поддержать способность мозга к адаптации и восстановлению после травмы.
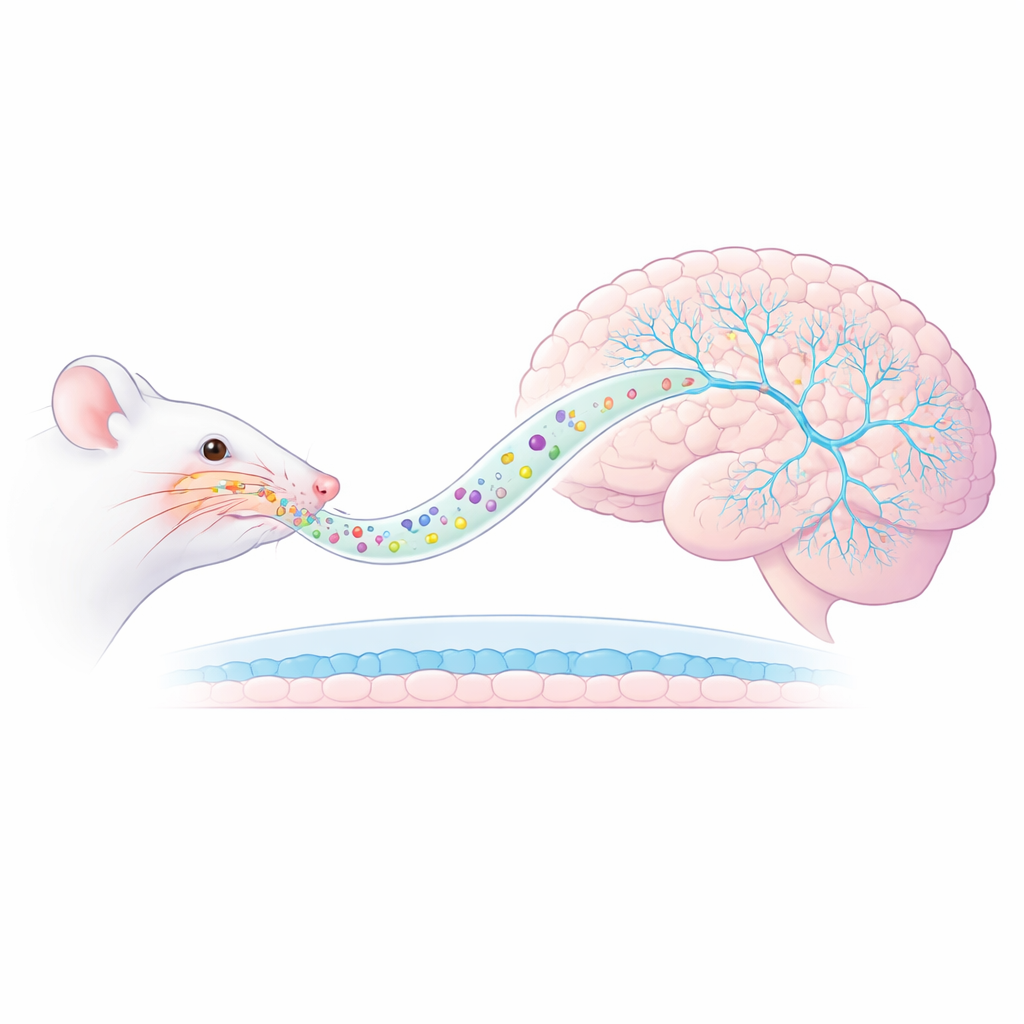
Новый путь от носа к мозгу
Исследователи сосредоточились на модели ПТСР у крыс, в которой животные подвергаются запаху хищника — это вызывает длительную тревогу и повышенную реактивность на напоминания об угрозе. Вместо внутривенных инъекций кетамин поместили в нановезикулы AmyloLipid — наномасштабные капли с жировым ядром в оболочке из модифицированного крахмала. При распылении в нос эти частицы должны перемещаться по нервным путям прямо в мозг, обходя обычный гематоэнцефалический барьер, ограничивающий проникновение препаратов. Предыдущие измерения показали, что такой подход значительно повышает концентрацию кетамина в мозговой ткани при низком уровне в крови, что указывает на более направленную доставку и потенциально меньше системных побочных эффектов.
Тестирование стресса, страха и вздрагивания
После травмирующего воздействия крысам трижды в неделю в течение двух недель вводили интраназальные препараты: нановезикулы с кетамином в разных дозах, пустые нановезикулы, раствор кетамина без носителя или физиологический раствор. Команда затем оценивала тревожность животных в поднятом лабиринте, их рефлекторное вздрагивание от громких звуков и степень замирания при повторном воздействии безвредного напоминания о запахе хищника. Также животных разделяли на группы с выраженным, частичным или минимальным нарушением, имитируя индивидуальные различия в реакциях на травму у людей. Низкая доза кетамина в нановезикулах — особенно 0,6 миллиграмма на килограмм — выделялась: она снижала поведение, похожее на тревогу, уменьшала чрезмерное вздрагивание и сокращала долю животных с выраженными ПТСР-подобными реакциями почти вдвое по сравнению с теми, кто получал пустые частицы. Напротив, самая высокая доза увеличивала замирание и тревожность, что подчеркивает: больше препарата не всегда лучше.
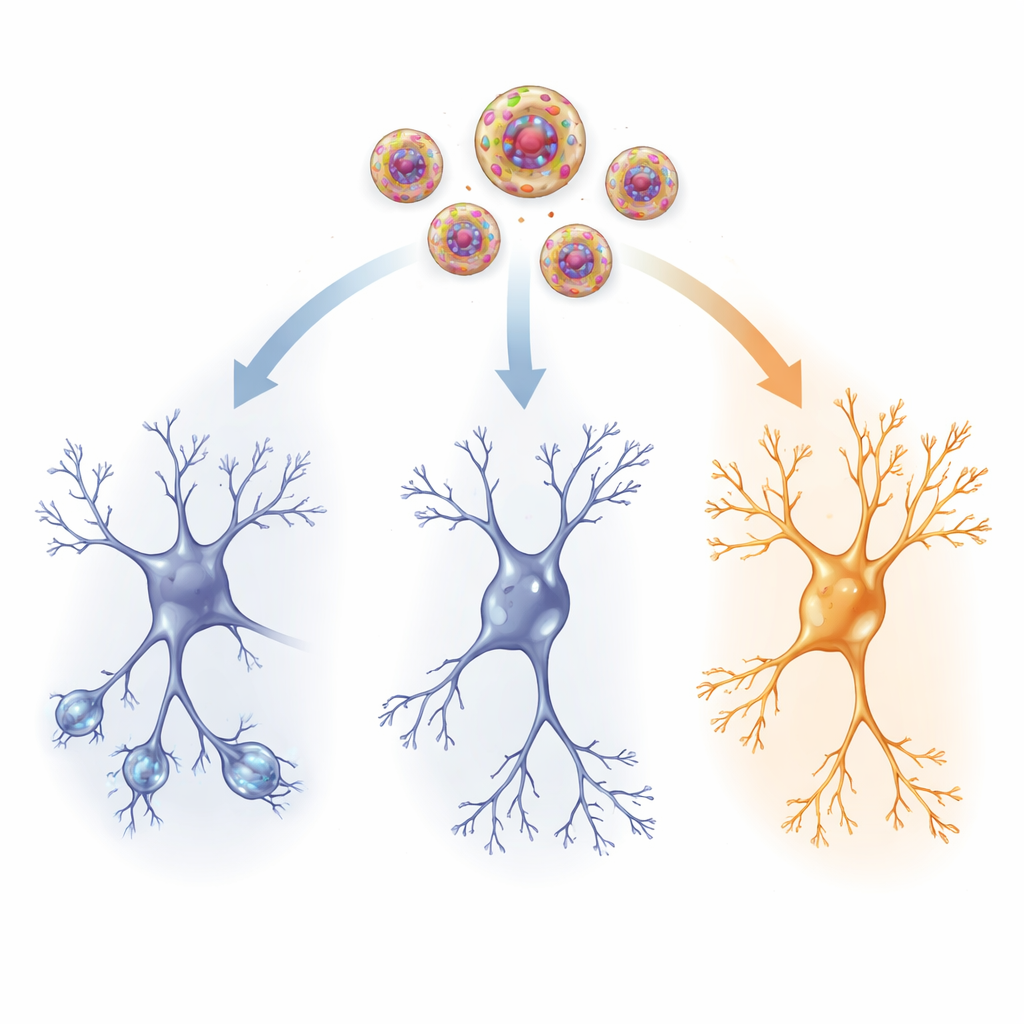
Внутри проводящих путей мозга
Чтобы увидеть физические изменения, исследователи изучали ключевую область памяти — гиппокамп — и центр контроля стресса, паратравматическое ядро (paraventricular nucleus) гипоталамуса. У травмированных крыс без активного препарата нервные клетки гиппокампа имели меньше и короче ветвей и меньше пучков-«шпилек» (spines), где формируются синапсы — признаки ослабленных связей. Уровни фактора роста, связанного с мозгом (BDNF), и нейропептида Y (NPY), молекулы, связанной с устойчивостью к стрессу, также были снижены. Одновременно наблюдалось увеличение каналов HCN1 — белков в мембране клетки, определяющих легкость возбуждения нейронов. В совокупности эти сдвиги указывают на сеть мозга, которая после травмы стала менее гибкой и менее отзывчивой.
Восстановление баланса в нервных клетках
Низкая доза кетамина, введенная через нановезикулы, обращала многие из этих признаков повреждения. Нейроны у обработанных животных восстановили более длинные и более сложные ветви и больше шипиков, особенно в верхнем слое гиппокампа, куда поступают отдаленные входы. Уровни BDNF и NPY выросли ближе к норме как в гиппокампе, так и в регионе контроля стресса, что свидетельствует о восстановлении поддержки выживания клеток, их роста и устойчивости. Одновременно спал ненормальный рост каналов HCN1, что помогло вернуть здоровый уровень электрической возбудимости. Эти структурные и химические изменения тесно коррелировали с поведенческими улучшениями, что позволяет предположить: направленная доставка кетамина помогает травмированному мозгу перенастроиться более адаптивным образом.
Почему важны доза и способ доставки
Сравнение кетамина в нановезикулах с обычным раствором кетамина показало, насколько важно, как и в каком количестве вводят препарат. При низких дозах система «нос — мозг» превосходила стандартный кетамин в снижении тревожного поведения, вздрагивания и замирания. Однако при самой высокой дозе кетамин в нановезикулах, по-видимому, усугублял стрессовые реакции, вероятно потому, что большая часть препарата попала в кровоток, превратилась в активные метаболиты и достигла мозга менее направленными путями. Эта картина указывает на узкую «зону оптимума», где прямая доставка в мозг при низкой дозе максимально эффективна и минимизирует побочные эффекты.
Что это может значить для будущего лечения
Проще говоря, эта работа показывает: аккуратная доставка небольших доз кетамина прямо из носа в мозг может сделать травмированных животных спокойнее и устойчивее, а также помочь их клеткам мозга отрастить связи и восстановить здоровую активность. Хотя исследование проведено на крысах, оно указывает на стратегию лечения ПТСР с использованием умных носителей и тщательной дозировки вместо увеличения количества препарата. Путем модуляции каналов HCN1 и повышения уровней молекул роста и устойчивости, таких как BDNF и NPY, интраназальный кетамин в нановезикулах AmyloLipid может в будущем предложить более точный, длительный и безопасный способ помочь мозгу восстановиться после сильного стресса.
Цитирование: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Ключевые слова: ПТСР, кетамин, назальная доставка, наночастицы, нейропластичность