Clear Sky Science · nl
Impact van subanesthetische ketamine toegediend via AmyloLipid-nanovesikels (ALN)-gebaseerd intranasaal systeem op biogedragsreacties in een diermodel van PTSS
Helpen de hersenen te herstellen van trauma
Posttraumatische stressstoornis (PTSS) kan jaren aanhouden en mensen gevangen houden in cycli van angst, spanning en opdringerige herinneringen. Veel huidige behandelingen werken slechts gedeeltelijk of heel traag. Deze studie onderzoekt een nieuwe manier om een bekend middel, ketamine, rechtstreeks naar de hersenen te brengen via de neus met behulp van piepkleine vet- en zetmeelblaasjes. De hoop is dat dit de werking versterkt, bijwerkingen vermindert en de natuurlijke capaciteit van de hersenen om zich aan te passen en te herstellen na trauma beter ondersteunt.
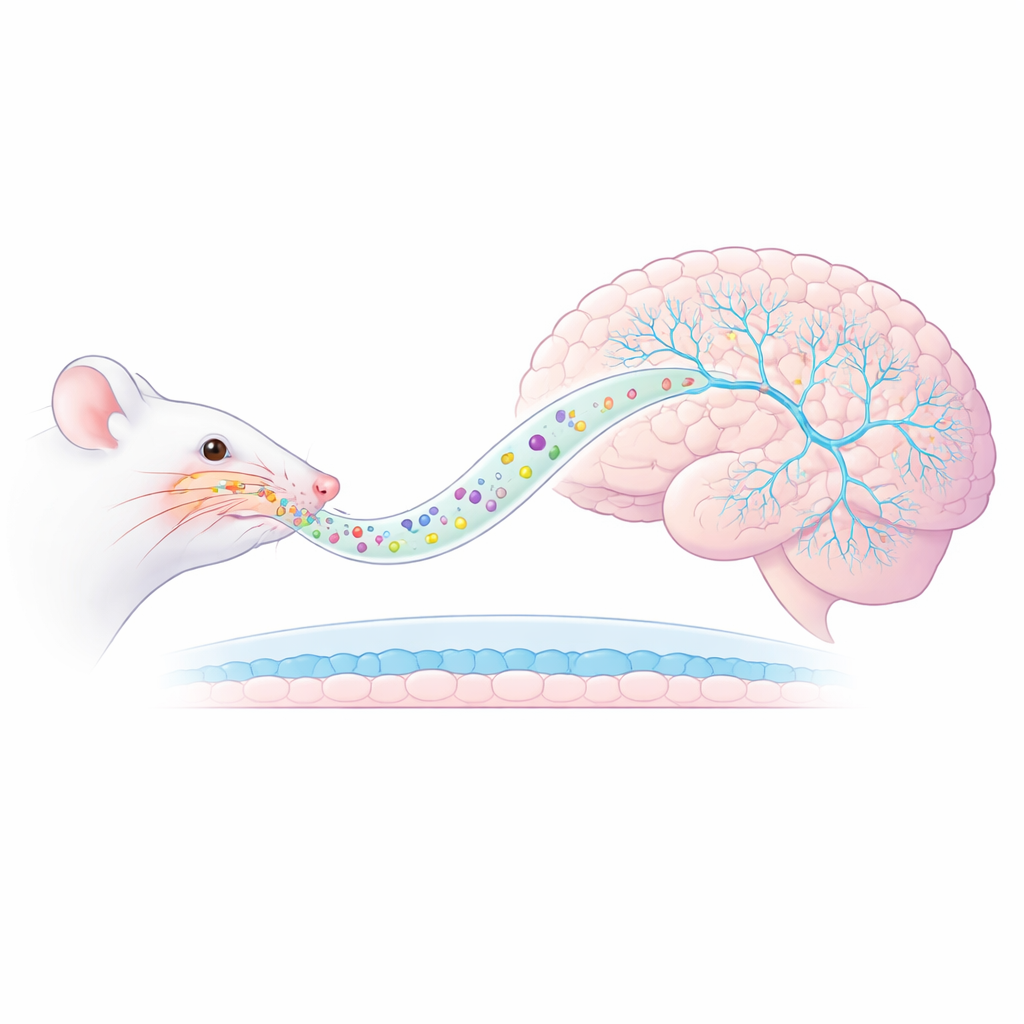
Een nieuw neus-naar-hersenen pad
De onderzoekers concentreerden zich op een rattenmodel van PTSS waarin dieren worden blootgesteld aan de geur van een predator, wat langdurige angst en overdreven reacties op herinneringen aan de dreiging oproept. In plaats van ketamine via injectie te geven, verpakten ze het in AmyloLipid-nanovesikels—nanometerschaal druppeltjes met een vetkern omhuld door een gemodificeerde zetmellaag. Wanneer in de neus gespoten, zijn deze deeltjes ontworpen om langs zenuwbanen rechtstreeks de hersenen te bereiken en zo de gebruikelijke bloed–hersenbarrière te omzeilen die de toegang van geneesmiddelen beperkt. Eerdere metingen toonden aan dat deze benadering de ketamineconcentratie in hersenweefsel sterk verhoogde terwijl de bloedspiegels laag bleven, wat wijst op meer gerichte toediening en mogelijk minder systeemwide bijwerkingen.
Testen van stress, angst en schrikreactie
Na de traumatische blootstelling kregen de ratten drie keer per week gedurende twee weken intranasale behandelingen: verschillende doses ketamine-geladen nanovesikels, lege nanovesikels, gewone ketamine-oplossing of zoutoplossing. Het team mat vervolgens hoe angstig de dieren leken in een verhoogd doolhof, hoe sterk ze schrokken van luide geluiden en hoeveel ze verstijfden wanneer ze opnieuw werden blootgesteld aan een onschuldige herinnering aan de predatorgeur. Ze verdeelden de individuele ratten ook in groepen die extreme, gedeeltelijke of minimale verstoring toonden, om na te bootsen hoe mensen verschillend op trauma reageren. Lage-dosis ketamine in nanovesikels—vooral 0,6 milligram per kilogram—viel op: het verminderde angstig-achtig gedrag, nam overdreven schrikreacties af en halveerden bijna het aandeel dieren met sterke PTSS-achtige reacties vergeleken met die een lege deeltje ontvingen. Daarentegen verhoogde de hoogste dosis bevriezing en angst, wat benadrukt dat meer medicijn niet altijd beter is.
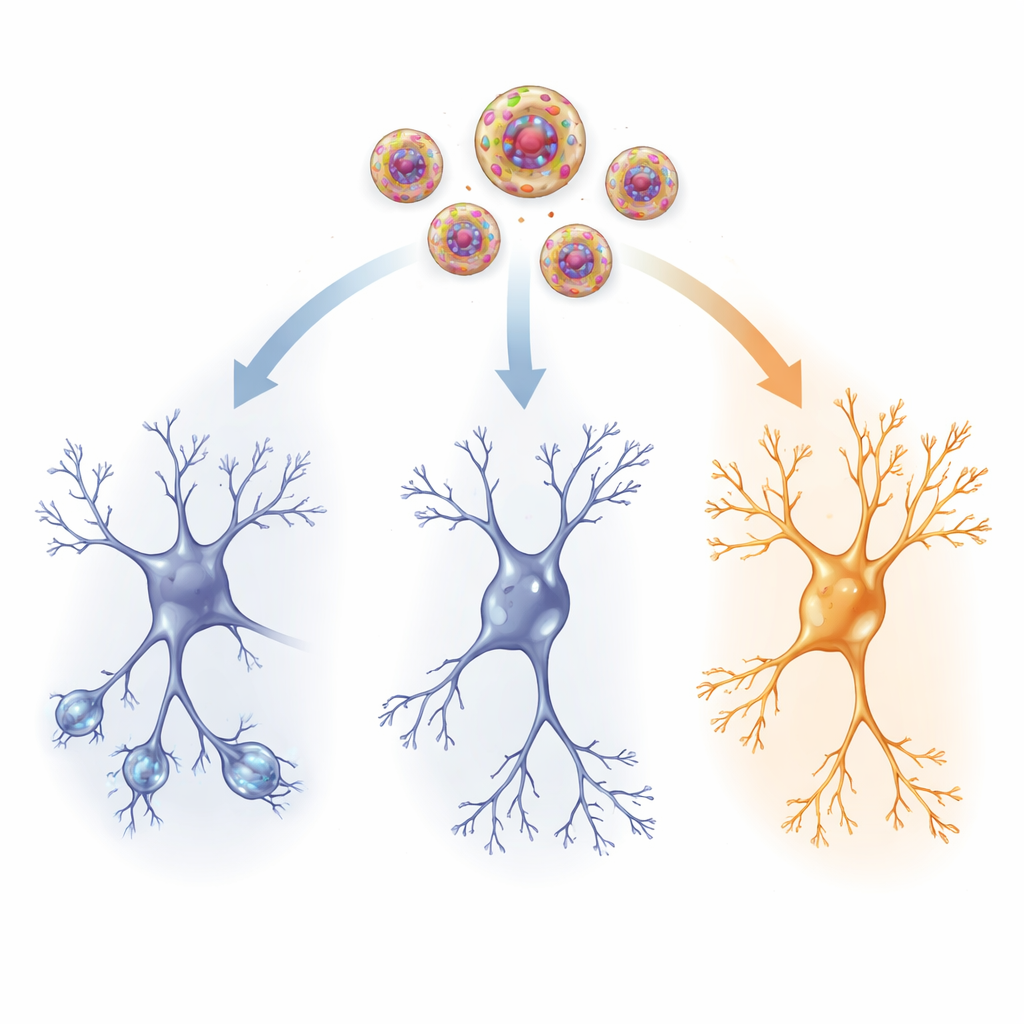
In de bedrading van de hersenen
Om te zien wat fysiek veranderde, onderzochten de onderzoekers een sleutelgebied voor geheugen, de hippocampus, en een stressregulerend knooppunt, de paraventriculaire nucleus van de hypothalamus. Bij getraumatiseerde ratten die geen actief middel kregen, hadden hippocampale zenuwcellen minder en kortere vertakkingen en minder kleine uitsteeksels (spines) waar synapsen ontstaan—tekens van verzwakte verbindingen. De niveaus van brain-derived neurotrophic factor (BDNF), een groeiondersteunend eiwit, en neuropeptide Y (NPY), een molecuul dat samenhangt met stressresistentie, waren ook verlaagd. Tegelijkertijd was er een toename van HCN1-kanalen, membraaneiwitten die bepalen hoe gemakkelijk neuronen vuren. Gezamenlijk wijzen deze verschuivingen op een hersennetwerk dat minder flexibel en minder responsief is na trauma.
Herstel van balans in zenuwcellen
Lage-dosis ketamine toegediend via nanovesikels keerde veel van deze schadekenmerken om. Neuronen bij behandelde ratten kregen langere en complexere vertakkingen en meer spines terug, vooral in de bovenste laag van de hippocampus waar verre inputs binnenkomen. BDNF- en NPY-niveaus stegen richting normaal in zowel de hippocampus als het stresscontrolegebied, wat suggereert dat er hernieuwde ondersteuning is voor celdoodpreventie, groei en veerkracht. Tegelijkertijd nam de abnormale toename van HCN1-kanalen af, wat hielp een gezond niveau van elektrische responsiviteit te herstellen. Deze structurele en chemische veranderingen kwamen nauw overeen met de gedragsverbeteringen, wat impliceert dat gerichte ketaminetoediening het getraumatiseerde brein helpt zich op een adaptievere manier te herbedraden.
Waarom dosis en toediening ertoe doen
De vergelijking tussen ketamine in nanovesikels en gewone ketamine-oplossing benadrukte het belang van de wijze en hoeveelheid van toediening. Bij lage doses presteerde het neus-naar-hersenen systeem beter dan standaard ketamine bij het verminderen van angstig-achtig gedrag, schrik en bevriezing. Bij de hoogste dosis leek ketamine in nanovesikels de stressreacties echter te verergeren, waarschijnlijk omdat meer medicijn in de bloedbaan terechtkwam, werd omgezet in actieve afbraakproducten en de hersenen bereikte via minder gerichte routes. Dit patroon suggereert dat er een smalle ‘sweet spot’ is waarin directe hersentoevoer bij lage dosis de gunstige effecten maximaliseert en ongewenste effecten minimaliseert.
Wat dit kan betekenen voor toekomstige zorg
In eenvoudige termen toont dit werk aan dat het voorzichtig toedienen van kleine hoeveelheden ketamine rechtstreeks van neus naar hersenen getraumatiseerde dieren rustiger en veerkrachtiger kan maken, terwijl het hun hersencellen helpt verbindingen te herbouwen en gezonde activiteit te herstellen. Hoewel de studie bij ratten is uitgevoerd, wijst het op een strategie voor de behandeling van PTSS die gebruikmaakt van slimme dragers en zorgvuldige dosering in plaats van alleen hogere hoeveelheden medicijn. Door HCN1-kanalen te sturen en groeifactoren en veerkrachtbevorderende moleculen zoals BDNF en NPY te versterken, kan intranasaal ketamine in AmyloLipid-nanovesikels mogelijk een meer precieze, duurzamere en veiligere manier bieden om het brein te helpen herstellen van ernstige stress.
Bronvermelding: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Trefwoorden: PTSS, ketamine, intranasaal toediening, nanodeeltjes, neuroplasticiteit