Clear Sky Science · es
Impacto de ketamina subanestésica administrada mediante un sistema intranasal basado en nanovesículas AmyloLipid (ALN) sobre las respuestas bioconductuales en un modelo animal de TEPT
Ayudando al cerebro a recuperarse del trauma
El trastorno por estrés postraumático (TEPT) puede persistir durante años, dejando a las personas atrapadas en ciclos de miedo, ansiedad y recuerdos intrusivos. Muchos tratamientos actuales funcionan solo parcialmente o muy lentamente. Este estudio explora una nueva vía para administrar un fármaco bien conocido, la ketamina, directamente al cerebro a través de la nariz utilizando diminutas burbujas de grasa y almidón. La esperanza es aumentar el beneficio, reducir los efectos secundarios y apoyar mejor la capacidad del cerebro para adaptarse y recuperarse tras el trauma.
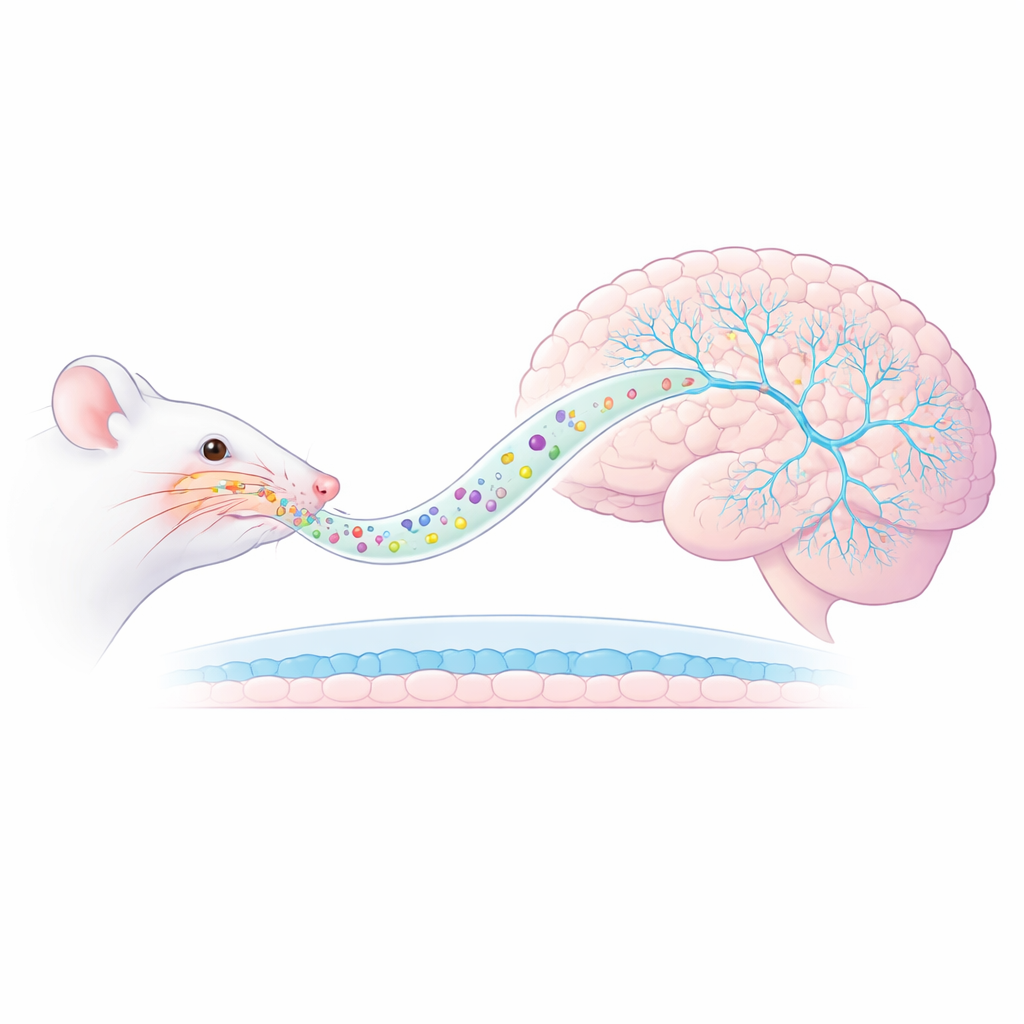
Una nueva vía de la nariz al cerebro
Los investigadores se centraron en un modelo de TEPT en ratas en el que los animales se exponen al olor de un depredador, desencadenando ansiedad duradera y respuestas exageradas a los recordatorios de la amenaza. En lugar de administrar ketamina por inyección, la encapsularon dentro de nanovesículas AmyloLipid: gotas a escala nanométrica con un núcleo graso envuelto en una cápsula de almidón modificada. Al pulverizarse en la nariz, estas partículas están diseñadas para viajar a lo largo de vías nerviosas directamente hacia el cerebro, sorteando la barrera hematoencefálica habitual que limita la entrada de fármacos. Mediciones previas mostraron que este enfoque aumentó considerablemente los niveles de ketamina en el tejido cerebral mientras mantenía bajos los niveles en sangre, lo que sugiere una administración más dirigida y, potencialmente, menos efectos secundarios sistémicos.
Evaluando estrés, miedo y sobresalto
Tras la exposición traumática, las ratas recibieron tratamientos intranasales tres veces por semana durante dos semanas: diferentes dosis de nanovesículas cargadas con ketamina, nanovesículas vacías, solución de ketamina simple o suero salino. El equipo midió luego cuánto parecían ansiosos los animales en un laberinto elevado, con qué intensidad se sobresaltaban ante sonidos fuertes y cuánto tiempo permanecían inmóviles (freezing) cuando se reexponían a un recordatorio inofensivo del olor del depredador. También clasificaron a las ratas en grupos que mostraban alteración extrema, parcial o mínima, imitando cómo las personas difieren en sus respuestas al trauma. La ketamina en nanovesículas a baja dosis —especialmente 0,6 miligramos por kilogramo— destacó: redujo conductas ansiosas, disminuyó las respuestas de sobresalto exageradas y redujo en casi la mitad la proporción de animales con reacciones tipo TEPT fuertes en comparación con los que recibieron partículas vacías. En contraste, la dosis más alta aumentó el freezing y la ansiedad, subrayando que más fármaco no siempre es mejor.
Dentro del cableado del cerebro
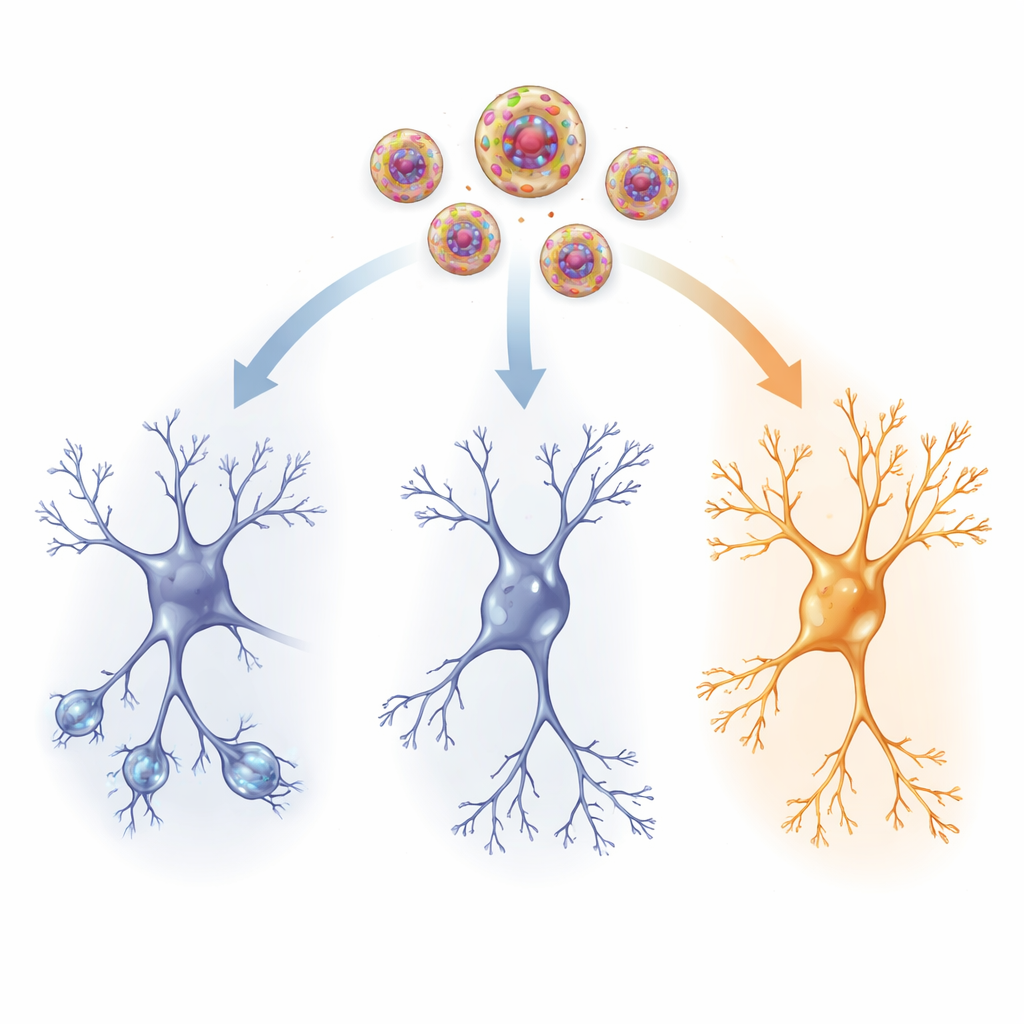
Para ver qué cambiaba físicamente, los investigadores examinaron una región clave de la memoria, el hipocampo, y un centro de control del estrés, el núcleo paraventricular del hipotálamo. En las ratas traumatizadas que no recibieron fármaco activo, las células nerviosas del hipocampo tenían ramas más cortas y menos numerosos, y menos espinas diminutas donde se forman las sinapsis —señales de conexiones debilitadas. Los niveles del factor neurotrófico derivado del cerebro (BDNF), una proteína que apoya el crecimiento, y del neuropéptido Y (NPY), una molécula ligada a la resiliencia al estrés, también estaban reducidos. Al mismo tiempo, hubo un aumento en los canales HCN1, proteínas en la membrana celular que influyen en la facilidad con la que disparan las neuronas. En conjunto, estos cambios apuntan a una red cerebral menos flexible y menos receptiva tras el trauma.
Restaurando el equilibrio en las neuronas
La ketamina a baja dosis administrada mediante nanovesículas revirtió muchos de estos signos de daño. Las neuronas en las ratas tratadas recuperaron ramas más largas y complejas y más espinas, especialmente en la capa más superficial del hipocampo donde llegan entradas distantes. Los niveles de BDNF y NPY aumentaron hacia la normalidad tanto en el hipocampo como en la región de control del estrés, lo que sugiere un renovado apoyo para la supervivencia, el crecimiento y la resiliencia celular. Al mismo tiempo, la subida anómala de canales HCN1 disminuyó, ayudando a restaurar un nivel saludable de respuesta eléctrica. Estos cambios estructurales y químicos coincidieron estrechamente con las mejoras conductuales, lo que implica que la administración dirigida de ketamina ayuda al cerebro traumatizado a reconectarse de forma más adaptativa.
Por qué importan la dosis y la vía de administración
La comparación de la ketamina en nanovesículas con la solución de ketamina ordinaria puso de relieve la importancia de cómo y cuánto fármaco se administra. A bajas dosis, el sistema de nariz a cerebro superó a la ketamina estándar en aliviar conductas ansiosas, el sobresalto y el freezing. Sin embargo, en la dosis más alta, la ketamina en nanovesículas pareció empeorar las respuestas al estrés, probablemente porque más fármaco escapó al torrente sanguíneo, se transformó en productos de degradación activos y alcanzó el cerebro por rutas menos dirigidas. Este patrón sugiere que existe un “punto óptimo” estrecho donde la administración directa al cerebro a baja dosis maximiza los efectos beneficiosos y minimiza los indeseados.
Qué podría significar esto para la atención futura
En términos sencillos, este trabajo muestra que enviar suavemente pequeñas cantidades de ketamina directamente desde la nariz al cerebro puede hacer que los animales traumatizados estén más calmados y resilientes, al tiempo que ayuda a que sus células cerebrales vuelvan a crecer conexiones y recuperen una actividad saludable. Aunque el estudio se realizó en ratas, apunta hacia una estrategia para tratar el TEPT que usa transportadores inteligentes y dosificación cuidadosa en lugar de simplemente aumentar la cantidad de fármaco. Al modular los canales HCN1 y aumentar moléculas de crecimiento y resiliencia como BDNF y NPY, la ketamina intranasal en nanovesículas AmyloLipid podría algún día ofrecer una forma más precisa, duradera y segura de ayudar al cerebro a sanar tras un estrés severo.
Cita: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Palabras clave: TEPT, ketamina, administración intranasal, nanopartículas, neuroplasticidad