Clear Sky Science · fr
Impact de la kétamine sous-anesthésique administrée via un système intranasal basé sur des nanovésicules AmyloLipid (ALN) sur les réponses biocomportementales dans un modèle animal de trouble de stress post-traumatique
Aider le cerveau à guérir après un traumatisme
Le trouble de stress post-traumatique (TSPT) peut perdurer des années, emprisonnant les personnes dans des cycles de peur, d’anxiété et de souvenirs intrusifs. De nombreux traitements actuels ne fonctionnent que partiellement ou agissent très lentement. Cette étude explore une nouvelle façon d’administrer un médicament bien connu, la kétamine, directement au cerveau par le nez à l’aide de minuscules bulles de lipides et d’amidon. L’objectif est d’accroître les bénéfices, de réduire les effets secondaires et de mieux soutenir la capacité du cerveau à s’adapter et à récupérer après un traumatisme.
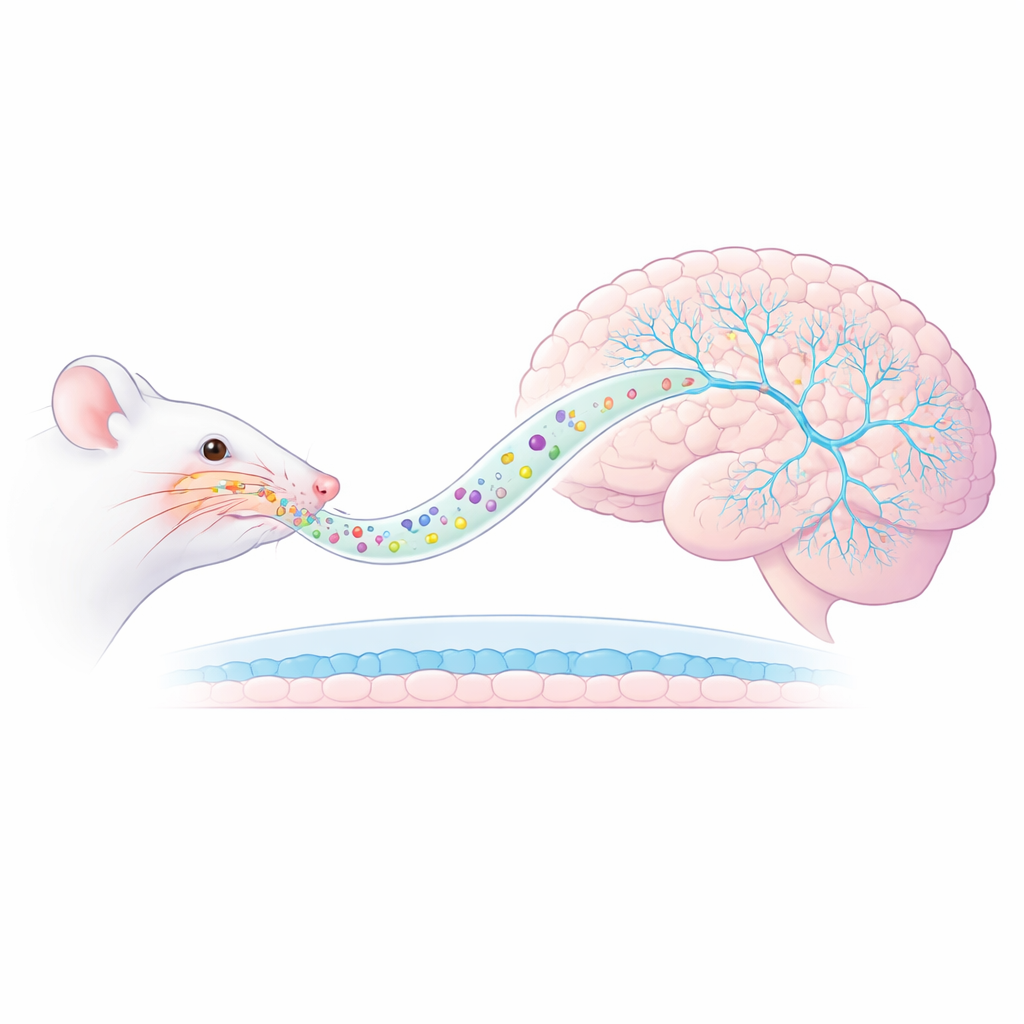
Une nouvelle voie nez–cerveau
Les chercheurs se sont concentrés sur un modèle de TSPT chez le rat dans lequel les animaux sont exposés à une odeur de prédateur, déclenchant une anxiété durable et des réactions exagérées aux rappels de la menace. Plutôt que d’administrer la kétamine par injection, ils l’ont encapsulée dans des nanovésicules AmyloLipid — des gouttelettes de l’ordre du nanomètre avec un cœur gras entouré d’une coque d’amidon modifiée. Lorsqu’elles sont pulvérisées dans le nez, ces particules sont conçues pour emprunter des voies nerveuses et atteindre directement le cerveau, contournant la barrière hémato‑encéphalique habituelle qui limite l’entrée des médicaments. Des mesures antérieures ont montré que cette approche augmentait fortement les concentrations de kétamine dans le tissu cérébral tout en maintenant de faibles niveaux sanguins, suggérant une distribution plus ciblée et potentiellement moins d’effets indésirables systémiques.
Évaluer stress, peur et sursaut
Après l’exposition traumatique, les rats ont reçu des traitements intranasaux trois fois par semaine pendant deux semaines : différentes doses de nanovésicules chargées en kétamine, des nanovésicules vides, une solution de kétamine ordinaire ou du sérum physiologique. L’équipe a ensuite mesuré l’anxiété apparente des animaux dans un labyrinthe surélevé, leur intensité de sursaut face à des sons forts, et leur comportement d’immobilité lorsqu’ils étaient réexposés à un rappel inoffensif de l’odeur du prédateur. Ils ont aussi classé les rats individuels en groupes affichant des troubles extrêmes, partiels ou minimes, reproduisant la variabilité humaine dans les réponses au traumatisme. La kétamine à faible dose dans des nanovésicules — en particulier 0,6 milligramme par kilogramme — s’est distinguée : elle a réduit les comportements anxieux, amoindri les réponses de sursaut exagérées et diminué de près de moitié la proportion d’animaux présentant des réactions de type TSPT comparé aux particules vides. En revanche, la dose la plus élevée a augmenté l’immobilité et l’anxiété, soulignant que plus de médicament n’est pas toujours mieux.
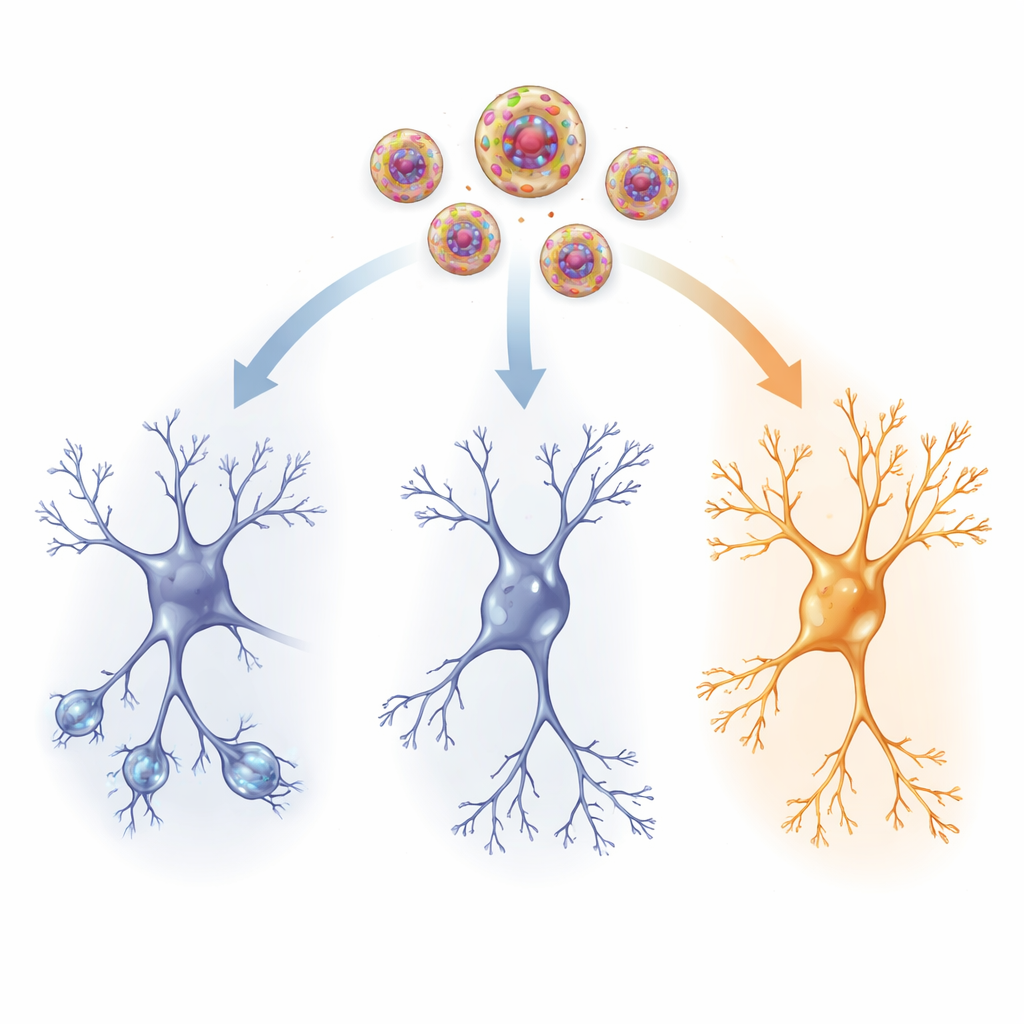
Dans le câblage du cerveau
Pour observer les changements physiques, les chercheurs ont examiné une région clé de la mémoire, l’hippocampe, et un centre de contrôle du stress, le noyau paraventriculaire de l’hypothalamus. Chez les rats traumatisés qui n’avaient reçu aucun médicament actif, les cellules nerveuses de l’hippocampe présentaient des branches moins nombreuses et plus courtes et moins de petites épines où se forment les synapses — signes de connexions affaiblies. Les niveaux de facteur neurotrophique dérivé du cerveau (BDNF), une protéine favorisant la croissance, et de neuropeptide Y (NPY), une molécule liée à la résilience au stress, étaient également réduits. Parallèlement, on observait une augmentation des canaux HCN1, protéines membranaires qui modulant la facilité de décharge des neurones. Ensemble, ces modifications témoignent d’un réseau cérébral moins flexible et moins réactif après un traumatisme.
Rétablir l’équilibre des neurones
La kétamine à faible dose administrée via les nanovésicules a inversé bon nombre de ces signes de dommage. Les neurones des rats traités ont retrouvé des branches plus longues et plus complexes et davantage d’épines, en particulier dans la couche la plus superficielle de l’hippocampe où arrivent les entrées distales. Les niveaux de BDNF et de NPY sont remontés vers la normale à la fois dans l’hippocampe et dans le centre de contrôle du stress, suggérant un soutien renouvelé à la survie, à la croissance et à la résilience cellulaires. Parallèlement, la hausse anormale des canaux HCN1 a diminué, contribuant à rétablir un niveau sain de réactivité électrique. Ces changements structurels et biochimiques correspondaient étroitement aux améliorations comportementales, ce qui suggère qu’une administration ciblée de kétamine aide le cerveau traumatisé à se reconfigurer de façon plus adaptative.
Pourquoi la dose et la voie d’administration comptent
La comparaison entre la kétamine en nanovésicules et la solution de kétamine ordinaire a mis en évidence l’importance du mode et de la quantité de médicament administrés. À faibles doses, le système nez–cerveau a surpassé la kétamine standard pour réduire l’anxiété, le sursaut et l’immobilité. Toutefois, à la dose la plus élevée, la kétamine en nanovésicules a semblé aggraver les réponses au stress, probablement parce qu’une plus grande quantité de médicament a atteint la circulation sanguine, s’est transformée en métabolites actifs et a atteint le cerveau par des voies moins ciblées. Ce schéma suggère l’existence d’une « zone optimale » étroite où une livraison directe au cerveau à faible dose maximise les effets bénéfiques tout en minimisant les effets indésirables.
Ce que cela pourrait signifier pour les soins futurs
En termes simples, ce travail montre que l’envoi doux de faibles quantités de kétamine directement du nez au cerveau peut rendre les animaux traumatisés plus calmes et plus résilients, tout en aidant leurs cellules cérébrales à recréer des connexions et à retrouver une activité saine. Bien que l’étude ait été réalisée chez le rat, elle indique une stratégie pour traiter le TSPT qui mise sur des vecteurs intelligents et un dosage précis plutôt que sur une augmentation des quantités de médicament. En modulant les canaux HCN1 et en renforçant des molécules de croissance et de résilience telles que le BDNF et le NPY, la kétamine intranasale dans des nanovésicules AmyloLipid pourrait un jour offrir un moyen plus précis, plus durable et plus sûr d’aider le cerveau à se remettre d’un stress sévère.
Citation: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Mots-clés: TSPT, kétamine, administration intranasale, nanoparticules, neuroplasticité