Clear Sky Science · it
Impatto della ketamina subanestetica somministrata tramite un sistema intranasale a base di nanovesicole AmyloLipid (ALN) sulle risposte biocomportamentali in un modello animale di PTSD
Aiutare il cervello a guarire dal trauma
Il disturbo post-traumatico da stress (PTSD) può persistere per anni, lasciando le persone intrappolate in cicli di paura, ansia e ricordi intrusivi. Molti trattamenti attuali funzionano solo parzialmente o molto lentamente. Questo studio esplora un nuovo modo di somministrare un farmaco noto, la ketamina, direttamente al cervello attraverso il naso usando piccole bolle di grasso e amido. L’obiettivo è aumentare i benefici, ridurre gli effetti collaterali e sostenere meglio la capacità del cervello di adattarsi e recuperare dopo il trauma.
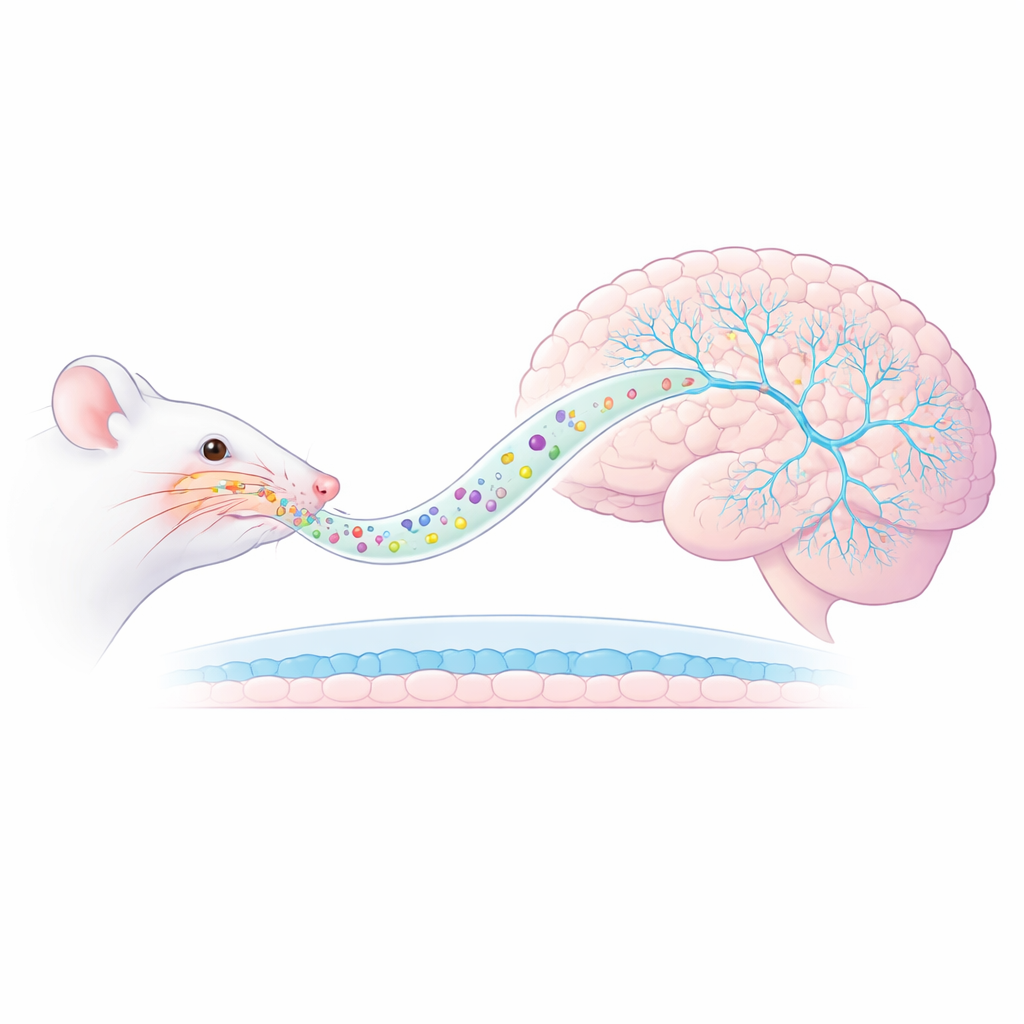
Una nuova via dal naso al cervello
I ricercatori si sono concentrati su un modello di PTSD nel ratto in cui gli animali sono esposti all’odore di un predatore, scatenando ansia di lunga durata e risposte esagerate ai richiami della minaccia. Invece di somministrare la ketamina per iniezione, l’hanno incapsulata all’interno di nanovesicole AmyloLipid—goccioline su scala nanometrica con un nucleo grasso avvolto da un involucro di amido modificato. Quando nebulizzate nel naso, queste particelle sono progettate per viaggiare lungo le vie nervose direttamente nel cervello, aggirando la normale barriera emato-encefalica che limita l’ingresso dei farmaci. Misurazioni precedenti hanno mostrato che questo approccio aumenta notevolmente i livelli di ketamina nel tessuto cerebrale mantenendo bassi i livelli ematici, suggerendo una somministrazione più mirata e potenzialmente meno effetti collaterali sistemici.
Valutare stress, paura e sobbalzo
Dopo l’esposizione traumatica, i ratti hanno ricevuto trattamenti intranasali tre volte alla settimana per due settimane: diverse dosi di nanovesicole cariche di ketamina, nanovesicole vuote, soluzione di ketamina semplice o soluzione salina. Il team ha poi misurato quanto gli animali apparivano ansiosi in un labirinto elevato, quanto forte fosse il loro sobbalzo a suoni forti e quanto si immobilizzassero quando riesposti a un richiamo innocuo dell’odore del predatore. Hanno anche classificato i singoli ratti in gruppi che mostravano disturbo estremo, parziale o minimo, imitando come le persone differiscono nelle risposte al trauma. La ketamina a bassa dose nelle nanovesicole—in particolare 0,6 milligrammi per chilogrammo—si è distinta: ha ridotto i comportamenti simili all’ansia, attenuato le risposte di sobbalzo esagerate e dimezzato quasi la percentuale di animali con reazioni forti simili al PTSD rispetto a quelli trattati con particelle vuote. Al contrario, la dose più alta ha aumentato l’immobilità e l’ansia, sottolineando che più farmaco non è sempre migliore.
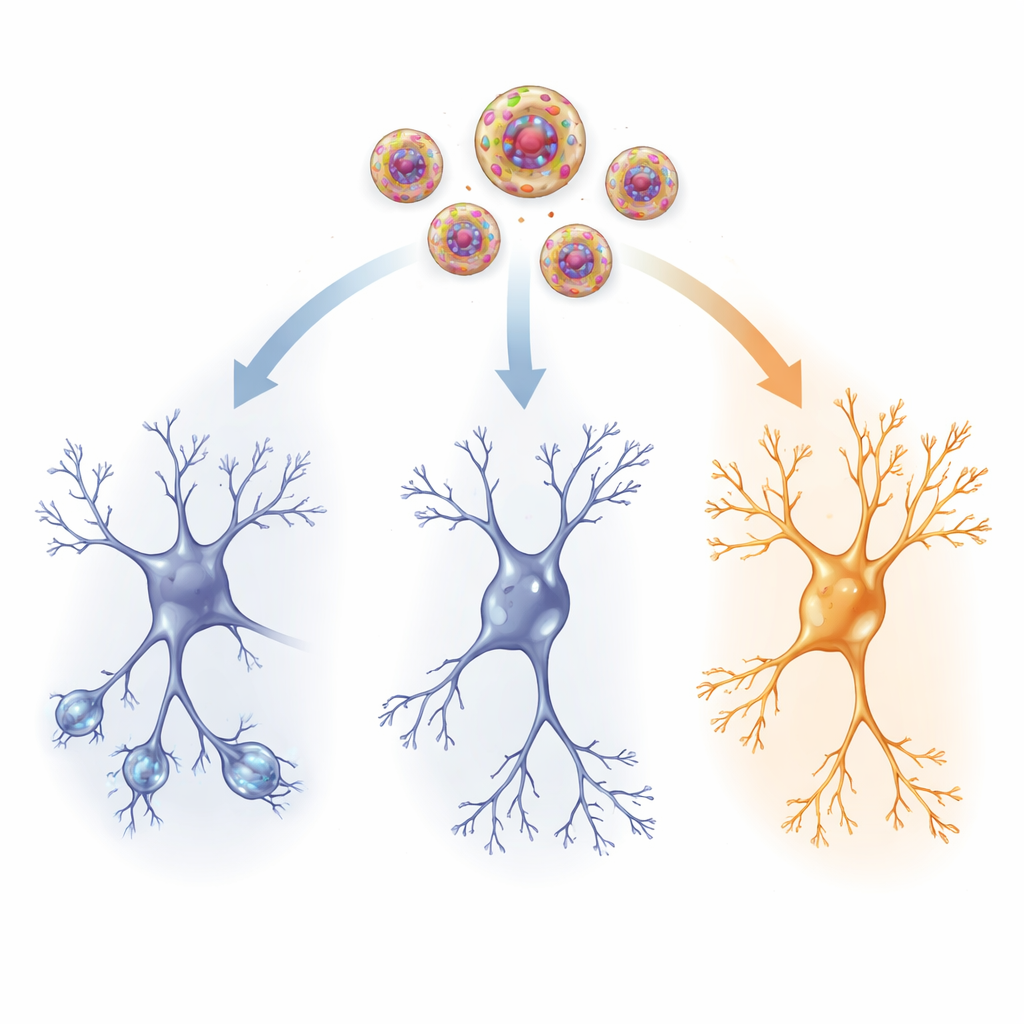
All’interno dell’architettura cerebrale
Per vedere cosa cambiava a livello fisico, i ricercatori hanno esaminato una regione chiave della memoria, l’ippocampo, e un centro di controllo dello stress, il nucleo paraventricolare dell’ipotalamo. Nei ratti traumatizzati che non hanno ricevuto farmaco attivo, le cellule nervose dell’ippocampo avevano rami più corti e meno numerosi e meno piccole spine dove si formano le sinapsi—segni di connessioni indebolite. Anche i livelli del fattore neurotrofico derivato dal cervello (BDNF), una proteina che sostiene la crescita, e del neuropeptide Y (NPY), una molecola legata alla resilienza allo stress, erano ridotti. Allo stesso tempo, si è osservato un aumento dei canali HCN1, proteine nella membrana cellulare che influenzano la facilità con cui i neuroni si attivano. Nel loro insieme, questi cambiamenti indicano una rete cerebrale meno flessibile e meno reattiva dopo il trauma.
Ripristinare l’equilibrio nelle cellule nervose
La ketamina a bassa dose somministrata tramite nanovesicole ha invertito molti di questi segni di danno. I neuroni nei ratti trattati hanno recuperato rami più lunghi e complessi e un maggior numero di spine, specialmente nello strato più superficiale dell’ippocampo dove arrivano input distali. I livelli di BDNF e NPY sono risaliti verso la normalità sia nell’ippocampo sia nella regione di controllo dello stress, suggerendo un rinnovato supporto per la sopravvivenza cellulare, la crescita e la resilienza. Contemporaneamente, la crescita anomala dei canali HCN1 si è attenuata, contribuendo a ristabilire un livello sano di reattività elettrica. Questi cambiamenti strutturali e chimici corrispondevano strettamente ai miglioramenti comportamentali, implicando che la somministrazione mirata di ketamina aiuta il cervello traumatizzato a riorganizzarsi in modo più adattivo.
Perché dose e modalità di somministrazione contano
Il confronto tra ketamina in nanovesicole e soluzione di ketamina ordinaria ha messo in evidenza l’importanza di come e quanto farmaco viene somministrato. A basse dosi, il sistema naso-cervello ha superato la ketamina standard nel ridurre comportamenti ansiosi, il sobbalzo e l’immobilità. Tuttavia, alla dose più alta, la ketamina nelle nanovesicole sembrava peggiorare le risposte allo stress, probabilmente perché più farmaco è sfuggito nel flusso sanguigno, è stato trasformato in metaboliti attivi e ha raggiunto il cervello tramite vie meno mirate. Questo schema suggerisce l’esistenza di una stretta “finestra terapeutica” in cui la somministrazione diretta al cervello a bassa dose massimizza gli effetti utili riducendo quelli indesiderati.
Cosa potrebbe significare per le cure future
In termini semplici, questo lavoro mostra che inviare delicatamente piccole quantità di ketamina direttamente dal naso al cervello può rendere gli animali traumatizzati più calmi e resilienti, aiutando nel contempo le loro cellule cerebrali a ricostruire connessioni e a ritrovare un’attività sana. Sebbene lo studio sia stato condotto su ratti, indica una strategia per trattare il PTSD che utilizza vettori intelligenti e dosaggi accurati anziché quantità maggiori di farmaco. Mettendo a punto i canali HCN1 e aumentando molecole di crescita e resilienza come BDNF e NPY, la ketamina intranasale in nanovesicole AmyloLipid potrebbe un giorno offrire un modo più preciso, duraturo e sicuro per aiutare il cervello a guarire dallo stress severo.
Citazione: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Parole chiave: PTSD, ketamina, somministrazione intranasale, nanoparticelle, neuroplasticità