Clear Sky Science · tr
AmiloLipid nanovesikül (ALN) bazlı intranazal sistemle verilen subanestezik ketaminin, bir PTSD hayvan modelinde biyolojik-davranışsal tepkiler üzerine etkisi
Travmanın Beyni İyileştirmesine Yardım Etmek
Travma Sonrası Stres Bozukluğu (PTSD) yıllarca sürebilir ve insanları korku, kaygı ve müdahaleci anılar döngüsünde sıkışmış bırakabilir. Mevcut tedavilerin birçoğu ya kısmen etkilidir ya da çok yavaş etki gösterir. Bu çalışma, iyi bilinen bir ilaç olan ketamini, burun yoluyla doğrudan beyne ulaştırmak için küçük yağ ve nişasta kabarcıkları kullanan yeni bir teslim yöntemi araştırıyor. Amaç, yararı artırmak, yan etkileri azaltmak ve travma sonrası beynin kendi uyum ve iyileşme kapasitesini daha iyi desteklemektir.
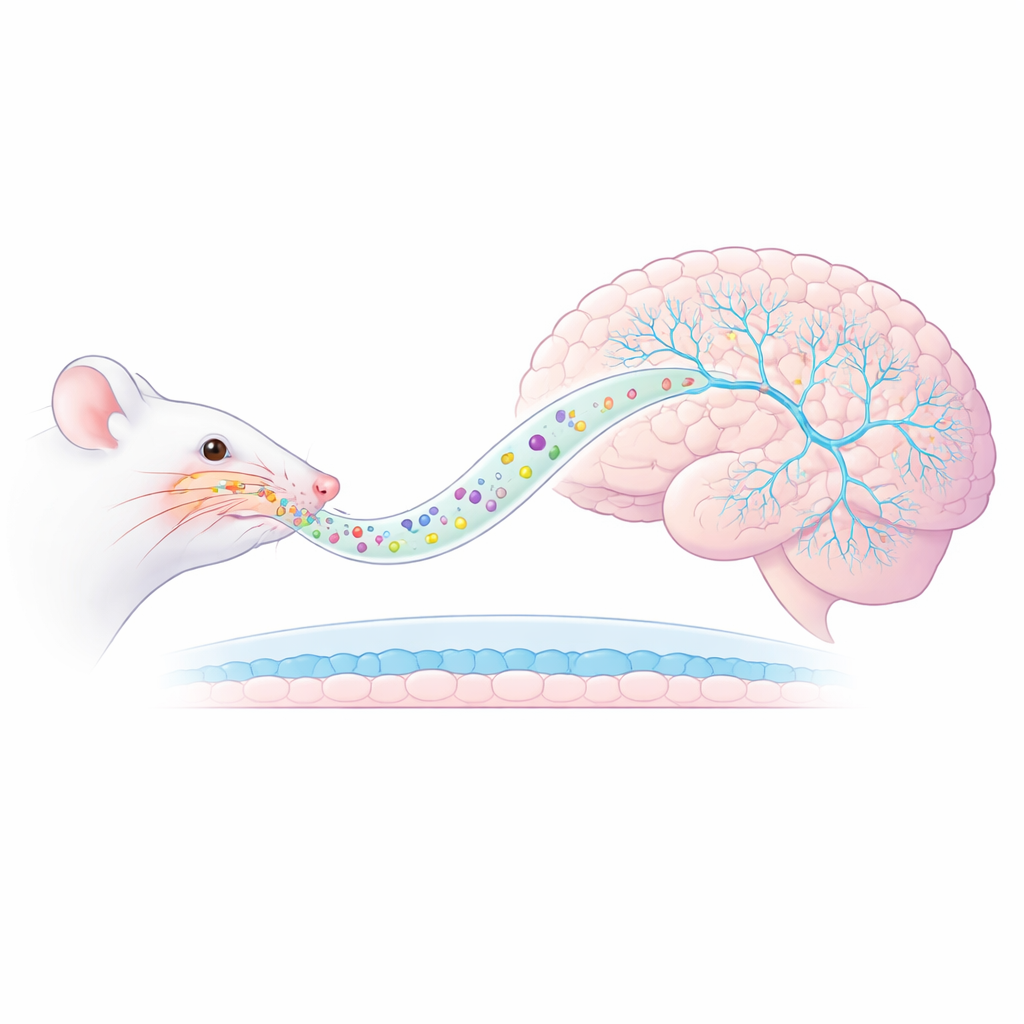
Burun-Beyin İçin Yeni Bir Yol
Araştırmacılar, hayvanların bir avcı kokusuna maruz bırakıldığı ve bunun uzun süreli anksiyete ile tehdide dair hatırlatmalara aşırı tepkiler tetiklediği bir sıçan PTSD modeline odaklandı. Ketamini enjeksiyonla vermek yerine, onu AmyloLipid nanovesiküllerinin içine paketlediler—modifiye nişasta kabuğa sarılmış yağlı bir çekirdeğe sahip nanometre ölçeğinde damlacıklar. Nazal sprey olarak uygulandıklarında, bu partiküllerin klasik kan-beyin bariyerini atlatarak sinir yolları boyunca doğrudan beyne gitmesi amaçlanır. Önceki ölçümler, bu yaklaşımın beyin dokusunda ketamin düzeylerini büyük oranda artırırken kan düzeylerini düşük tuttuğunu gösterdi; bu da daha hedeflenmiş bir teslim ve muhtemelen daha az bütün vücut yan etkisi olduğunu düşündürüyor.
Stres, Korku ve Sıçrama Tepkilerini Test Etme
Travmatik maruziyetin ardından, sıçanlara iki hafta boyunca haftada üç kez intranazal uygulamalar verildi: farklı dozlarda ketamin yüklü nanovesiküller, boş nanovesiküller, düz ketamin çözeltisi veya salin. Araştırma ekibi daha sonra hayvanların yükseltilmiş bir labirentte ne kadar kaygılı göründüğünü, yüksek seslere karşı ne kadar şiddetle sıçradıklarını ve avcı kokusunun zararsız bir hatırlatıcısına yeniden maruz kaldıklarında ne kadar donup kaldıklarını ölçtü. Ayrıca bireysel sıçanları aşırı, kısmi veya minimum bozulma gösteren gruplara ayırdılar; bu, insanların travmaya verdikleri yanıtların nasıl farklılık gösterdiğini taklit eder. Düşük doz ketamin içeren nanovesiküller—özellikle kilogram başına 0,6 miligram—öne çıktı: kaygı benzeri davranışları azalttı, abartılı sıçrama tepkilerini düşürdü ve boş partiküller verilenlere kıyasla güçlü PTSD-benzeri reaksiyon gösteren hayvanların oranını yaklaşık yarı yarıya azalttı. Buna karşılık, en yüksek doz donma ve kaygıyı artırdı; bu da daha fazla ilacın her zaman daha iyi olmadığını vurguluyor.
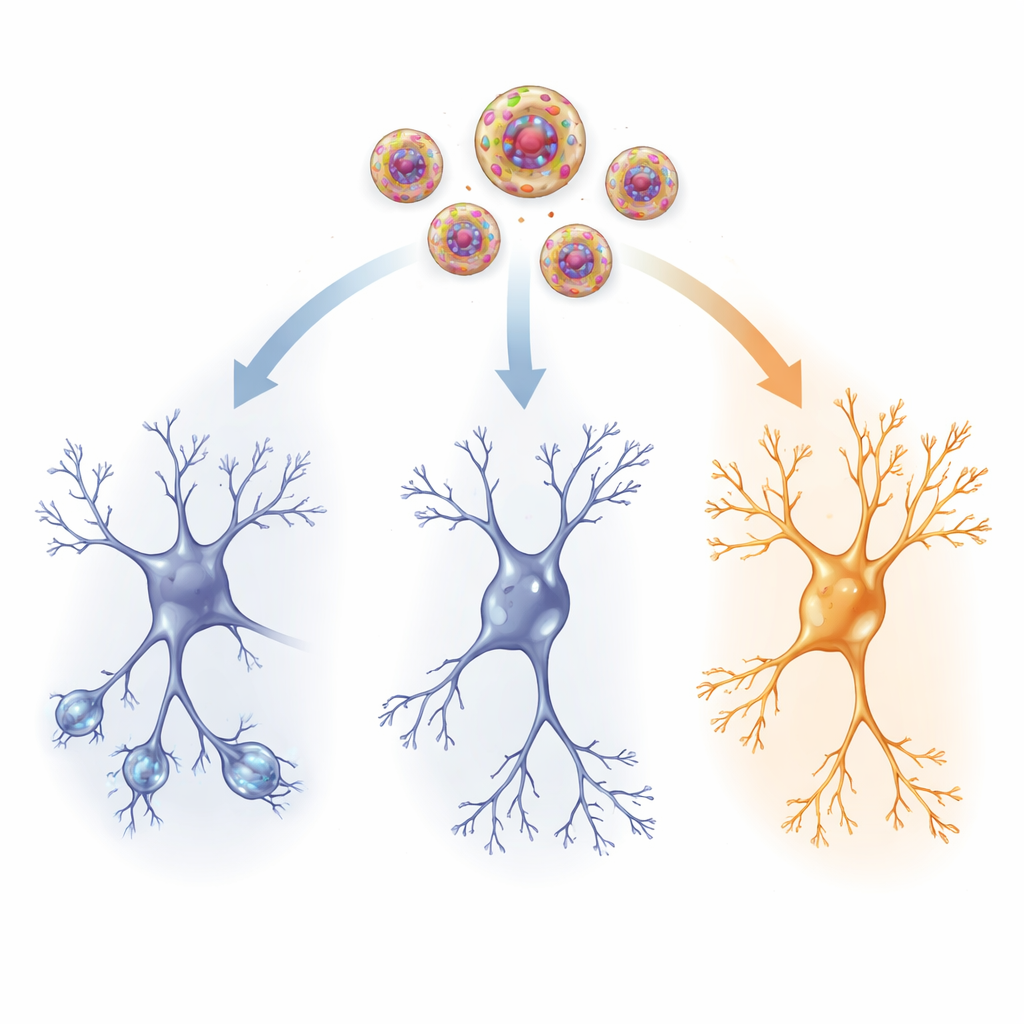
Beynin Devreleri İçinde
Fiziksel olarak nelerin değiştiğini görmek için araştırmacılar önemli bir hafıza bölgesi olan hipokampusu ve stres kontrolünde rol oynayan bir merkez olan hipotalamus paraventriküler çekirdeğini incelediler. Aktif ilaç almayan travmatize sıçanlarda, hipokampustaki sinir hücreleri daha az ve daha kısa dallanma ile sinapsların oluştuğu küçük dikenciklerin daha az olması gibi zayıflamış bağlantı göstergeleri sergiledi. Büyümeyi destekleyen bir protein olan beyin kaynaklı nörotrofik faktör (BDNF) ile stres dirençliliğiyle ilişkili nöropeptid Y (NPY) seviyeleri de azalmıştı. Aynı zamanda, hücre zarında nöronların ateşlenme kolaylığını şekillendiren HCN1 kanallarında artış gözlendi. Birlikte bu değişiklikler, travma sonrası daha az esnek ve daha az yanıt veren bir beyin ağına işaret ediyor.
Sinir Hücrelerinde Dengenin Yeniden Sağlanması
Nanovesiküller yoluyla verilen düşük doz ketamin bu hasar belirtilerinin çoğunu tersine çevirdi. Tedavi edilen sıçanlarda nöronlar daha uzun ve daha karmaşık dallanma ile özellikle uzak girişlerin ulaştığı hipokampusun en üst katmanında daha fazla dikençik kazandı. BDNF ve NPY düzeyleri hem hipokampusta hem de stres kontrol bölgesinde normale doğru yükseldi; bu, hücre hayatta kalması, büyüme ve direnç için yenilenmiş bir desteğe işaret ediyor. Aynı zamanda HCN1 kanallarındaki anormal artış azaldı ve elektriksel yanıt verebilirliğin sağlıklı bir düzeye kavuşmasına yardımcı oldu. Bu yapısal ve kimyasal değişiklikler davranışsal gelişmelerle yakından eşleşti; bu da hedeflenmiş ketamin uygulamasının travmatize beyinin daha uyumlu bir şekilde yeniden devreye girmesine yardımcı olduğunu gösteriyor.
Doz ve Uygulamanın Neden Önemi Var
Nanovesikül bazlı ketamini sıradan ketamin çözeltisiyle karşılaştırmak, ilacın nasıl ve ne kadar verildiğinin önemini vurguladı. Düşük dozlarda burun-beyin sistemi, anksiyete benzeri davranış, sıçrama ve donma tepkilerini hafifletmede standart ketaminden daha iyi performans gösterdi. Ancak en yüksek dozda, nanovesiküllerdeki ketamin stres tepkilerini kötüleştirmiş gibi göründü; muhtemelen daha fazla ilacın kana karışması, aktif yıkım ürünlerine dönüşmesi ve daha az hedeflenmiş yollarla beyne ulaşması nedeniyle. Bu desen, düşük dozda doğrudan beyin tesliminin yararlı etkileri maksimize ederken istenmeyenleri en aza indiren dar bir “tatlı nokta” olduğunu öne sürüyor.
Gelecekteki Bakım İçin Ne Anlama Gelebilir
Basitçe söylemek gerekirse, bu çalışma burundan beyne küçük miktarlarda ketamin gönderilmesinin travmatize hayvanları daha sakin ve dayanıklı hale getirebileceğini ve beyin hücrelerinin bağlantılarını yeniden büyütmesine ve sağlıklı aktiviteyi yeniden kazanmasına yardımcı olabileceğini gösteriyor. Çalışma sıçanlarda yapılmış olsa da, akıllı taşıyıcılar ve dikkatli dozlamayı kullanan bir PTSD tedavi stratejisine işaret ediyor; sadece ilaç miktarını artırmak yerine daha hassas bir yaklaşım sunuyor. HCN1 kanallarını ayarlayarak ve BDNF ile NPY gibi büyüme ve direnç moleküllerini artırarak, AmiloLipid nanovesiküllerinde intranazal ketamin bir gün şiddetli stresten etkilenen beynin iyileşmesine daha kesin, daha kalıcı ve daha güvenli bir yol sunabilir.
Atıf: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Anahtar kelimeler: PTSD, ketamin, intrnazal uygulama, nanopartiküller, nöroplastisite