Clear Sky Science · ar
تأثير الكيتامين دون تأثير مخدر كامل المُعطى عبر نظام داخل الأنف قائم على حويصلات نانوية AmyloLipid (ALN) على الاستجابات السلوكية والبيولوجية في نموذج حيواني للاكتئاب التالي للصدمة (PTSD)
مساعدة الدماغ على الشفاء من الصدمة
يمكن أن يستمر اضطراب ما بعد الصدمة (PTSD) لسنوات، ويترك الأشخاص محاصرين في دوائر من الخوف والقلق والذكريات المتطفلة. العديد من العلاجات الحالية تعمل جزئياً أو ببطء شديد. تستكشف هذه الدراسة طريقة جديدة لتوصيل دواء معروف جيداً، الكيتامين، مباشرة إلى الدماغ عبر الأنف باستخدام فقاعات صغيرة من الدهون والنشا. الهدف هو تعزيز الفائدة، تقليل الآثار الجانبية، ودعم قدرة الدماغ على التكيف والتعافي بعد الصدمة.
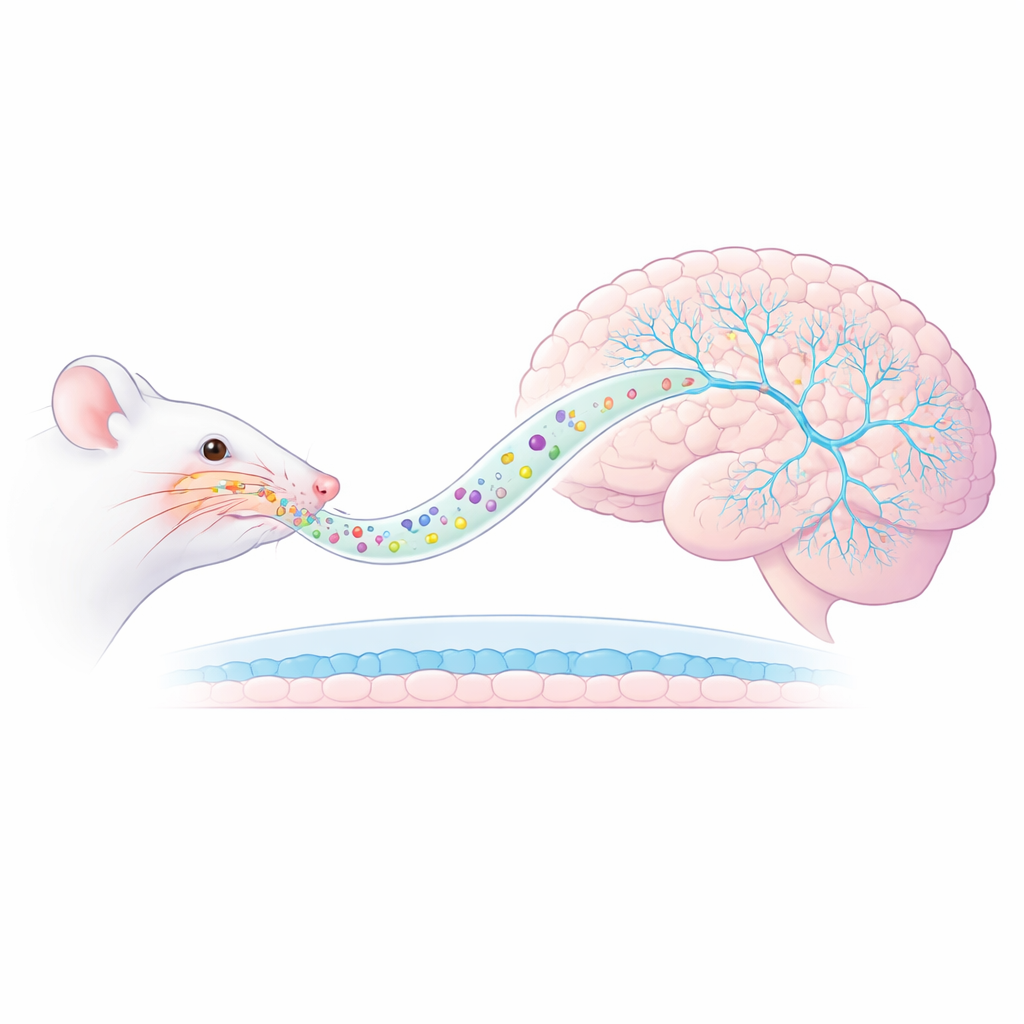
مسار جديد من الأنف إلى الدماغ
ركز الباحثون على نموذج فأر للاكتئاب التالي للصدمة حيث تتعرض الحيوانات لرائحة مفترس، ما يثير قلقاً طويل الأمد واستجابات مبالغ فيها لمثيرات تذكرها بالتهديد. بدلاً من إعطاء الكيتامين عن طريق الحقن، حزموه داخل حويصلات نانوية AmyloLipid—قطرات بحجم نانوي ذات قلب دهني مغلف بغلاف من النشا المعدّل. عند رشه في الأنف، صُممت هذه الجسيمات لتسير على طول المسارات العصبية مباشرة إلى الدماغ، متجاوزة الحاجز الدماغي الدموي الذي يحدّ عادةً من دخول الأدوية. أظهرت القياسات السابقة أن هذه الطريقة زادت بشكل كبير مستويات الكيتامين في نسيج الدماغ مع إبقاء مستويات الدم منخفضة، مما يوحي بتوصيل موجه أكثر واحتمال لآثار جانبية جهازية أقل.
اختبار التوتر والخوف ورد الفعل المفاجئ
بعد التعرض الصادم، تلقت الفئران علاجات داخل الأنف ثلاث مرات أسبوعياً لمدة أسبوعين: جرعات مختلفة من الحويصلات النانوية المحمّلة بالكيتامين، حويصلات نانوية فارغة، محلول كيتامين عادي، أو محلول ملحي. ثم قيّمت الفريق مدى قلق الحيوانات في متاهة مرتفعة، وشدة رد فعلها المفاجئ للأصوات العالية، ومقدار تجمّدها عند إعادة تعريضها لذكرى غير ضارة من رائحة المفترس. صنّفوا أيضاً الفئران إلى مجموعات أظهرت اضطراباً شديداً أو جزئياً أو ضئيلاً، محاكية كيف يختلف الناس في استجاباتهم للصدمة. تميز الكيتامين بجرعة منخفضة في الحويصلات النانوية—وخاصة 0.6 ملليغرام لكل كيلوغرام: فقد خفّض سلوكيات شبيهة بالقلق، وقلّل ردود الفعل المفاجئة المبالغ فيها، وخفّض نسبة الحيوانات ذات الاستجابات الشبيهة بـPTSD بحوالي النصف مقارنةً بمن أعطوا جسيمات فارغة. بالمقابل، زادت أعلى جرعة التجمّد والقلق، مما يؤكد أن المزيد من الدواء ليس دائماً أفضل.
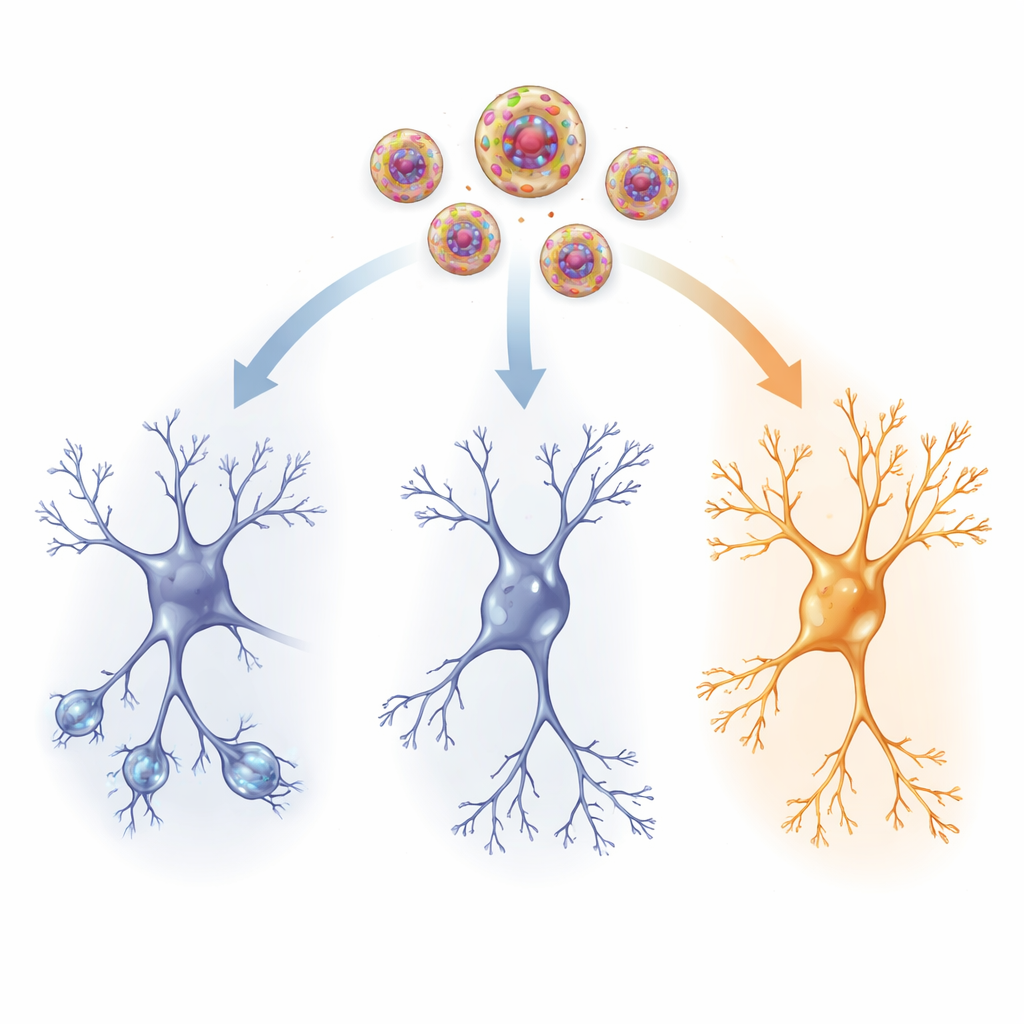
داخل توصيلات الدماغ
لمعرفة ما الذي تغيّر مادياً، فحص الباحثون منطقة ذاكرة رئيسية، الحُصين، ومركز تحكم بالتوتر، النواة فوق البُطينية داخل الوطاء. لدى الفئران المتعرضة للصدمة التي لم تتلقَ دواء فعال، كانت خلايا الحصين العصبية أقل تشعيعاً وأقصر فروعاً ومع وجود عدد أقل من الشوكات الصغيرة حيث تتكوّن المشابك—علامات على تضعف الاتصالات. كما انخفضت مستويات عامل التغذية العصبية المشتق من الدماغ (BDNF)، وببتيد عصبي Y (NPY) المرتبط بالمرونة تجاه التوتر. في الوقت نفسه، لوحظت زيادة في قنوات HCN1، بروتينات في غشاء الخلية تشكّل مدى سهولة استثارة الخلايا العصبية. مجتمعة، تشير هذه التغيرات إلى شبكة دماغية أقل مرونة وأقل استجابة بعد الصدمة.
استعادة التوازن في الخلايا العصبية
قلب الكيتامين بجرعة منخفضة الموصّل عبر الحويصلات النانوية العديد من علامات التلف هذه. استعادت الخلايا العصبية في الفئران المعالجة فروعاً أطول وأكثر تعقيداً ومزيداً من الشوكات، خصوصاً في الطبقة العلوية من الحصين حيث تصل المداخل البعيدة. صعدت مستويات BDNF وNPY نحو الطبيعي في كل من الحصين ومنطقة التحكم بالتوتر، ما يوحي بتجدد الدعم لبقاء الخلايا ونموها ومرونتها. في الوقت نفسه، هدأ الارتفاع غير الطبيعي في قنوات HCN1، مما ساعد على استعادة مستوى صحي من الاستجابة الكهربائية. انسجمت هذه التغيرات البنيوية والكيميائية مع التحسن السلوكي، ما يوحي بأن توصيل الكيتامين الموجه يساعد الدماغ المتأثر بالصدمة على إعادة توصيل نفسه بطريقة أكثر تكيفية.
لماذا الجرعة وطريقة التوصيل مهمتان
أبرزت المقارنة بين الكيتامين في الحويصلات النانوية ومحلول الكيتامين العادي أهمية طريقة وكمية الدواء المعطاة. عند الجرعات المنخفضة، تفوق نظام الأنف إلى الدماغ على الكيتامين المعتاد في تخفيف السلوكيات الشبيهة بالقلق وردود الفعل المفاجئة والتجمّد. ومع ذلك، عند أعلى جرعة، بدا أن الكيتامين في الحويصلات النانوية يفاقم استجابات التوتر، على الأرجح لأن كمية أكبر من الدواء تسربت إلى مجرى الدم، وتحولت إلى نواتج تفكك نشطة، ووصلت إلى الدماغ عبر طرق أقل توجيهاً. يشير هذا النمط إلى وجود "نقطة مثالية" ضيقة حيث يحقق التوصيل المباشر إلى الدماغ بجرعة منخفضة أقصى فائدة مع تقليل الآثار غير المرغوبة.
ماذا قد يعني هذا للرعاية المستقبلية
بعبارات بسيطة، تُظهر هذه الدراسة أن توجيه كميات صغيرة من الكيتامين بلطف من الأنف إلى الدماغ يمكن أن يجعل الحيوانات المتأثرة بالصدمة أكثر هدوءاً ومرونة، بينما يساعد خلايا دماغها على إعادة نمو الروابط واستعادة النشاط الصحي. رغم أن الدراسة أُجريت على الفئران، فهي تشير إلى استراتيجية لعلاج اضطراب ما بعد الصدمة تعتمد على ناقلات ذكية وجرعات مدروسة بدل الاعتماد فقط على زيادات كمية الدواء. عبر ضبط قنوات HCN1 وتعزيز جزيئات النمو والمرونة مثل BDNF وNPY، قد يوفر الكيتامين داخل الأنف في حويصلات AmyloLipid النانوية يوماً ما طريقة أكثر دقة وطويلة الأمد وأكثر أماناً لمساعدة الدماغ على التعافي من التوتر الشديد.
الاستشهاد: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
الكلمات المفتاحية: اضطراب ما بعد الصدمة, الكيتامين, التوصيل عبر الأنف, جسيمات نانوية, اللدونة العصبية