Clear Sky Science · sv
Effekt av subanestetisk ketamin levererad via AmyloLipid-nanovesikel (ALN)-baserat intranasalt system på biobeteendemässiga svar i en djurmodell för PTSD
Hjälpa hjärnan att läka efter trauma
Posttraumatiskt stressyndrom (PTSD) kan dröja kvar i åratal och lämna människor fast i cykler av rädsla, ångest och påträngande minnen. Många av dagens behandlingar hjälper endast delvis eller verkar mycket långsamt. Denna studie undersöker en ny väg att leverera ett välkänt läkemedel, ketamin, direkt till hjärnan via näsan med hjälp av mycket små fett- och stärkelseblåsor. Förhoppningen är att öka nyttan, minska biverkningar och bättre stödja hjärnans egen förmåga att anpassa sig och återhämta sig efter trauma.
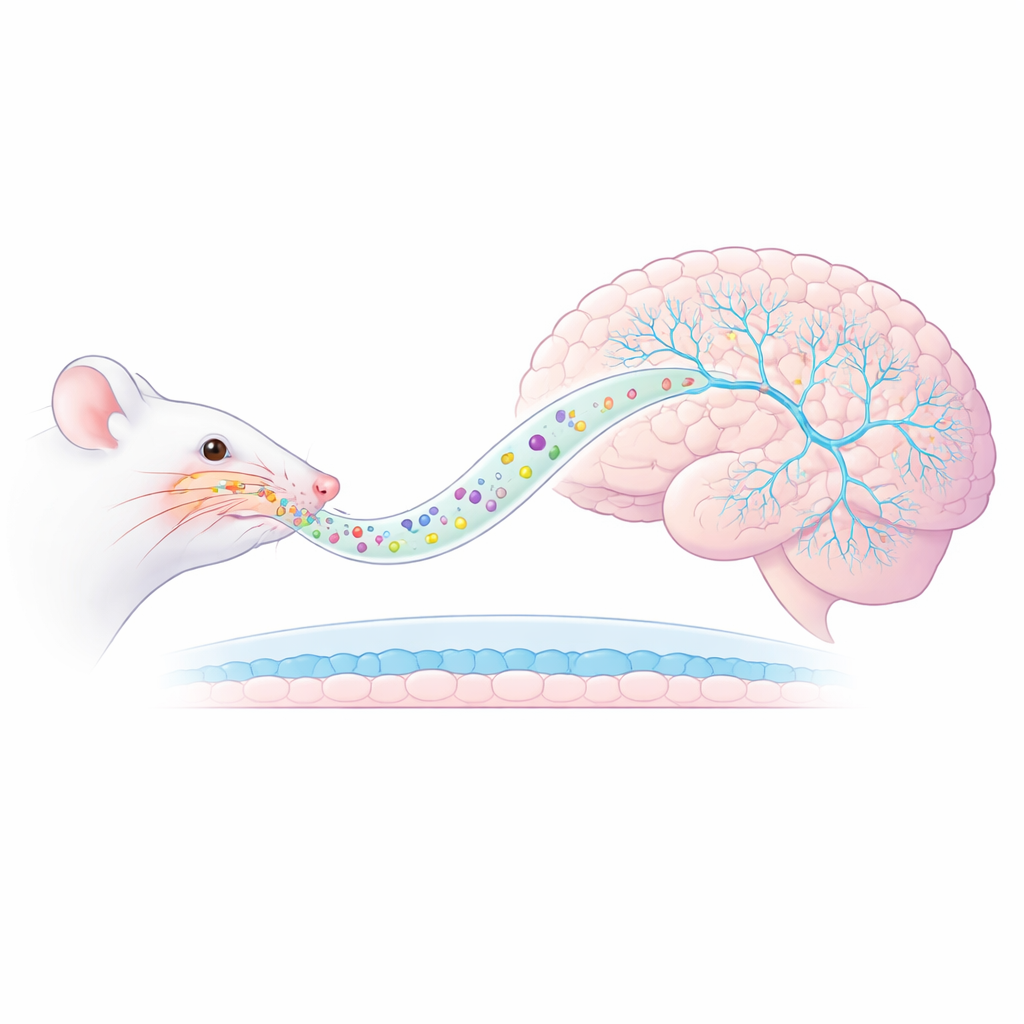
En ny näsa-till-hjärna-väg
Forskarlaget fokuserade på en råttmodell för PTSD där djuren exponeras för ett rovdjursspärr, vilket utlöser långvarig ångest och överdrivna reaktioner på påminnelser om hotet. Istället för att ge ketamin via injektion förpackade de det i AmyloLipid-nanovesiklar—nanometerstora droppar med en fet kärna omsluten av ett modifierat stärkelsehölje. När dessa partiklar sprayas in i näsan är de utformade för att färdas längs nervbanor direkt in i hjärnan och kringgå det vanliga blod-hjärnbarriären som begränsar läkemedelsintrång. Tidigare mätningar visade att detta tillvägagångssätt kraftigt ökade ketaminnivåerna i hjärnvävnad samtidigt som blodnivåerna hölls låga, vilket tyder på mer riktad leverans och potentiellt färre hela kroppens biverkningar.
Test av stress, rädsla och skräckstart
Efter den traumatiska exponeringen fick råttorna intranasala behandlingar tre gånger i veckan under två veckor: olika doser ketaminfyllda nanovesiklar, tomma nanovesiklar, vanlig ketaminlösning eller saltlösning. Forskarna mätte sedan hur ångestliknande djuren verkade i en upphöjd labyrint, hur kraftigt de ryckte till vid höga ljud och hur mycket de frös när de återexponerades för en ofarlig påminnelse om rovdjursspärren. De delade också in enskilda råttor i grupper som visade extrema, partiella eller minimala störningar, vilket efterliknar hur människor skiljer sig i sina reaktioner på trauma. Lågdos ketamin i nanovesiklar—särskilt 0,6 milligram per kilogram—framträdde: det minskade ångestliknande beteende, reducerade överdrivna skräckstartar och halverade andelen djur med starka PTSD-liknande reaktioner jämfört med de som fick tomma partiklar. I kontrast ökade den högsta dosen frysningar och ångest, vilket understryker att mer läkemedel inte alltid är bättre.
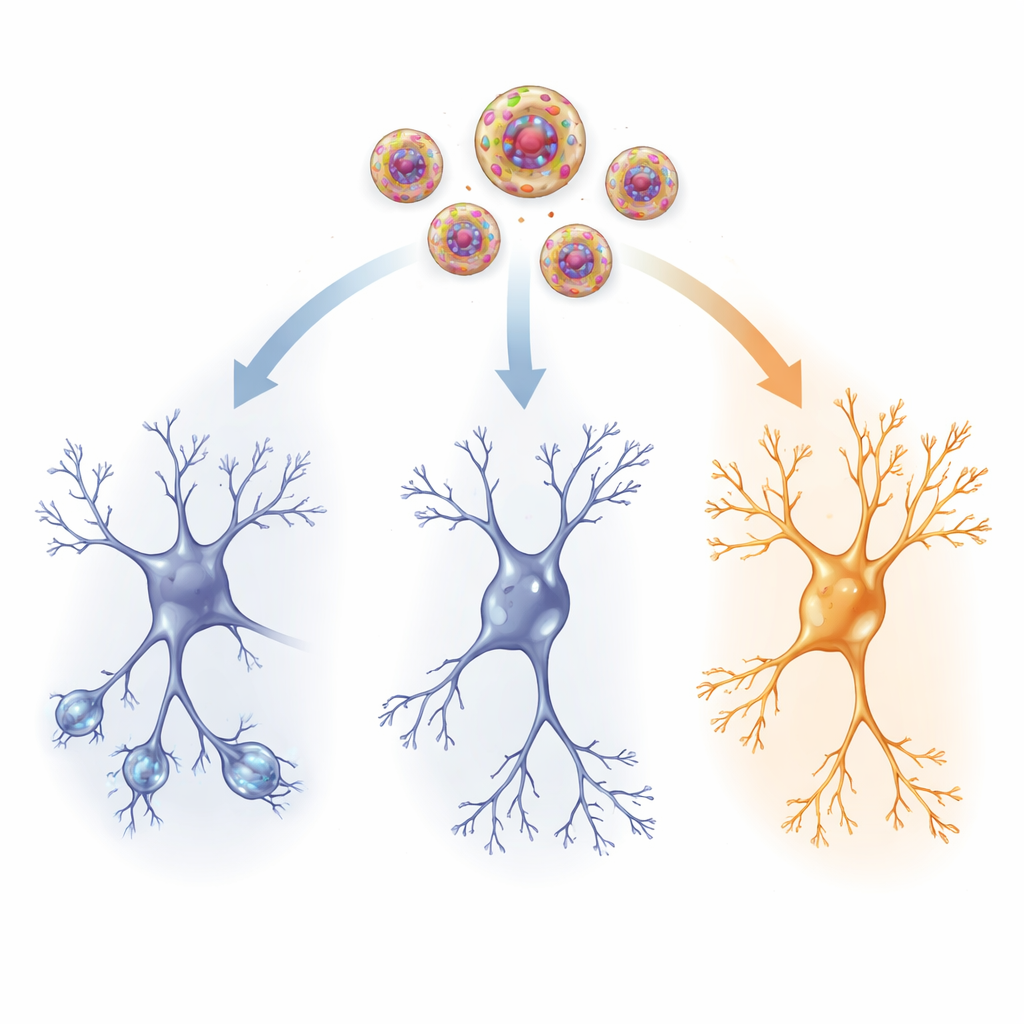
Inuti hjärnans kopplingar
För att se vad som förändrades fysiskt undersökte forskarna en nyckelregion för minne, hippocampus, och en stresskontrollerande nod, paraventrikulära kärnan i hypotalamus. Hos traumatiserade råttor som inte fick aktivt läkemedel hade hippocampala nervceller färre och kortare grenar och färre små spines där synapser bildas—tecken på försvagade förbindelser. Nivåerna av hjärnans härledda neurotrofiska faktor (BDNF), ett protein som stödjer tillväxt, och neuropeptid Y (NPY), en molekyl kopplad till stresstålighet, var också reducerade. Samtidigt noterades en ökning av HCN1-kanaler, proteiner i cellmembranet som påverkar hur lätt neuroner fyrar. Tillsammans pekar dessa skift mot ett hjärnnätverk som är mindre flexibelt och mindre mottagligt efter trauma.
Återställa balans i nervceller
Lågdos ketamin levererad via nanovesiklar vände många av dessa skadetecken. Neuroner hos behandlade råttor återfick längre och mer komplexa grenar samt fler spines, särskilt i det översta lagret av hippocampus där avlägsna indata når fram. BDNF- och NPY-nivåerna steg tillbaka mot normala värden både i hippocampus och i stresskontrollregionen, vilket tyder på förnyat stöd för cellöverlevnad, tillväxt och motståndskraft. Samtidigt avtog den onormala ökningen av HCN1-kanaler, vilket hjälpte till att återställa en hälsosam elektrisk responsförmåga. Dessa strukturella och kemiska förändringar matchade nära de beteendemässiga förbättringarna, vilket antyder att riktad ketaminleverans hjälper den traumatiserade hjärnan att omkoppla sig i en mer adaptiv riktning.
Varför dos och leverans spelar roll
Jämförelsen mellan nanovesikelbaserat ketamin och vanlig ketaminlösning betonade vikten av hur och hur mycket läkemedel som ges. Vid låga doser överträffade näsa-till-hjärna-systemet standardketamin när det gällde att lindra ångestliknande beteende, skräckstart och frysning. Vid den högsta dosen verkade dock ketamin i nanovesiklar förvärra stressreaktionerna, troligen eftersom mer läkemedel undslapp till blodomloppet, omvandlades till aktiva nedbrytningsprodukter och nådde hjärnan via mindre riktade vägar. Detta mönster tyder på att det finns ett smalt "sweet spot" där direkt hjärnleverans i låg dos maximerar gynnsamma effekter samtidigt som oönskade effekter minimeras.
Vad detta kan betyda för framtida vård
Enkelt uttryckt visar detta arbete att försiktig sändning av små mängder ketamin direkt från näsan till hjärnan kan göra traumatiserade djur lugnare och mer motståndskraftiga, samtidigt som deras hjärnceller hjälper till att återbygga förbindelser och återfå hälsosam aktivitet. Även om studien gjordes på råttor pekar den mot en strategi för behandling av PTSD som använder smarta bärare och noggrann dosering snarare än bara högre mängder läkemedel. Genom att finjustera HCN1-kanaler och öka nivåerna av tillväxt- och motståndskraftsmolekyler såsom BDNF och NPY kan intranasalt ketamin i AmyloLipid-nanovesiklar en dag erbjuda ett mer precist, mer långvarigt och säkrare sätt att hjälpa hjärnan att läka efter svår stress.
Citering: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Nyckelord: PTSD, ketamin, intranasal administrering, nanopartiklar, neuroplasticitet