Clear Sky Science · de
Auswirkungen subanästhetischer Ketaminverabreichung über ein AmyloLipid-Nanovesikel-(ALN)-basiertes intranasales System auf biobehaviorale Reaktionen in einem Tiermodell für PTBS
Dem Gehirn helfen, von Traumata zu heilen
Die posttraumatische Belastungsstörung (PTBS) kann über Jahre anhalten und Menschen in Kreisläufen aus Angst, Sorge und aufdringlichen Erinnerungen gefangen halten. Viele der derzeitigen Behandlungen wirken nur teilweise oder sehr langsam. Diese Studie untersucht einen neuen Weg, ein bekanntes Medikament, Ketamin, direkt durch die Nase zum Gehirn zu bringen—mithilfe winziger Fett‑und Stärkevesikel. Ziel ist es, den Nutzen zu erhöhen, Nebenwirkungen zu verringern und die Fähigkeit des Gehirns zur Anpassung und Erholung nach einem Trauma besser zu unterstützen.
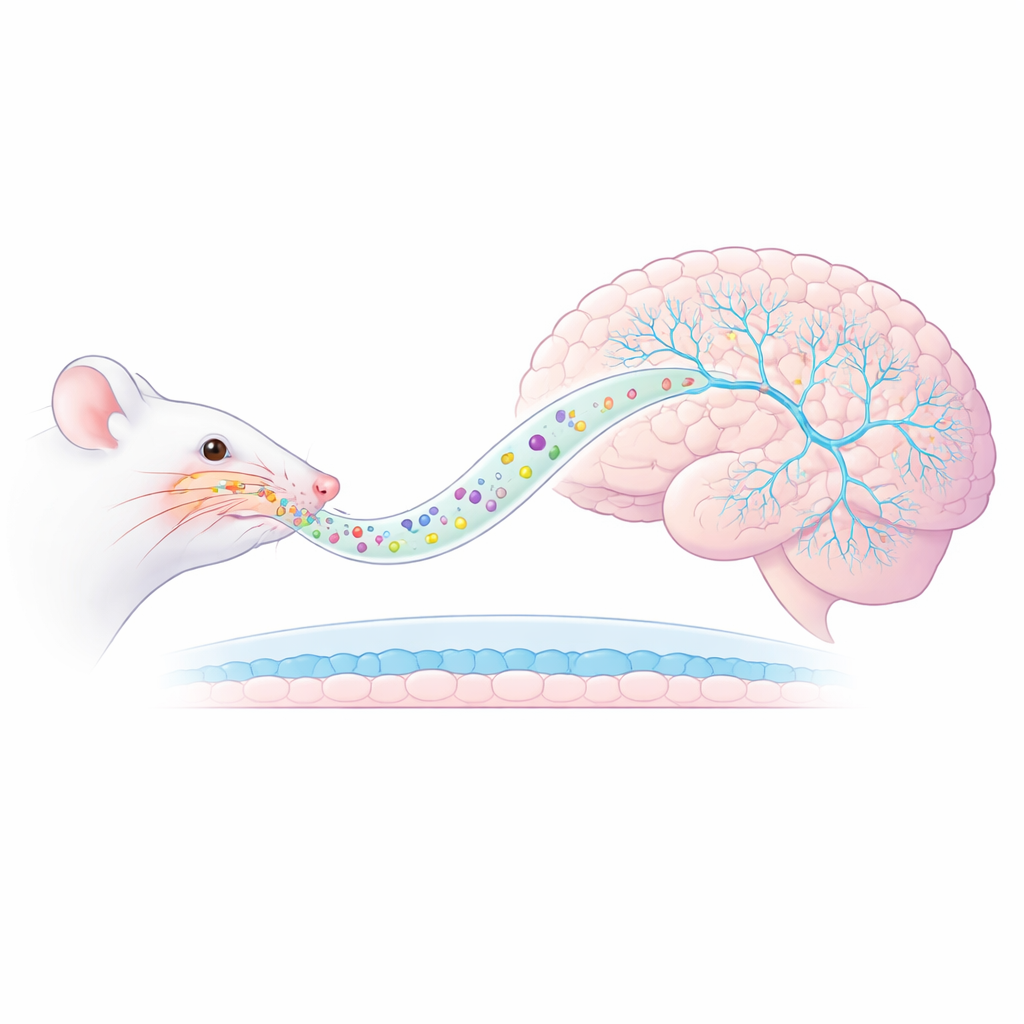
Ein neuer Weg von der Nase zum Gehirn
Die Forschenden konzentrierten sich auf ein Rattenmodell der PTBS, bei dem die Tiere einem Raubtiergeruch ausgesetzt werden, was langanhaltende Angst und übersteigerte Reaktionen auf Erinnerungssignale der Bedrohung auslöst. Anstatt Ketamin zu injizieren, verpackten sie es in AmyloLipid‑Nanovesikel—nanometergroße Tröpfchen mit einem fetthaltigen Kern, umhüllt von einer modifizierten Stärkeschale. Beim Einsprühen in die Nase sollen diese Partikel entlang von Nervenwegen direkt ins Gehirn gelangen und die übliche Blut-Hirn-Schranke umgehen, die den Wirkstoffeintritt einschränkt. Frühere Messungen zeigten, dass dieser Ansatz die Ketaminspiegel im Gehirngewebe deutlich erhöhte, während die Blutspiegel niedrig blieben, was auf gezieltere Verabreichung und potenziell weniger systemische Nebenwirkungen hindeutet.
Testen von Stress, Angst und Schreckreaktion
Nach der traumatischen Exposition erhielten die Ratten drei Mal pro Woche über zwei Wochen intranasale Behandlungen: verschiedene Dosen ketaminbeladener Nanovesikel, leere Nanovesikel, einfache Ketaminlösung oder Kochsalzlösung. Das Team erfasste anschließend, wie ängstlich sich die Tiere in einem erhöhten Labyrinth verhielten, wie stark sie bei lauten Geräuschen zusammenzuckten und wie sehr sie erstarrten, wenn sie einem harmlosen Erinnerungssignal des Raubtiergeruchs erneut ausgesetzt wurden. Außerdem teilten sie einzelne Tiere in Gruppen mit starken, teilweisen oder minimalen Störungen ein, um die individuelle Unterschiedlichkeit der Traumareaktionen beim Menschen nachzuahmen. Niedrig dosiertes Ketamin in Nanovesikeln—insbesondere 0,6 Milligramm pro Kilogramm—fiel besonders positiv auf: Es verringerte angstähnliches Verhalten, reduzierte übersteigerte Schreckreaktionen und halbierte ungefähr den Anteil der Tiere mit ausgeprägten PTBS‑ähnlichen Reaktionen im Vergleich zu denen, die leere Partikel erhielten. Im Gegensatz dazu steigerten die höchsten Dosen Erstarrung und Angst, was zeigt, dass mehr Wirkstoff nicht zwangsläufig besser ist.
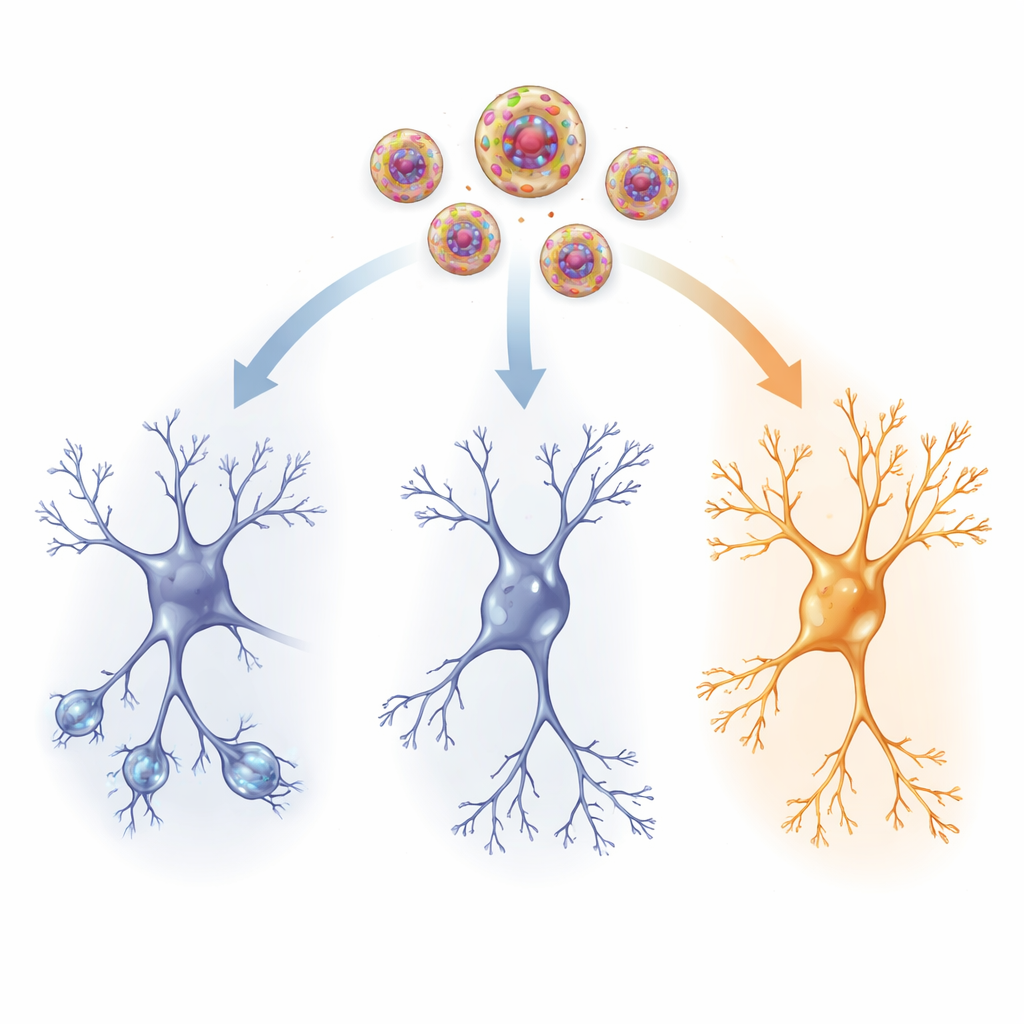
Im inneren Netzwerk des Gehirns
Um physische Veränderungen zu untersuchen, betrachteten die Forschenden eine Schlüsselregion für Gedächtnis, den Hippocampus, und einen Stress‑Kontrollknoten, den paraventrikulären Kern des Hypothalamus. Bei traumatisierten Ratten ohne aktive Behandlung zeigten hippocampale Nervenzellen weniger und kürzere Verzweigungen sowie weniger winzige Dornen, an denen Synapsen entstehen—Anzeichen geschwächter Verbindungen. Die Werte des brain-derived neurotrophic factor (BDNF), eines wachstumsfördernden Proteins, und des Neuropeptids Y (NPY), eines Moleküls, das mit Stressresilienz verknüpft ist, waren ebenfalls reduziert. Gleichzeitig nahm die Menge der HCN1‑Kanäle zu, Proteine in der Zellmembran, die beeinflussen, wie leicht Neuronen feuern. Zusammengenommen deuten diese Veränderungen auf ein weniger flexibles und weniger reaktionsfähiges Gehirnnetzwerk nach dem Trauma hin.
Wiederherstellung des Gleichgewichts in Nervenzellen
Niedrig dosiertes Ketamin, verabreicht über Nanovesikel, kehrte viele dieser Schädigungszeichen um. Die Neuronen der behandelten Ratten gewannen längere und komplexere Verzweigungen sowie mehr Dornen zurück, besonders in der obersten Schicht des Hippocampus, in die entfernte Eingänge einmünden. BDNF‑ und NPY‑Werte stiegen sowohl im Hippocampus als auch in der Stress‑Kontrollregion wieder in Richtung Normalwerte, was auf erneuerte Unterstützung für Überleben, Wachstum und Resilienz der Zellen hindeutet. Gleichzeitig ließ der abnorme Anstieg der HCN1‑Kanäle nach, was half, ein gesundes Maß elektrischer Erregbarkeit wiederherzustellen. Diese strukturellen und chemischen Veränderungen korrelierten eng mit den Verhaltensverbesserungen und legen nahe, dass zielgerichtete Ketaminverabreichung dem traumatisierten Gehirn hilft, sich adaptiver neu zu verdrahten.
Warum Dosis und Verabreichung wichtig sind
Der Vergleich von ketaminbeladenen Nanovesikeln mit gewöhnlicher Ketaminlösung machte deutlich, wie entscheidend Art und Menge der Gabe sind. Bei niedrigen Dosen übertraf das Nase‑zum‑Gehirn‑System die Standard‑Ketaminbehandlung in Bezug auf Linderung von angstähnlichem Verhalten, Schreckreaktion und Erstarrung. Bei der höchsten Dosis schien Ketamin in Nanovesikeln jedoch die Stressreaktionen zu verschlechtern, wahrscheinlich weil mehr Wirkstoff ins Blut gelangte, in aktive Abbauprodukte umgewandelt wurde und das Gehirn über weniger gezielte Wege erreichte. Dieses Muster legt nahe, dass es ein enges ‚Sweet Spot‘‑Fenster gibt, in dem direkte Gehirnverabreichung bei niedriger Dosis die hilfreichen Effekte maximiert und unerwünschte minimiert.
Was das für die künftige Versorgung bedeuten könnte
Einfach ausgedrückt zeigt diese Arbeit, dass das schonende Senden kleiner Ketaminmengen direkt von der Nase ins Gehirn traumatisierten Tieren Ruhe und Belastbarkeit verleihen kann und gleichzeitig das Nachwachsen von Verbindungen und die Wiederherstellung gesunder Aktivität ihrer Gehirnzellen unterstützt. Obwohl die Studie an Ratten durchgeführt wurde, weist sie auf eine Strategie zur Behandlung von PTBS hin, die auf intelligente Träger und sorgfältige Dosierung statt auf bloß höhere Wirkstoffmengen setzt. Indem HCN1‑Kanäle moduliert und wachstums‑ sowie resilienzfördernde Moleküle wie BDNF und NPY erhöht werden, könnte intranasales Ketamin in AmyloLipid‑Nanovesikeln eines Tages eine präzisere, länger wirksame und sicherere Möglichkeit bieten, dem Gehirn bei der Erholung von schweren Stressfolgen zu helfen.
Zitation: Levi, G., Sintov, A.C., Zohar, J. et al. Impact of subanesthetic ketamine delivered via AmyloLipid nanovesicle (ALN)-based intranasal system on biobehavioral responses in an animal model of PTSD. Transl Psychiatry 16, 230 (2026). https://doi.org/10.1038/s41398-026-03979-7
Schlüsselwörter: PTBS, Ketamin, intranasale Verabreichung, Nanopartikel, Neuroplastizität