Clear Sky Science · zh
mTOR驱动的富含整合素β4的外泌体来自雷替尼耐药的肝细胞癌,通过成纤维细胞利基形成助长肺转移
为何这项研究重要
肝癌是全球最致命的癌症之一,即便是强效的新药也常因肿瘤适应而失去疗效。本研究探讨了对雷替尼产生耐药的肝肿瘤如何反而更易发生肺转移。通过揭示这些耐药肿瘤向远处器官发送的隐秘“信息”,研究者找到了一个可被针对的薄弱环节,既可减缓转移,也有望恢复药物敏感性。
伴随危险后果的药物耐受
雷替尼是晚期肝癌的一线口服药,可通过切断血供和阻断生长信号发挥作用。然而许多患者初期有效,随后肿瘤通过旁路机制复发。在小鼠模型中,作者比较了原代肝癌细胞与获得雷替尼耐药的细胞变体。结果发现,耐药肿瘤不仅能在药物存在下存活,还生长更快并产生更多肺转移,缩短了生存期。这表明耐药并非仅是药效丧失,而是与肿瘤更具侵袭性并更易扩散的行为相关。
准备肺部的微小信使
为弄清耐药肿瘤如何获得这种转移优势,研究组聚焦于细胞外囊泡——细胞释放的携带蛋白等货物的微小囊泡并可通过血液循环远距传递。借助成像和颗粒追踪,他们显示出耐药肝癌细胞释放的囊泡远多于非耐药细胞,且这些囊泡在小鼠肺部的累积更为明显。当用耐药肿瘤来源的囊泡“预处理”健康小鼠后,随后注入肝癌细胞会产生更多的肺部肿瘤,证明这些囊泡能积极为癌细胞“种子”准备有利的“土壤”。 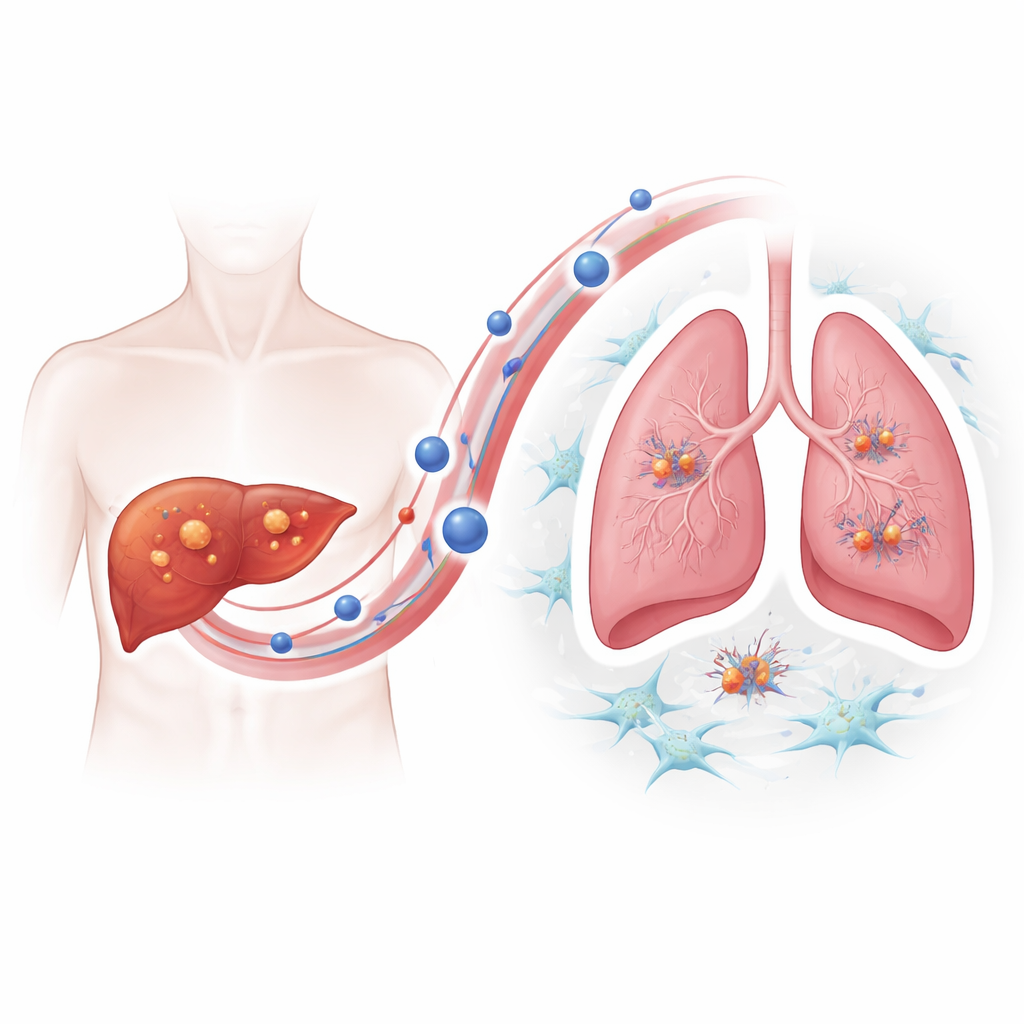
唤醒肺部“帮手”的分子握手
蛋白组学分析显示,耐药肿瘤来源的囊泡在表面富含一种名为整合素β4的蛋白。整合素有助于细胞附着到周围基质,此处囊泡表面的整合素β4像一种分子握手,与肺组织中的主要成分层粘连蛋白发生作用。囊泡被肺成纤维细胞——可重塑组织的支持细胞——最有效地摄取。成纤维细胞被这些囊泡激活后,呈现出更具肌肉样的收缩状态,并开始分泌炎性分子和生长因子。这一过程依赖于成纤维细胞内的PI3K–AKT–p65信号级联;阻断该级联的关键步骤可抑制成纤维细胞激活并减少其产生的促转移信号。缺乏整合素β4的囊泡在驱动肺定植方面基本失去能力。
促进囊泡释放的内在开关
为何耐药肿瘤细胞本身会大量释放囊泡?作者将其追溯到一个主控生长的调节因子mTOR的过度激活,mTOR也控制着被称为自噬的细胞回收系统。在耐药细胞中,活性的mTOR妨碍了多囊泡体(multivesicular bodies)的正常降解——这些细胞内隔室要么被分解,要么与细胞膜融合释放囊泡。当降解受阻时,这些隔室被引导走向分泌途径,从而大幅增加囊泡释放。用经典的mTOR抑制剂雷帕霉素处理耐药细胞可恢复这些隔室的自噬降解,减少囊泡释放,并降低剩余囊泡所携带的整合素β4水平。 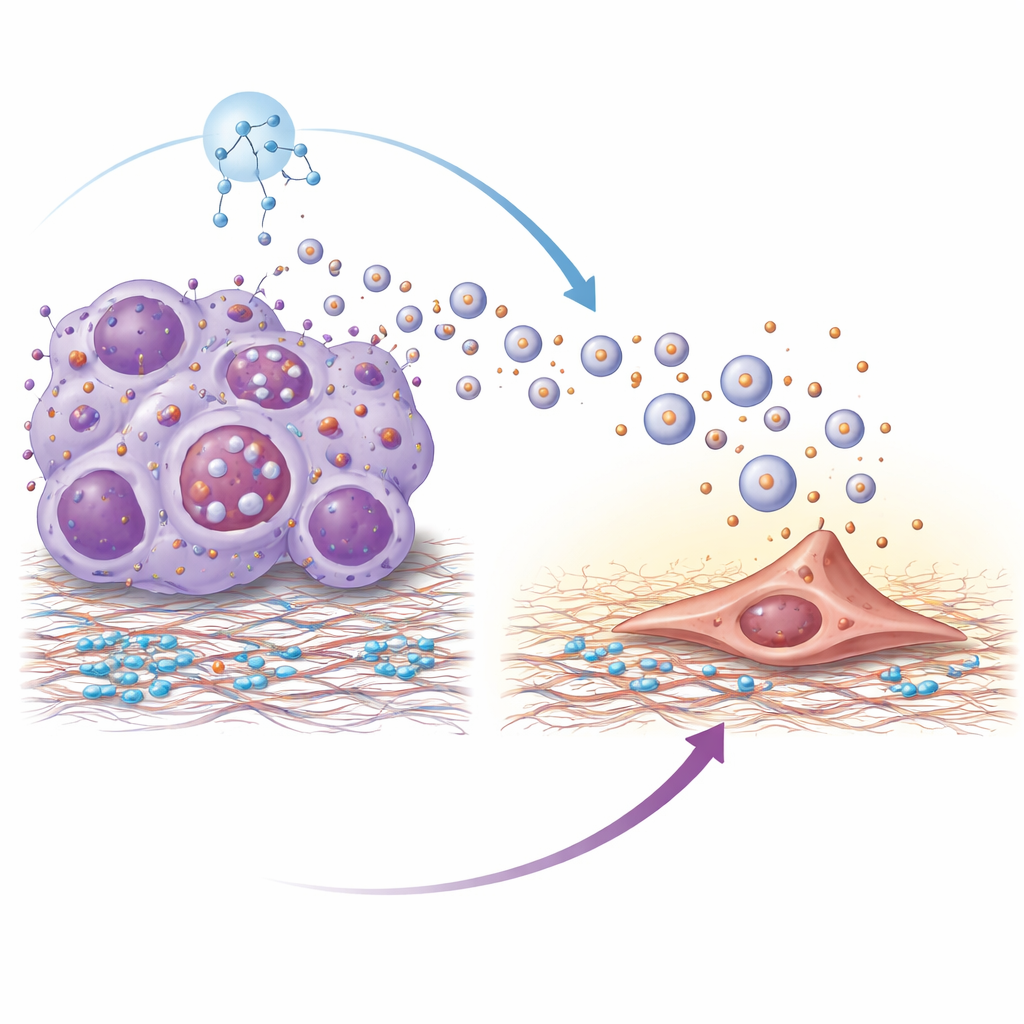
具有临床线索的联合策略
在小鼠中,将雷帕霉素与雷替尼联合使用比单用任一药物更能缩小耐药肿瘤、减少肺转移并延长生存期。来自雷帕霉素处理的耐药细胞的囊泡在激活肺成纤维细胞或促成肺前转移利基方面能力显著下降。在肝癌患者的血液样本中,循环囊泡上较高的整合素β4水平与雷替尼疗效不佳、肺转移更频繁及更差的生存相关,提示该标志物可用于识别有侵袭性转移风险的患者。
这对患者意味着什么
对非专业读者而言,这项工作表明耐药的肝肿瘤不仅仅是对治疗“视而不见”——它们还释放大量微小包裹,预先“软化”肺部,使局部支持细胞变为沉默的帮凶。通过识别mTOR作为提升这些危险信息的内部开关,以及整合素β4作为引导它们的关键地址标签,研究指向了两个可行的策略:在血液中测量囊泡的整合素β4水平作为早期预警信号,以及将mTOR抑制剂(如雷帕霉素)与雷替尼联合使用,以既恢复药物敏感性又遏制肺转移。
引用: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
关键词: 肝细胞癌, 药物耐受, 细胞外囊泡, 肺转移, mTOR 信号通路