Clear Sky Science · fr
Des vésicules extracellulaires enrichies en intégrine β4 et pilotées par mTOR, issues d’un carcinome hépatocellulaire résistant au lénvatinib, favorisent les métastases pulmonaires via la formation d’un niche fibroblastique
Pourquoi cette recherche importe
Le cancer du foie est l’un des cancers les plus mortels au monde, et même les nouveaux traitements puissants perdent souvent de leur efficacité à mesure que les tumeurs s’adaptent. Cette étude explore comment des tumeurs hépatiques devenues résistantes au lénvatinib peuvent en réalité acquérir une plus grande propension à se propager aux poumons. En dévoilant les « messages » cachés que ces tumeurs résistantes envoient aux organes distants, les chercheurs identifient une faiblesse exploitable pour à la fois ralentir les métastases et restaurer la sensibilité au médicament.
Résistance médicamenteuse avec un effet secondaire dangereux
Le lénvatinib est un traitement oral de première ligne pour les cancers hépatiques avancés qui agit en coupant l’approvisionnement sanguin et en bloquant des signaux de croissance. Pourtant, de nombreux patients répondent d’abord puis rechutent, la tumeur trouvant des moyens de contourner le blocage. Chez la souris, les auteurs ont comparé des cellules de carcinome hépatocellulaire d’origine et des versions ayant acquis une résistance au lénvatinib. Ils ont constaté que les tumeurs résistantes non seulement survivaient au traitement, mais croissaient plus rapidement et produisaient beaucoup plus de métastases pulmonaires, raccourcissant la survie. Cela suggère que la résistance s’accompagnait d’un comportement plus agressif et invasif, au‑delà d’une simple perte d’efficacité du médicament.
De minuscules messagers qui préparent les poumons
Pour comprendre comment les tumeurs résistantes gagnent cet avantage métastatique, l’équipe s’est intéressée aux vésicules extracellulaires — de petites bulles émises par les cellules qui transportent des protéines et d’autres cargaisons dans la circulation. Grâce à l’imagerie et au suivi des particules, ils ont montré que les cellules résistantes au lénvatinib libéraient sensiblement plus de ces vésicules que leurs homologues non résistantes, et que les vésicules s’accumulaient préférentiellement dans les poumons des souris. Lorsque des souris saines étaient « prétraitées » avec des vésicules issues de tumeurs résistantes, des injections ultérieures de cellules tumorales hépatiques donnaient lieu à beaucoup plus de tumeurs pulmonaires, démontrant que ces vésicules préparent activement un « sol » favorable pour les graines cancéreuses. 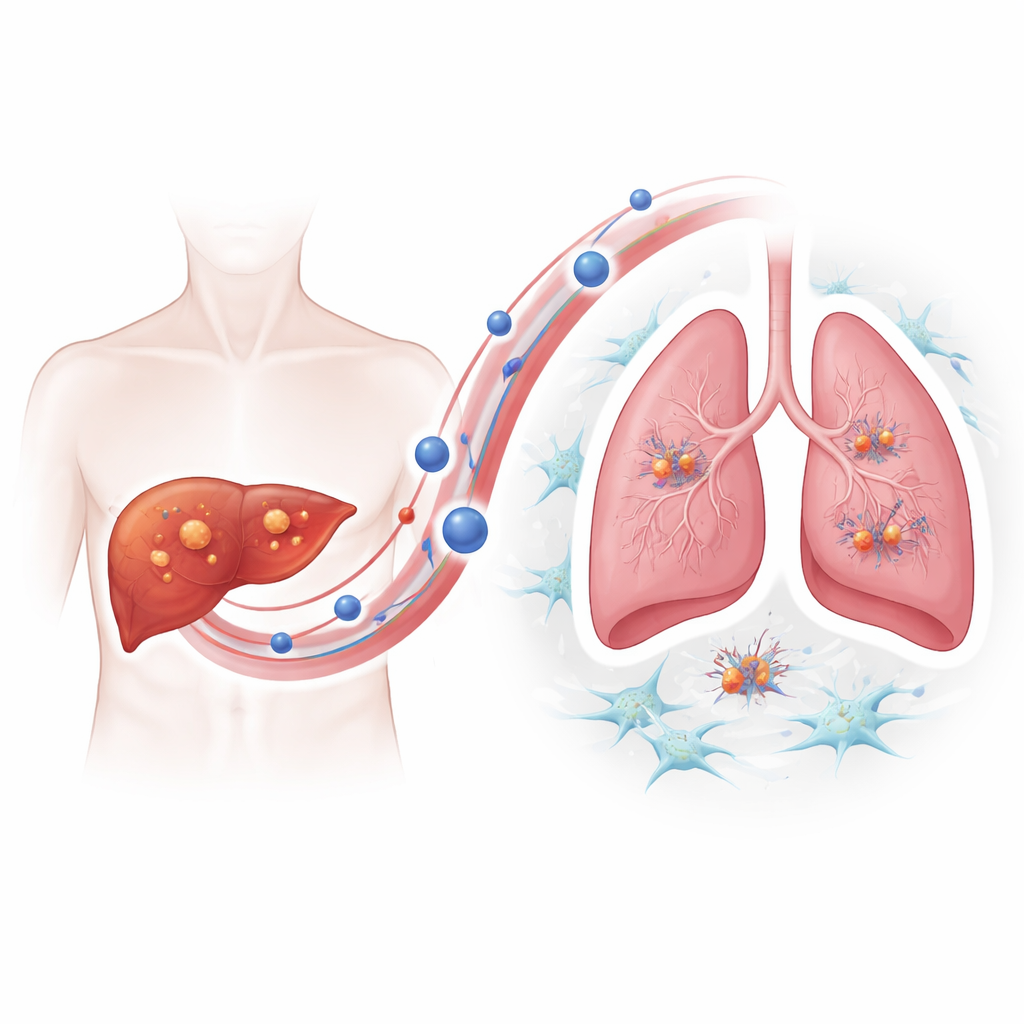
Une poignée de main moléculaire qui éveille les « aides » pulmonaires
Une analyse protéomique a révélé que les vésicules des tumeurs résistantes étaient enrichies en une protéine de surface appelée intégrine bêta‑4. Les intégrines aident les cellules à s’accrocher à leur environnement, et ici l’intégrine bêta‑4 portée par les vésicules jouait le rôle d’une « poignée de main » moléculaire avec la laminine, un composant majeur du tissu pulmonaire. Les vésicules étaient captées de façon préférentielle par les fibroblastes pulmonaires — des cellules de soutien capables de remodeler le tissu. Une fois activés par ces vésicules, les fibroblastes adoptaient un état plus musculaire et contractile et commençaient à sécréter des molécules inflammatoires et des facteurs de croissance. Ce processus dépendait d’une cascade de signalisation intracellulaire connue sous le nom de voie PI3K–AKT–p65 ; bloquer des étapes clé de cette voie atténuait l’activation des fibroblastes et réduisait les signaux pro‑métastatiques qu’ils produisaient. Les vésicules dépourvues d’intégrine bêta‑4 perdaient en grande partie leur capacité à favoriser la colonisation pulmonaire.
Un interrupteur interne qui augmente la libération de vésicules
Pourquoi les cellules tumorales résistantes libèrent‑elles autant de vésicules ? Les auteurs ont relié ce phénomène à l’hyperactivation d’un régulateur maître de la croissance appelé mTOR, qui contrôle aussi un système cellulaire de recyclage connu sous le nom d’autophagie. Dans les cellules résistantes, un mTOR actif perturbait la dégradation normale des corps multivésiculaires — des compartiments internes qui peuvent soit être dégradés, soit fusionner avec la membrane cellulaire pour libérer des vésicules. Lorsque la dégradation était bloquée, ces compartiments étaient détournés vers la sécrétion, augmentant fortement la production de vésicules. Le traitement des cellules résistantes par du rapamycine, un inhibiteur classique de mTOR, restaura la dégradation autophagique de ces compartiments, réduisit la libération de vésicules et diminua la quantité d’intégrine bêta‑4 portée par les vésicules restantes. 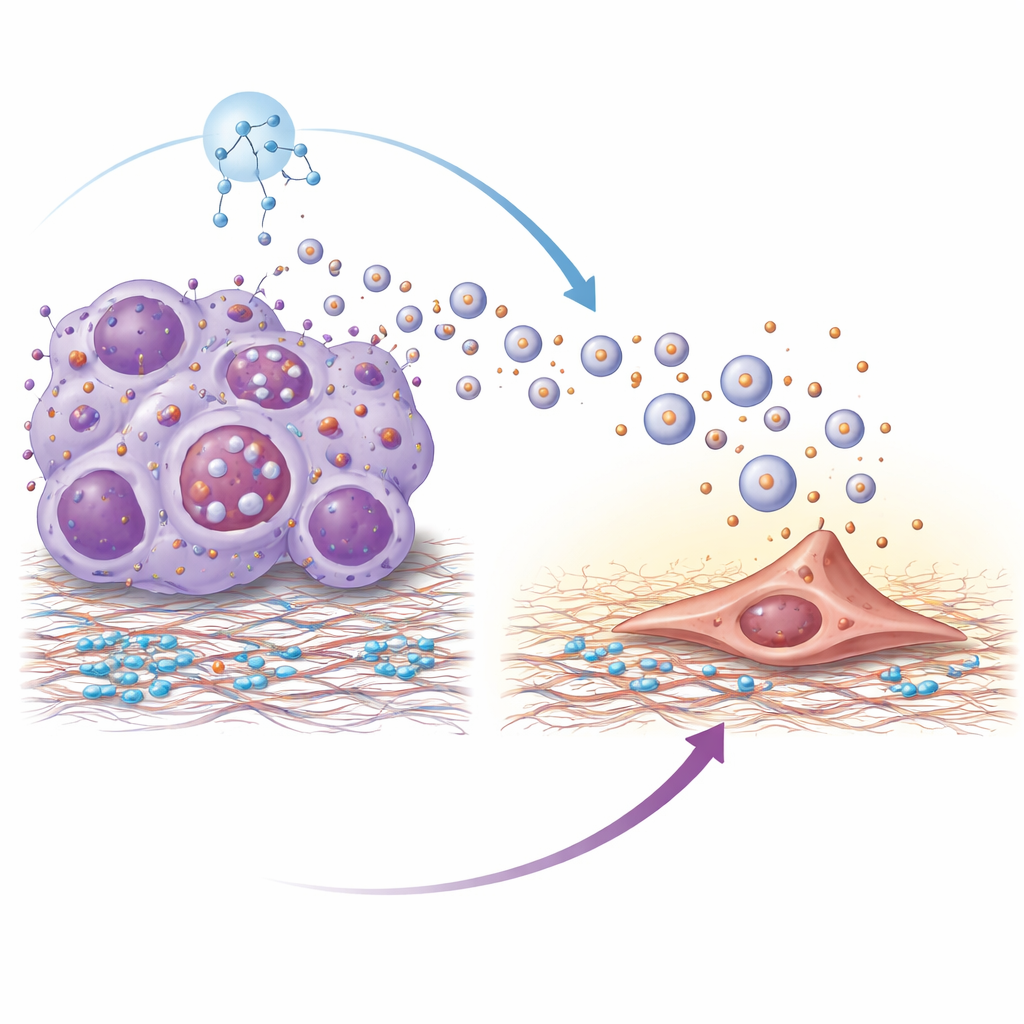
Une stratégie combinée avec des indices cliniques
Chez la souris, la combinaison de la rapamycine avec le lénvatinib réduisait plus efficacement les tumeurs résistantes, diminuait les métastases pulmonaires et prolongeait la survie par rapport à chaque médicament utilisé seul. Les vésicules issues de cellules résistantes traitées par rapamycine étaient beaucoup moins capables d’activer les fibroblastes pulmonaires ou de favoriser la formation d’une niche pulmonaire pré‑métastatique. Dans des échantillons sanguins de patients atteints de cancer du foie, des niveaux plus élevés d’intégrine bêta‑4 sur les vésicules circulantes étaient associés à une mauvaise réponse au lénvatinib, à une métastatisation pulmonaire plus fréquente et à une survie réduite, suggérant que ce marqueur pourrait aider à identifier les patients à risque de diffusion agressive.
Ce que cela signifie pour les patients
Pour un lecteur non spécialiste, ce travail montre que les tumeurs hépatiques résistantes ne se contentent pas d’ignorer le traitement — elles envoient des flottes de colis microscopiques qui « ramollissent » les poumons, transformant les cellules de soutien locales en complices silencieux. En identifiant mTOR comme l’interrupteur interne qui augmente ces messages dangereux, et l’intégrine bêta‑4 comme une étiquette d’adresse clé qui les guide, l’étude pointe vers deux opportunités pratiques : utiliser le niveau d’intégrine bêta‑4 sur les vésicules sanguines comme signal d’alerte précoce, et associer des médicaments bloquant mTOR comme la rapamycine au lénvatinib pour à la fois restaurer la sensibilité au traitement et freiner les métastases pulmonaires.
Citation: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Mots-clés: carcinome hépatocellulaire, résistance aux médicaments, vésicules extracellulaires, métastase pulmonaire, signalisation mTOR