Clear Sky Science · es
Vesículas extracelulares enriquecidas en integrina β4 impulsadas por mTOR procedentes de carcinoma hepatocelular resistente a lenvatinib fomentan la metástasis pulmonar mediante la formación de nichos fibroblásticos
Por qué importa esta investigación
El cáncer de hígado es uno de los más letales a nivel mundial, y aun los medicamentos más potentes suelen perder eficacia a medida que los tumores se adaptan. Este estudio explora cómo los tumores hepáticos que han desarrollado resistencia a lenvatinib pueden volverse, en realidad, más propensos a diseminarse al pulmón. Al descubrir los “mensajes” ocultos que estos tumores resistentes envían a órganos distantes, los investigadores identifican un punto débil que podría atacarse para frenar la metástasis y restaurar la sensibilidad al fármaco.
Resistencia a fármacos con un efecto secundario peligroso
Lenvatinib es un fármaco oral de primera línea para el cáncer hepático avanzado que actúa cortando el suministro sanguíneo y bloqueando señales de crecimiento. Sin embargo, muchos pacientes responden inicialmente y luego recaen cuando el tumor encuentra vías alternativas. En modelos murinos, los autores compararon células originales de cáncer de hígado con variantes que habían adquirido resistencia a lenvatinib. Encontraron que los tumores resistentes no solo sobrevivían al fármaco, sino que crecía n más rápido y producían muchas más metástasis pulmonares, acortando la supervivencia. Esto sugiere que la resistencia está ligada a un comportamiento más agresivo y diseminante, no solo a la pérdida de efecto del fármaco.
Mensajeros diminutos que preparan los pulmones
Para entender cómo los tumores resistentes adquieren esta ventaja metastásica, el equipo se centró en las vesículas extracelulares: burbujas diminutas desprendidas por las células que transportan proteínas y otros cargos por la sangre. Mediante imágenes y rastreo de partículas, mostraron que las células de carcinoma hepatocelular resistentes a lenvatinib liberaban significativamente más de estas vesículas que sus contrapartes no resistentes, y que las vesículas se acumulaban preferentemente en los pulmones de los ratones. Cuando ratones sanos fueron “pretratados” con vesículas procedentes de tumores resistentes, inyecciones posteriores de células hepáticas dieron lugar a muchas más lesiones pulmonares, demostrando que las vesículas preparan activamente un “suelo” favorable para las semillas cancerosas. 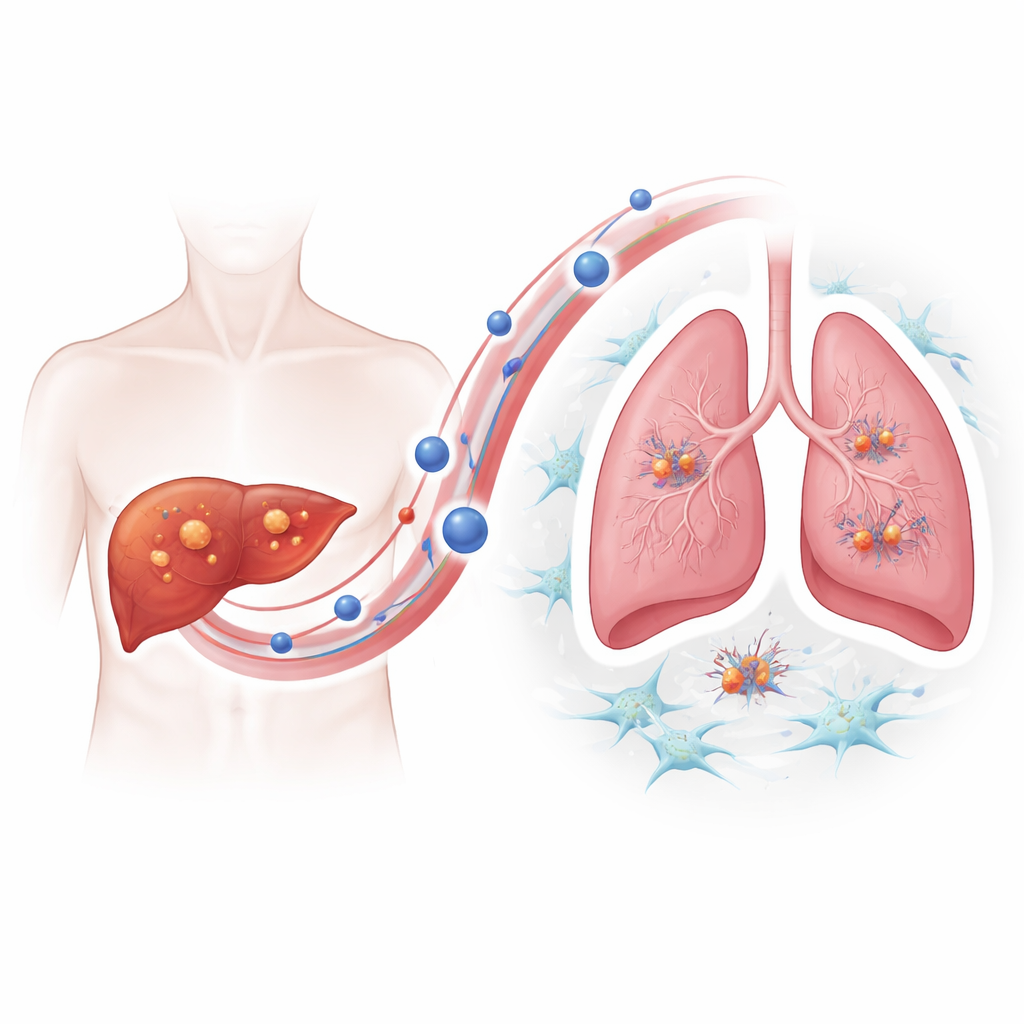
Un apretón molecular que despierta a los ayudantes pulmonares
El análisis proteómico reveló que las vesículas de tumores resistentes estaban enriquecidas en una proteína de superficie llamada integrina beta-4. Las integrinas ayudan a las células a anclarse a su entorno, y aquí la integrina beta-4 en las vesículas actuaba como un apretón de manos molecular con la laminina, un componente importante del tejido pulmonar. Las vesículas eran captadas con mayor eficiencia por fibroblastos pulmonares, células de soporte que pueden remodelar el tejido. Una vez activados por estas vesículas, los fibroblastos adquirieron un estado más muscular y contráctil y empezaron a secretar moléculas inflamatorias y factores de crecimiento. Este proceso dependía de una cascada de señalización intracelular en los fibroblastos conocida como la vía PI3K–AKT–p65; bloquear pasos clave en esa cascada atenuó la activación de los fibroblastos y redujo las señales pro-metastásicas que producían. Las vesículas que carecían de integrina beta-4 perdían en gran medida su capacidad de impulsar la colonización pulmonar.
Un interruptor interno que aumenta la liberación de vesículas
¿Por qué las células tumorales resistentes liberan tantas vesículas en primer lugar? Los autores lo atribuyeron a la hiperactivación de un regulador maestro del crecimiento llamado mTOR, que también controla un sistema celular de reciclaje conocido como autofagia. En las células resistentes, el mTOR activo impedía la degradación normal de los cuerpos multivesiculares, compartimentos internos que pueden ser degradados o fusionarse con la superficie celular para liberar vesículas. Cuando la degradación se bloqueaba, estos compartimentos se redirigían hacia la secreción, aumentando considerablemente la emisión de vesículas. Tratar las células resistentes con rapamicina, un inhibidor clásico de mTOR, restauró la degradación autofágica de estos compartimentos, redujo la liberación de vesículas y disminuyó la cantidad de integrina beta-4 transportada por las vesículas restantes. 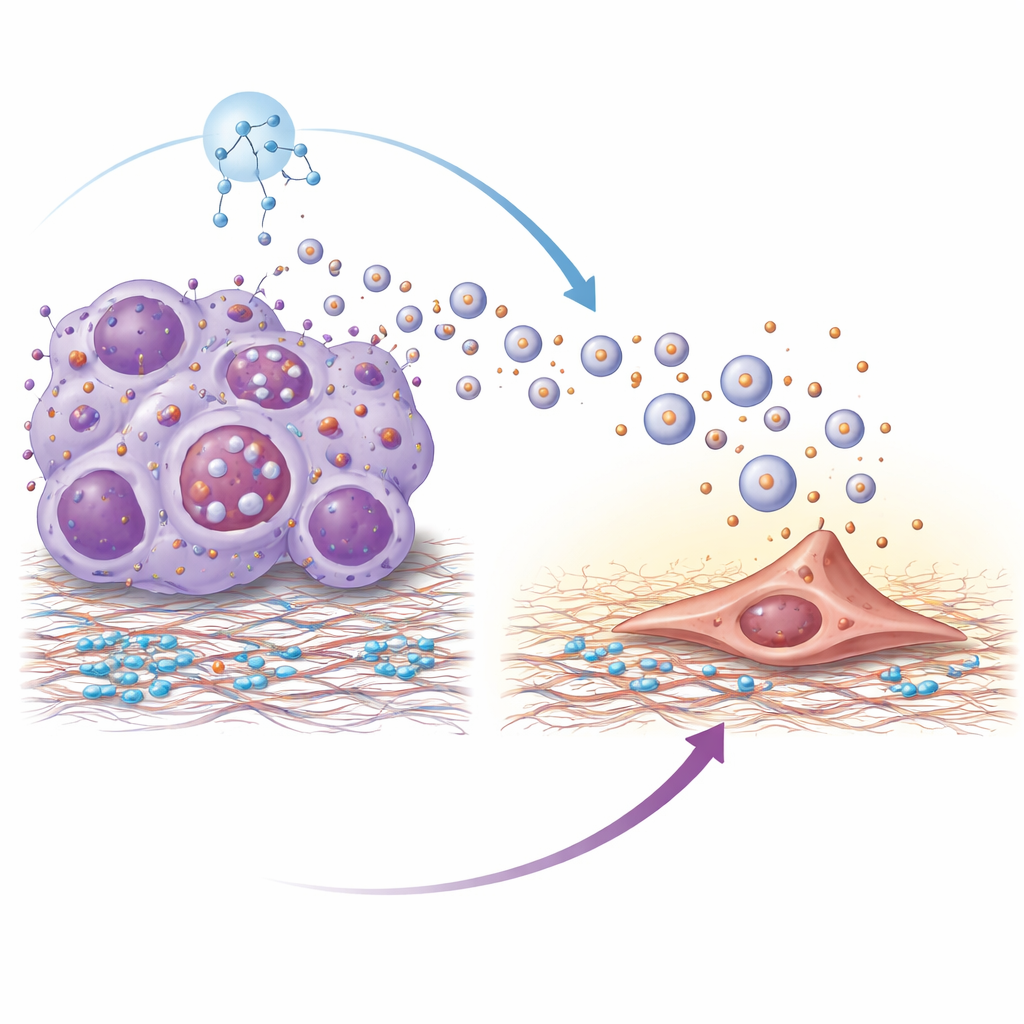
Una estrategia combinada con indicios clínicos
En ratones, combinar rapamicina con lenvatinib redujo los tumores resistentes de forma más eficaz, disminuyó las metástasis pulmonares y prolongó la supervivencia en comparación con cualquiera de los fármacos por separado. Las vesículas procedentes de células resistentes tratadas con rapamicina tenían mucha menor capacidad para activar fibroblastos pulmonares o favorecer un nicho pulmonar premetastásico. En muestras de sangre de pacientes con cáncer de hígado, niveles más altos de integrina beta-4 en vesículas circulantes se asociaron con mala respuesta a lenvatinib, mayor frecuencia de metástasis pulmonares y peor supervivencia, lo que sugiere que este marcador podría ayudar a identificar a pacientes en riesgo de diseminación agresiva.
Qué significa esto para los pacientes
Para un observador no especializado, este trabajo muestra que los tumores hepáticos resistentes a los fármacos hacen más que ignorar el tratamiento: envían flotas de paquetes microscópicos que “blandecen” los pulmones, convirtiendo a las células de soporte locales en cómplices silenciosos. Al identificar a mTOR como el interruptor interno que potencia estos mensajes peligrosos y a la integrina beta-4 como una etiqueta clave que los dirige, el estudio apunta a dos oportunidades prácticas: usar los niveles de integrina beta-4 en vesículas circulantes como señal temprana de alarma y combinar inhibidores de mTOR como la rapamicina con lenvatinib para restaurar la sensibilidad al fármaco y frenar la metástasis pulmonar.
Cita: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Palabras clave: carcinoma hepatocelular, resistencia a fármacos, vesículas extracelulares, metástasis pulmonar, señalización mTOR