Clear Sky Science · it
Vescicole extracellulari ricche di integrina β4 guidate da mTOR nei carcinomi epatocellulari resistenti a lenvatinib favoriscono metastasi polmonari tramite formazione di nicchia fibroblastica
Perché questa ricerca conta
Il tumore del fegato è uno dei più letali a livello globale e anche farmaci potenti spesso perdono efficacia man mano che i tumori si adattano. Questo studio esplora come i tumori epatici che hanno sviluppato resistenza al farmaco lenvatinib possano in realtà diventare più abili a diffondersi ai polmoni. Colonizzando i “messaggi” nascosti che questi tumori resistenti inviano a organi distanti, i ricercatori individuano un punto vulnerabile che potrebbe essere preso di mira per rallentare le metastasi e ripristinare la sensibilità al trattamento.
Resistenza farmacologica con un effetto collaterale pericoloso
Il lenvatinib è una terapia orale di prima linea per il carcinoma epatocellulare avanzato che agisce tagliando l’apporto di sangue e bloccando segnali di crescita. Tuttavia molti pazienti rispondono inizialmente solo per poi recidivare quando il tumore trova vie alternative per aggirare il blocco. In modelli murini, gli autori hanno confrontato cellule tumorali epatiche originali con varianti che avevano acquisito resistenza a lenvatinib. Hanno osservato che i tumori resistenti non solo sopravvivevano al farmaco, ma crescevano più rapidamente e producevano molte più metastasi polmonari, riducendo la sopravvivenza. Questo suggerisce che la resistenza fosse legata a un comportamento più aggressivo e migratorio, non solo a una perdita di sensibilità al farmaco.
Piccoli messaggeri che preparano i polmoni
Per capire come i tumori resistenti acquisissero questo vantaggio metastatico, il gruppo si è concentrato sulle vescicole extracellulari — piccole bolle rilasciate dalle cellule che trasportano proteine e altri carichi nel flusso sanguigno. Mediante imaging e tracciamento delle particelle, hanno mostrato che le cellule di carcinoma epatocellulare resistenti a lenvatinib rilasciavano in modo significativamente maggiore queste vescicole rispetto alle controparti non resistenti, e che le vescicole si accumulavano preferenzialmente nei polmoni dei topi. Quando topi sani venivano “pretrattati” con vescicole provenienti da tumori resistenti, successivi inoculi di cellule tumorali epatiche generavano molte più lesioni polmonari, dimostrando che le vescicole preparano attivamente un “terreno” favorevole per i semi tumorali. 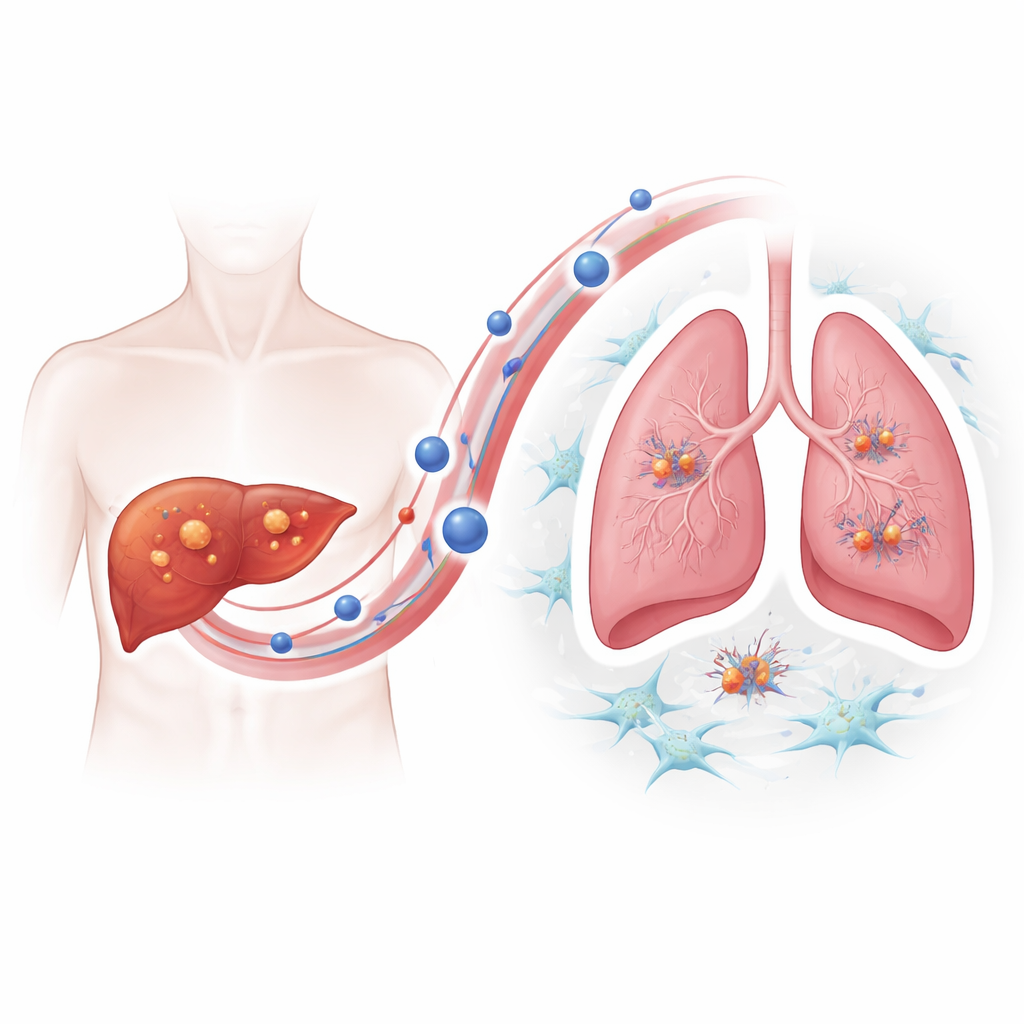
Una stretta di mano molecolare che risveglia i “collaboratori” polmonari
L’analisi proteomica ha rivelato che le vescicole dei tumori resistenti erano arricchite di una proteina di superficie chiamata integrina beta-4. Le integrine aiutano le cellule ad ancorarsi all’ambiente circostante e qui l’integrina beta-4 sulle vescicole agiva come una stretta di mano molecolare con la laminina, un componente principale del tessuto polmonare. Le vescicole venivano assorbite con maggiore efficienza dai fibroblasti polmonari — cellule di supporto in grado di rimodellare il tessuto. Una volta attivati da queste vescicole, i fibroblasti assumevano uno stato più muscolare e contrattil e cominciavano a secernere molecole infiammatorie e fattori di crescita. Questo processo dipendeva da una cascata di segnalazione intracellulare nei fibroblasti nota come via PI3K–AKT–p65; bloccare passaggi chiave di questa via attenuava l’attivazione dei fibroblasti e riduceva i segnali pro‑metastatici prodotti. Le vescicole prive di integrina beta-4 perdevano in gran parte la capacità di promuovere la colonizzazione polmonare.
Un interruttore interno che aumenta il rilascio di vescicole
Perché le cellule tumorali resistenti rilasciano così tante vescicole? Gli autori hanno ricondotto il fenomeno all’iperattivazione di un regolatore principale della crescita chiamato mTOR, che controlla anche un sistema cellulare di riciclo noto come autofagia. Nelle cellule resistenti, mTOR attivo comprometteva la normale degradazione dei corpi multivescicolari — compartimenti intracellulari che possono essere degradati o fondersi con la membrana cellulare per rilasciare vescicole. Quando la degradazione era inibita, questi compartimenti venivano deviati verso la secrezione, aumentando notevolmente la produzione di vescicole. Il trattamento delle cellule resistenti con rapamicina, un inibitore classico di mTOR, ripristinava la degradazione autofagica di questi compartimenti, riduceva il rilascio di vescicole e diminuiva la quantità di integrina beta-4 trasportata dalle vescicole rimaste. 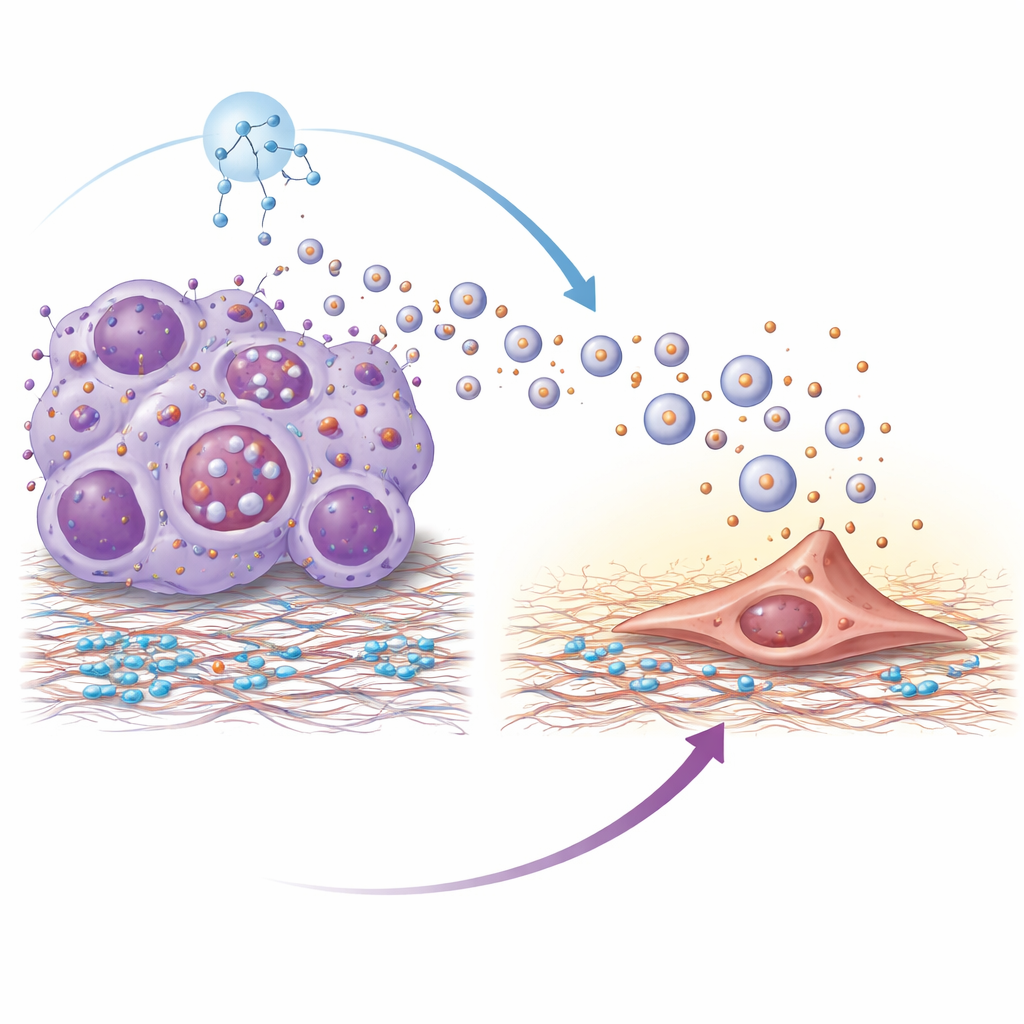
Una strategia combinata con indizi clinici
Nei topi, la combinazione di rapamicina con lenvatinib ridusse i tumori resistenti in modo più efficace, diminuì le metastasi polmonari e prolungò la sopravvivenza rispetto a ciascun farmaco da solo. Le vescicole provenienti da cellule resistenti trattate con rapamicina erano molto meno capaci di attivare i fibroblasti polmonari o di favorire la formazione di una nicchia pre‑metastatica. In campioni di sangue di pazienti con carcinoma epatocellulare, livelli più elevati di integrina beta‑4 sulle vescicole circolanti erano associati a scarsa risposta a lenvatinib, maggiore incidenza di metastasi polmonari e peggiore sopravvivenza, suggerendo che questo marcatore potrebbe aiutare a identificare i pazienti a rischio di diffusione aggressiva.
Cosa significa per i pazienti
Per un osservatore non specialista, questo lavoro mostra che i tumori epatici resistenti ai farmaci fanno più che ignorare il trattamento: inviano flotte di pacchetti microscopici che “ammorbidiscono” i polmoni, trasformando le cellule di supporto locali in complici silenziosi. Identificando mTOR come l’interruttore interno che amplifica questi messaggi pericolosi e integrina beta‑4 come un’etichetta che ne guida la destinazione, lo studio indica due opportunità pratiche: usare i livelli di integrina beta‑4 sulle vescicole nel sangue come segnale di allarme precoce e combinare farmaci inibitori di mTOR come la rapamicina con il lenvatinib per ripristinare la sensibilità al trattamento e contenere le metastasi polmonari.
Citazione: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Parole chiave: carcinoma epatocellulare, resistenza ai farmaci, vescicole extracellulari, metastasi polmonare, segnalazione mTOR