Clear Sky Science · he
אקסוזומים עשירים ב-integrin β4 מונעים על ידי mTOR מגידולי כבד עמידים ללנבנטיניב ומזינים גרורות ריאתיות דרך יצירת נישה של פיברובלסטים
מדוע מחקר זה חשוב
סרטן הכבד הוא אחד הסרטנים הקטלניים ביותר בעולם, ואף תרופות חזקות חדשות מאבדות לעיתים את יעילותן כשהגידול מסתגל. המחקר הזה בוחן כיצד גידולי כבד שפתחו עמידות ללנבנטיניב עשויים להפוך ליעילים יותר בהפצת גרורות לריאות. על ידי גילוי ה"הודעות" הסמויות ששלחו גידולים עמידים לאיברים מרוחקים, החוקרים מזהים נקודת תורפה שניתן למקד בה כדי להאט את הגרורתיות ולשחזר רגישות לתרופה.
עמידות לתרופה עם תופעת לוואי מסוכנת
לנבנטיניב היא תרופה פומית קו ראשון לסרטן כבד מתקדם שפועלת על ידי חסימת אספקת דם וחסימת אותות גדילה. עם זאת, בחולים רבים יש תגובה ראשונית אך לאחר מכן כשלון טיפולי כשהגידול מוצא דרכים לעקוף את החסימה. במודלים עכבריים השוו המחברים תאי סרטן כבד מקוריים עם וריאנטים שרכשו עמידות ללנבנטיניב. הם מצאו כי הגידולים העמידים לא רק שרדו את הטיפול אלא גם גדלו מהר יותר ויצרו הרבה יותר גרורות ריאתיות, מה שקיצר את ההישרדות. ממצא זה מצביע על כך שהעמידות קשורה להתנהגות תוקפנית ומפושטת יותר ולא רק לאיבוד השפעת התרופה.
שליחים זעירים שמכינים את הריאות
כדי להבין כיצד גידולים עמידים צוברים יתרון גרורתי, הקבוצה התמקדה בוזיקולות חוץ-תאיות — בועיות זעירות שנזרקות על ידי תאים ונושאות חלבונים ומטען אחר במחזור הדם. באמצעות הדמיה ומעקב חלקיקים הראו החוקרים שתאי סרטן כבד עמידים ללנבנטיניב שחררו במידה משמעותית יותר מהוזיקולות האלה בהשוואה לתאים לא עמידים, וכי הוזיקולות הצטברו באופן ממוקד יותר בריאות של עכברים. כאשר עכברים בריאים נותחו מראש עם ווזיקולות מהגידולים העמידים, הזרקות מאוחרות של תאי סרטן כבד יצרו עוד הרבה יותר גידולים ריאתיים, מה שהוכיח כי הוזיקולות מכינות באופן פעיל "קרקע" מזמינה לזרעים של סרטן. 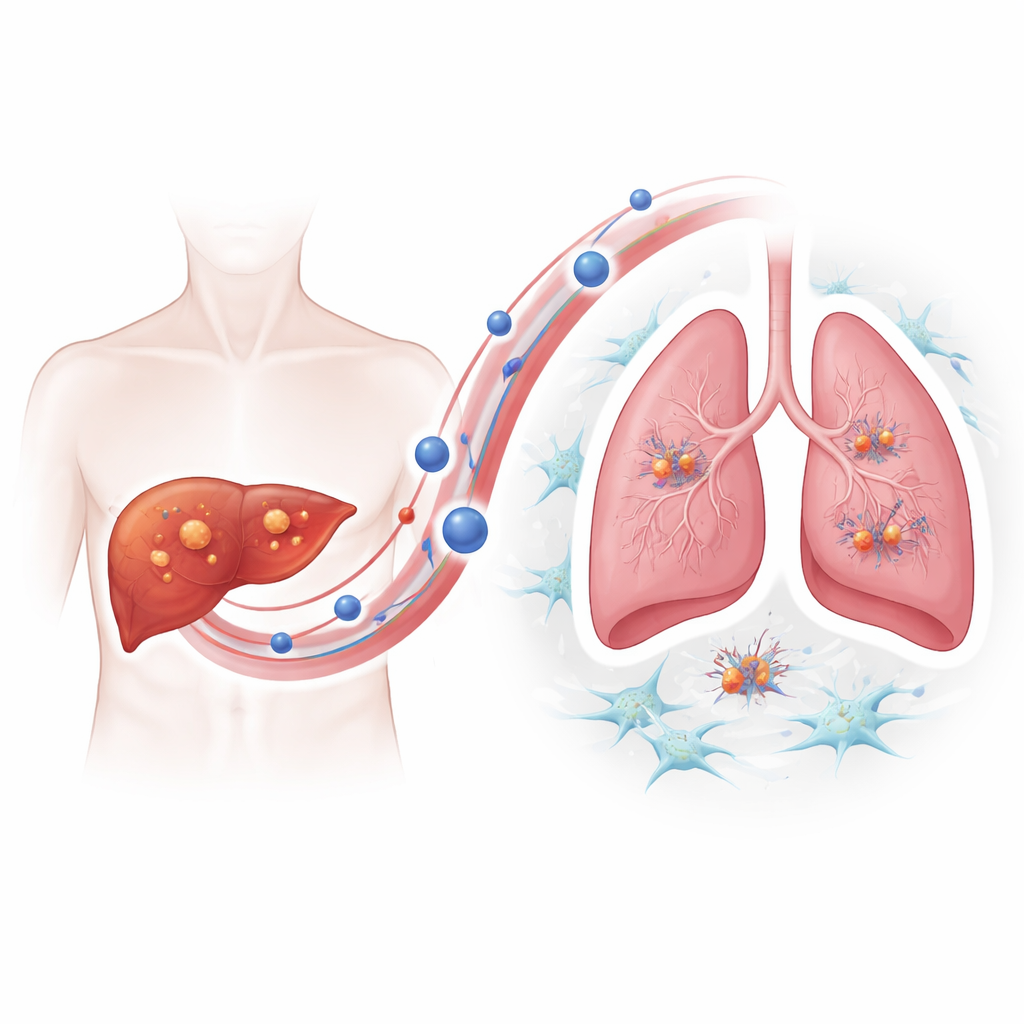
לחיצה מולקולרית שמעירה את המסייעים בריאות
ניתוח חלבומתי חשף כי הוזיקולות מהגידולים העמידים היו מועשרות בחלבון ממברנלי בשם integrin beta-4. אינטגרינים עוזרים לתאים להיצמד לסביבתם, וכאן integrin beta-4 על הוזיקולות פעל כמו לחיצת יד מולקולרית עם למינין, רכיב מרכזי ברקמת הריאה. הוזיקולות נקלטו ביעילות המרבית על ידי פיברובלסטים ריאתיים — תאי תמך שיכולים לעצב מחדש את המטריצה. לאחר הפעלה על ידי הוזיקולות, הפיברובלסטים נטו למצב שרירי-יותר, מתכווץ, והחלו להפריש מולקולות דלקתיות וגורמי גדילה. תהליך זה נשלט על ידי מסלול איתות בתוך הפיברובלסטים הידוע כ-PI3K–AKT–p65; חסימת צעדים מרכזיים בשרשרת זו דיכאה את הפעלת הפיברובלסטים והפחיתה את האותות הפרו-גרורתיים שהם ייצרו. ווזיקולות שחסרות integrin beta-4 איבדו ברובן את היכולת לקדם קולוניזציה ריאתית.
מתג פנימי שמגביר שחרור ווזיקולות
מדוע תאי גידול עמידים משחררים כל כך הרבה ווזיקולות מלכתחילה? המחברים עקבו והצביעו על היפראקטיבציה של מפעיל גדילה מרכזי בשם mTOR, אשר גם מבקר מערכת מחזור תאים שנקראת אוטופגיה. בתאים עמידים, mTOR פעיל פגע בפירוק התקין של גופים רב-בועתיים — קומפטמנטים פנימיים שיכולים либо להפורק או להיתמזג עם הממברנה התאית כדי לשחרר ווזיקולות. כאשר הפירוק נחסם, קומרטמנטים אלה נסללו לעבר הפרשה, מה שהגביר מאוד את יציאת הווזיקולות. טיפול בתאים עמידים ברפאמיצין, מדכא mTOR קלאסי, השיב את פירוק האוטופגי של הקומפטמנטים הללו, הקטין את שחרור הווזיקולות והפחית את כמות ה-integrin beta-4 הנישאת על הווזיקולות שנותרו. 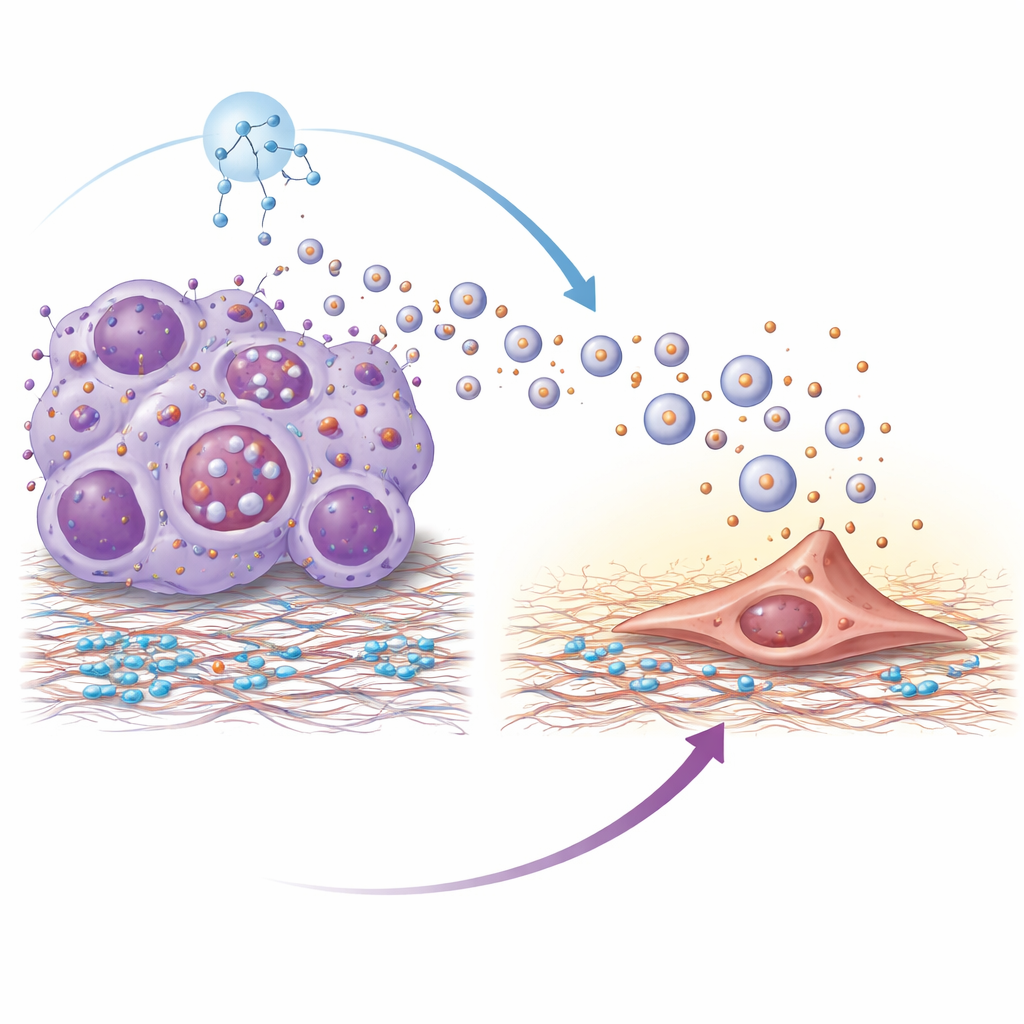
אסטרטגיית שילוב עם רמזים קליניים
בעכברים, שילוב רפאמיצין עם לנבנטיניב כיווץ גידולים עמידים ביעילות רבה יותר, הפחית גרורות ריאתיות והאריך הישרדות בהשוואה לכל תרופה בנפרד. ווזיקולות מתאי עמידים שטופלו ברפאמיצין היו הרבה פחות מסוגלות להפעיל פיברובלסטים ריאתיים או לטפח נישה ריאתית פרה-גרורתית. בדגימות דם של חולי סרטן כבד, רמות גבוהות יותר של integrin beta-4 על ווזיקולות במחזור נקשרו לתגובה גרועה ללנבנטיניב, לשכיחות גבוהה יותר של גרורות לריאות ולתוחלת הישרדות פחותה, מה שמציע שסמן זה עשוי לסייע בסינון חולים בסיכון להפצה תוקפנית.
מה המשמעות עבור המטופלים
לצופה שאינו מומחה, עבודה זו מראה כי גידולים עמידים לכאורה לא רק מתעלמים מהטיפול — הם שולחים צי של חבילות מיקרוסקופיות שמ"מרככות" את הריאות, והופכות תאי תמך מקומיים לשותפים שותקים. על ידי זיהוי mTOR כמפסק פנימי שמגביר את ההודעות המסוכנות האלה, ו-integrin beta-4 ככתובת מרכזית שמנחה אותן, המחקר מצביע על שתי הזדמנויות מעשיות: שימוש ברמות integrin beta-4 בווזיקולות בדם כאיתות מוקדם, ושילוב מעכבי mTOR כמו רפאמיצין עם לנבנטיניב כדי לשחזר רגישות לתרופה ולהקטין גרורות ריאתיות.
ציטוט: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
מילות מפתח: סרטן כבד תאי (הפטוצלולר), עמידות לתרופות, וזיקולות חוץ-תאיות, גרורות לריאות, תמסורת אותות mTOR