Clear Sky Science · nl
mTOR-gedreven integrine β4-verrijkte extracellulaire blaasjes van lenvatinib-resistente hepatocellulair carcinoom voeden longmetastasen via fibroblast-nichevorming
Waarom dit onderzoek ertoe doet
Baarmoederkanker van de lever is een van de dodelijkste vormen van kanker wereldwijd, en zelfs krachtige nieuwe geneesmiddelen verliezen vaak hun effect wanneer tumoren zich aanpassen. Deze studie onderzoekt hoe levertumoren die resistent zijn geworden tegen het middel lenvatinib juist beter kunnen worden in het uitzaaien naar de longen. Door de verborgen “berichten” te onthullen die deze resistente tumoren naar verre organen sturen, identificeren de onderzoekers een kwetsbaar punt dat kan worden aangegrepen om zowel metastasering te vertragen als de gevoeligheid voor medicatie te herstellen.
Medicatie-resistentie met een gevaarlijke bijwerking
Lenvatinib is een eerstelijnstablet voor gevorderde leverkanker dat werkt door de bloedtoevoer af te snijden en groeisignalen te blokkeren. Toch reageren veel patiënten aanvankelijk, maar krijgen later een terugval doordat de tumor manieren vindt om de blokkade te omzeilen. In muismodellen vergeleken de auteurs oorspronkelijke leverkankercellen met varianten die resistentie tegen lenvatinib hadden ontwikkeld. Zij ontdekten dat resistente tumoren niet alleen het middel overleefden, maar ook sneller groeiden en veel meer longmetastasen produceerden, waardoor de overleving afnam. Dit suggereerde dat resistentie gekoppeld was aan een agressievere, verspreidende gedragswijze in plaats van slechts een verlies van medicijneffect.
Kleine boodschappers die de longen voorbereiden
Om te begrijpen hoe resistente tumoren dit metastatische voordeel verkrijgen, richtte het team zich op extracellulaire blaasjes—kleine belletjes die door cellen worden afgescheiden en eiwitten en ander materiaal via de bloedbaan vervoeren. Met beeldvorming en deeltjestracking toonden zij aan dat lenvatinib-resistente leverkankercellen aanzienlijk meer van deze blaasjes vrijgaven dan hun niet-resistente tegenhangers, en dat de blaasjes zich bij voorkeur in de longen van muizen ophoopten. Wanneer gezonde muizen werden “voorbehandeld” met blaasjes van resistente tumoren, leidden latere injecties met leverkankercellen tot veel meer longtumoren, wat aantoont dat de blaasjes actief een gastvrije “bodem” voor kankerkernen klaarmaken. 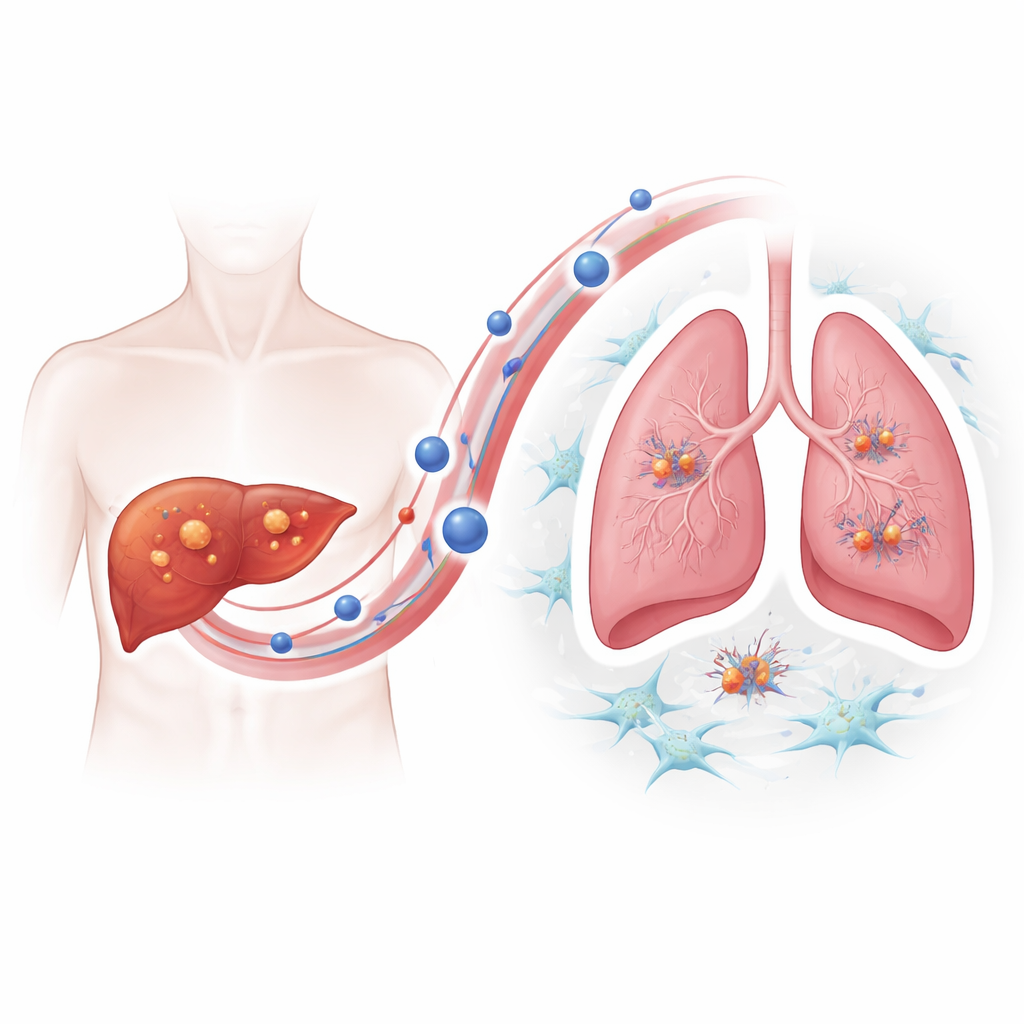
Een moleculaire handdruk die longhelpers wekt
Proteomische analyse onthulde dat blaasjes van resistente tumoren verrijkt waren in een oppervlakte-eiwit genaamd integrine beta-4. Integrines helpen cellen zich aan hun omgeving te hechten, en hier fungeerde integrine beta-4 op blaasjes als een moleculaire handdruk met laminine, een belangrijk bestanddeel van longweefsel. De blaasjes werden het meest efficiënt opgenomen door longfibroblasten—steuncellen die weefsel kunnen herschikken. Eenmaal geactiveerd door deze blaasjes kregen fibroblasten een meer gespierde, contractiele toestand en begonnen ze ontstekingsmoleculen en groeifactoren uit te scheiden. Dit proces hing af van een signaalcascade binnen fibroblasten die bekendstaat als het PI3K–AKT–p65-pad; het blokkeren van sleutelstappen in die cascade dempte de activatie van fibroblasten en verminderde de pro-metastatische signalen die ze produceerden. Blaasjes zonder integrine beta-4 verloren grotendeels hun vermogen longkolonisatie te stimuleren.
Een interne schakelaar die blaasjesafgifte verhoogt
Waarom geven resistente tumorcellen in de eerste plaats zoveel blaasjes af? De auteurs traceerden dit terug naar hyperactivatie van een hoofdregelaar van groei genaamd mTOR, die ook een cellulair recyclemechanisme regelt dat bekendstaat als autofagie. In resistente cellen verstoorde actief mTOR de normale afbraak van multivesiculaire lichamen—interne compartimenten die ofwel uiteen kunnen vallen of met het celoppervlak kunnen fuseren om blaasjes vrij te geven. Wanneer de afbraak werd geblokkeerd, werden deze compartimenten naar secretie geleid, waardoor de blaasjesproductie sterk toenam. Behandeling van resistente cellen met rapamycine, een klassieke mTOR-remmer, herstelde de autofagische afbraak van deze compartimenten, verminderde de blaasjesafgifte en verlaagde de hoeveelheid integrine beta-4 die door de overgebleven blaasjes werd gedragen. 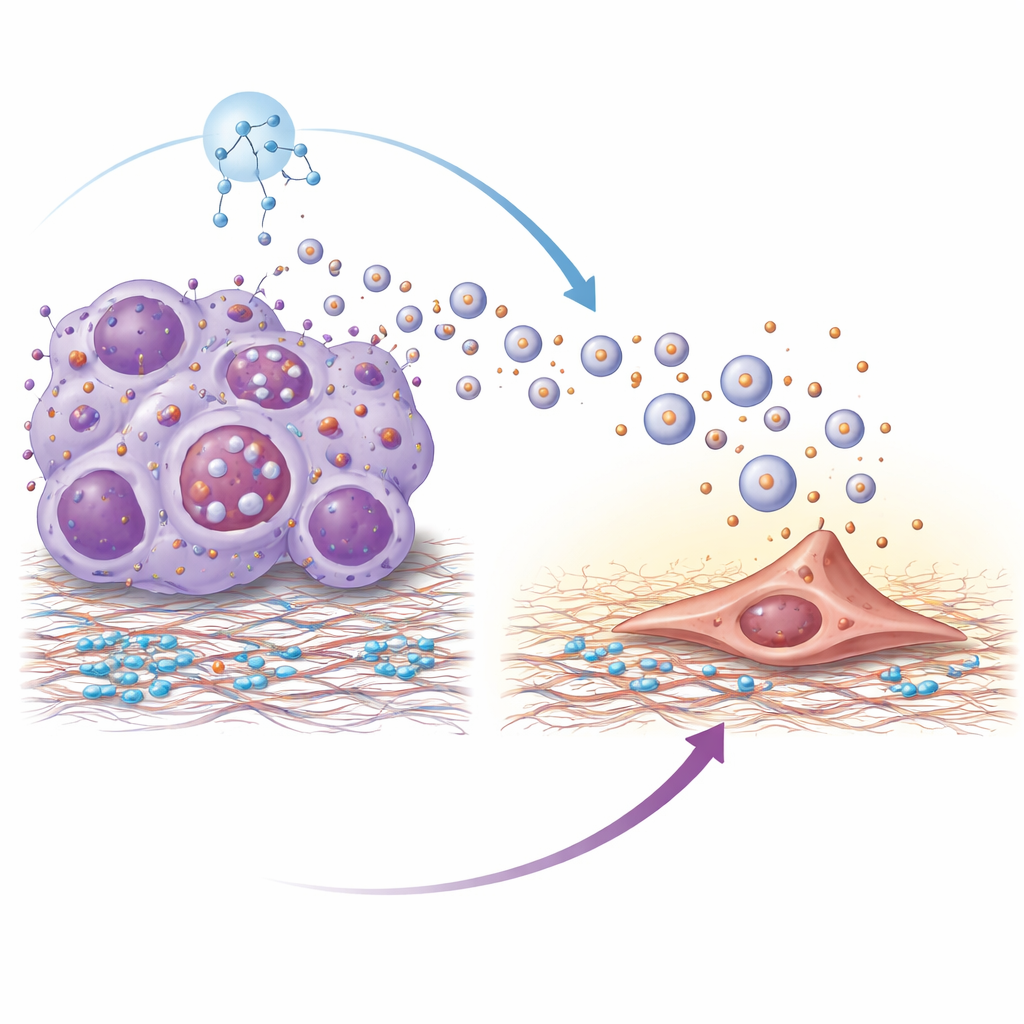
Een combinatiestrategie met klinische aanwijzingen
Bij muizen krompen resistente tumoren effectiever wanneer rapamycine met lenvatinib werd gecombineerd, werden longmetastasen verminderd en nam de overleving toe vergeleken met elk middel alleen. Blaasjes van rapamycine-behandelde resistente cellen waren veel minder in staat om longfibroblasten te activeren of een pre-metastatische longniche te bevorderen. In bloedmonsters van leverkankerpatiënten werden hogere niveaus van integrine beta-4 op circulerende blaasjes geassocieerd met een slechte respons op lenvatinib, meer frequente longmetastase en slechtere overleving, wat suggereert dat deze marker kan helpen patiënten te signaleren die risico lopen op agressieve verspreiding.
Wat dit betekent voor patiënten
Voor een niet-specialist laat dit werk zien dat medicatieresistente levertumoren meer doen dan behandeling negeren—ze sturen vloten microscopische pakketjes uit die de longen “zachter” maken en lokale steuncellen tot stilzwijgende medeplichtigen transformeren. Door mTOR als de interne schakel te identificeren die deze gevaarlijke boodschappen versterkt, en integrine beta-4 als een belangrijk adreslabel dat ze richting geeft, wijst de studie op twee praktische kansen: het gebruik van het niveau van integrine beta-4 op blaasjes in bloed als vroeg waarschuwingssignaal, en het combineren van mTOR-remmende geneesmiddelen zoals rapamycine met lenvatinib om zowel de medicijngevoeligheid te herstellen als longmetastasen te beperken.
Bronvermelding: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Trefwoorden: hepatocellulair carcinoom, medicatie-resistentie, extracellulaire blaasjes, longmetastase, mTOR-signaleringspad