Clear Sky Science · ru
внеклеточные везикулы, обогащённые интегрином β4 и управляемые mTOR, из гепатоцеллюлярной карциномы, резистентной к ленватинибу, способствуют метастазированию в лёгкие через формирование фибробластного нишевого микроокружения
Почему это исследование важно
Рак печени — одно из самых смертельных заболеваний в мире, и даже мощные новые препараты часто теряют эффективность по мере адаптации опухолей. В этом исследовании изучают, как опухоли печени, ставшие резистентными к ленватинибу, могут фактически лучше распространяться в лёгкие. Раскрывая скрытые «сообщения», которые эти резистентные опухоли посылают в отдалённые органы, авторы выявляют уязвимую точку, на которую можно воздействовать, чтобы замедлить метастазирование и восстановить чувствительность к препарату.
Лекарственная резистентность с опасным побочным эффектом
Ленватиниб — один из основных препаратов для продвинутой стадии рака печени; он действует за счёт ограничения кровоснабжения и блокирования сигнальных путей роста. Однако у многих пациентов первоначальный ответ сменяется рецидивом, когда опухоль обходит блокаду. В мышиных моделях авторы сравнили исходные клетки рака печени с вариантами, приобретшими резистентность к ленватинибу. Они обнаружили, что резистентные опухоли не только выживали при лечении, но и росли быстрее и давали значительно больше метастаз в лёгкие, укорачивая выживаемость. Это указывало на то, что резистентность связана с более агрессивным, склонным к распространению поведением, а не только с утратой чувствительности к лекарству.
Крошечные вестники, подготавливающие лёгкие
Чтобы понять, как резистентные опухоли приобретают преимущество в метастазировании, команда сосредоточилась на внеклеточных везикулах — маленьких пузырьках, которые выделяют клетки и которые переносят белки и другой груз через кровоток. С помощью визуализации и трекинга частиц они показали, что клетки рака печени, резистентные к ленватинибу, выделяют значительно больше таких везикул, чем нерезистентные аналоги, и что везикулы преимущественно накапливаются в лёгких мышей. Когда здоровых мышей «предварительно лечили» везикулами из резистентных опухолей, последующие инъекции клеток рака печени приводили к образованию гораздо большего числа лёгочных опухолей, что демонстрирует: везикулы активно готовят благоприятную «почву» для посевов рака. 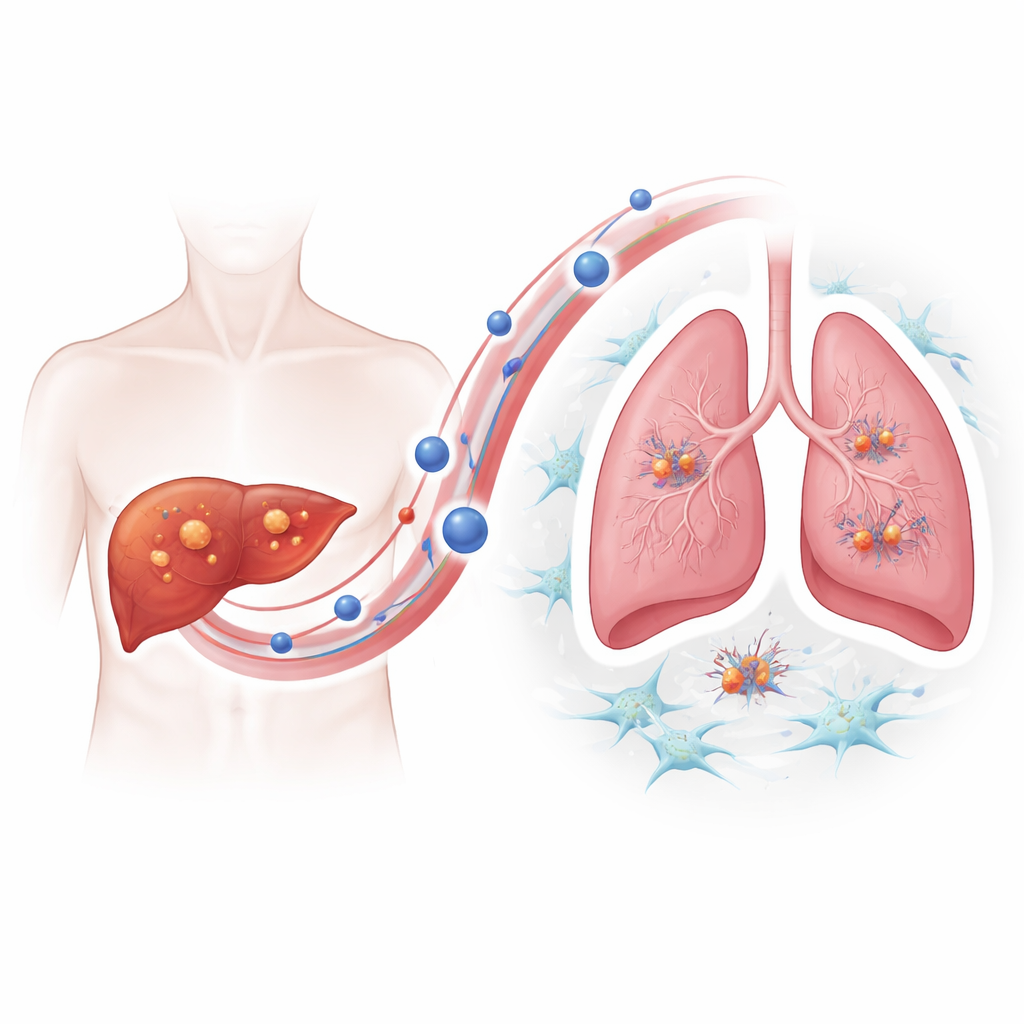
Молекулярное рукопожатие, пробуждающее лёгочных помощников
Протеомный анализ показал, что везикулы из резистентных опухолей обогащены белком поверхности — интегрином бета‑4. Интегрины помогают клеткам прикрепляться к окружению, и в данном случае интегрин β4 на везикулах действовал как молекулярное «рукопожатие» с ламинином — важным компонентом лёгочной ткани. Везикулы наиболее эффективно поглощались лёгочными фибробластами — поддерживающими клетками, способными ремоделировать ткань. После активации этими везикулами фибробласты переходили в более мышечное, контрактильное состояние и начинали секрецию провоспалительных молекул и факторов роста. Этот процесс зависел от сигнального каскада в фибробластах, известного как путь PI3K–AKT–p65; блокирование ключевых звеньев этого каскада ослабляло активацию фибробластов и снижало выработку про‑метастатических сигналов. Везикулы, лишённые интегрина β4, в значительной степени теряли способность вызывать колонизацию лёгких.
Внутренний переключатель, повышающий выделение везикул
Почему же резистентные клетки так много выделяют везикул? Авторы проследили это до гиперактивации главного регулятора роста mTOR, который также контролирует клеточную систему утилизации — аутофагию. В резистентных клетках активный mTOR нарушал нормальную деградацию мультивезикулярных телец — внутренних компартментов, которые либо разрушаются, либо сливаются с мембраной для выделения везикул. Когда деградация была нарушена, эти компартменты перенаправлялись на путь секреции, что значительно увеличивало объём выделяемых везикул. Обработка резистентных клеток рапамицином, классическим ингибитором mTOR, восстанавливала аутофагическое разрушение этих компартментов, снижала выделение везикул и уменьшала количество интегрина β4 в оставшихся везикулах. 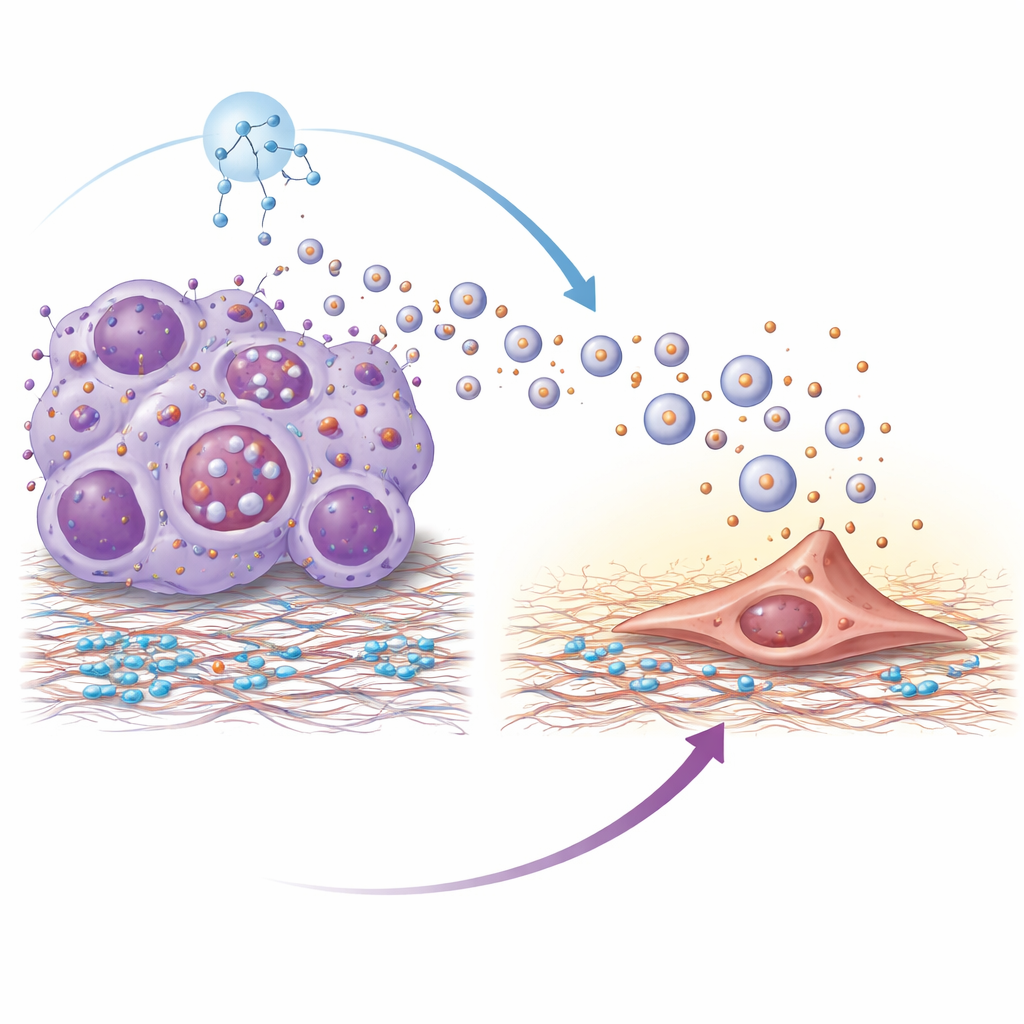
Комбинированная стратегия с клиническими указаниями
У мышей комбинация рапамицина и ленватиниба эффективнее уменьшала резистентные опухоли, снижала число метастазов в лёгкие и продлевала выживаемость по сравнению с каждым препаратом по отдельности. Везикулы из резистентных клеток, обработанных рапамицином, были значительно менее способны активировать лёгочные фибробласты и способствовать формированию преметастатической ниши. В образцах крови пациентов с раком печени более высокий уровень интегрина β4 на циркулирующих везикулах коррелировал с плохим ответом на ленватиниб, более частыми лёгочными метастазами и худшей выживаемостью, что указывает на то, что этот маркер может помочь выявлять пациентов с риском агрессивного распространения.
Что это значит для пациентов
Для непрофессионального читателя эта работа показывает: резистентные опухоли печени делают не только вид, что игнорируют лечение — они отправляют флот микроскопических «посылок», которые «смягчают» лёгкие, превращая местные клетки‑поддержки в молчаливых соучастников. Идентификация mTOR как внутреннего переключателя, усиливающего эти опасные сообщения, и интегрина β4 как ключевой «адресной» метки указывает на две практические возможности: использование уровня интегрина β4 в везикулах крови как раннего сигнала тревоги и комбинирование mTOR‑ингибиторов, таких как рапамицин, с ленватинибом для восстановления чувствительности к лечению и сдерживания метастазирования в лёгкие.
Цитирование: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Ключевые слова: гепатоцеллюлярная карцинома, лекарственная резистентность, внеклеточные везикулы, метастазирование в лёгкие, сигнализация mTOR