Clear Sky Science · pt
Vesículas extracelulares enriquecidas em integrina β4 dirigidas por mTOR de carcinoma hepatocelular resistente à lenvatinibe promovem metástase pulmonar via formação de nicho fibroblástico
Por que esta pesquisa importa
O câncer de fígado é um dos cânceres mais letais no mundo, e até medicamentos novos e potentes frequentemente perdem eficácia à medida que os tumores se adaptam. Este estudo investiga como tumores hepáticos que se tornaram resistentes à lenvatinibe podem, na verdade, tornar‑se melhores em se espalhar para os pulmões. Ao desvendar as “mensagens” ocultas que esses tumores resistentes enviam a órgãos distantes, os pesquisadores identificam um ponto vulnerável que pode ser mirado tanto para frear a metástase quanto para restaurar a sensibilidade ao medicamento.
Resistência a medicamentos com um efeito colateral perigoso
A lenvatinibe é um comprimido utilizado no tratamento avançado do câncer de fígado que atua cortando o suprimento sanguíneo e bloqueando sinais de crescimento. Ainda assim, muitos pacientes respondem inicialmente e depois recaem, à medida que o tumor encontra formas de contornar o bloqueio. Em modelos murinos, os autores compararam células de câncer de fígado originais com versões que haviam adquirido resistência à lenvatinibe. Eles descobriram que os tumores resistentes não apenas sobreviveram ao fármaco, mas também cresceram mais rápido e produziram muito mais metástases pulmonares, encurtando a sobrevida. Isso sugeriu que a resistência estava ligada a um comportamento mais agressivo e disseminador, e não meramente à perda do efeito do medicamento.
Mensageiros minúsculos que preparam os pulmões
Para entender como os tumores resistentes ganham essa vantagem metastática, a equipe concentrou‑se em vesículas extracelulares — pequenas bolhas liberadas pelas células que transportam proteínas e outras cargas pela corrente sanguínea. Usando imagem e rastreamento de partículas, eles mostraram que células de câncer de fígado resistentes à lenvatinibe liberavam significativamente mais dessas vesículas do que suas contrapartes não resistentes, e que as vesículas se acumulavam preferencialmente nos pulmões de camundongos. Quando camundongos saudáveis foram “pré‑tratados” com vesículas provenientes de tumores resistentes, injeções subsequentes de células de câncer de fígado geraram muito mais tumores pulmonares, demonstrando que as vesículas ativamente preparam um “solo” acolhedor para as sementes do câncer. 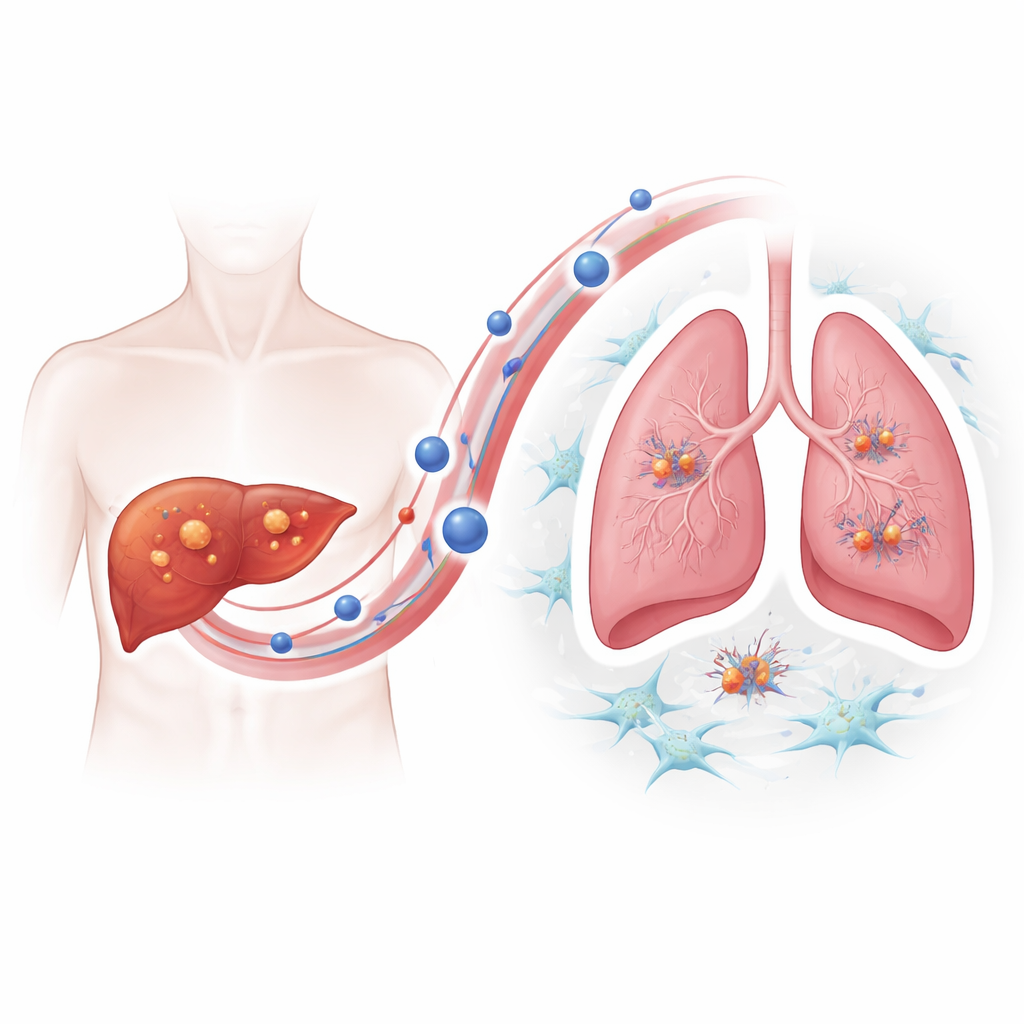
Um aperto de mão molecular que desperta os ajudantes pulmonares
Análises proteômicas revelaram que as vesículas de tumores resistentes eram enriquecidas em uma proteína de superfície chamada integrina beta‑4. Integrinas ajudam as células a se fixarem no entorno, e aqui a integrina beta‑4 nas vesículas atuava como um aperto de mão molecular com a laminina, um componente importante do tecido pulmonar. As vesículas eram internalizadas com maior eficiência por fibroblastos pulmonares — células de suporte que podem remodelar o tecido. Uma vez ativados por essas vesículas, os fibroblastos adotaram um estado mais muscular e contrátil e começaram a secretar moléculas inflamatórias e fatores de crescimento. Esse processo dependia de uma cascata de sinalização dentro dos fibroblastos conhecida como via PI3K–AKT–p65; bloquear etapas-chave dessa cascata atenuou a ativação dos fibroblastos e reduziu os sinais promotores de metástase que eles produziam. Vesículas desprovidas de integrina beta‑4 perderam em grande parte sua capacidade de promover a colonização pulmonar.
Um interruptor interno que aumenta a liberação de vesículas
Por que células tumorais resistentes liberam tantas vesículas em primeiro lugar? Os autores rastrearam isso até a hiperativação de um regulador mestre do crescimento chamado mTOR, que também controla um sistema celular de reciclagem conhecido como autofagia. Nas células resistentes, o mTOR ativo prejudicou a degradação normal de corpos multivesiculares — compartimentos internos que podem ser degradados ou fundir‑se com a superfície celular para liberar vesículas. Quando a degradação foi bloqueada, esses compartimentos foram direcionados para secreção, aumentando bastante a produção de vesículas. Tratar as células resistentes com rapamicina, um inibidor clássico de mTOR, restaurou a degradação autofágica desses compartimentos, reduziu a liberação de vesículas e diminuiu a quantidade de integrina beta‑4 transportada pelas vesículas remanescentes. 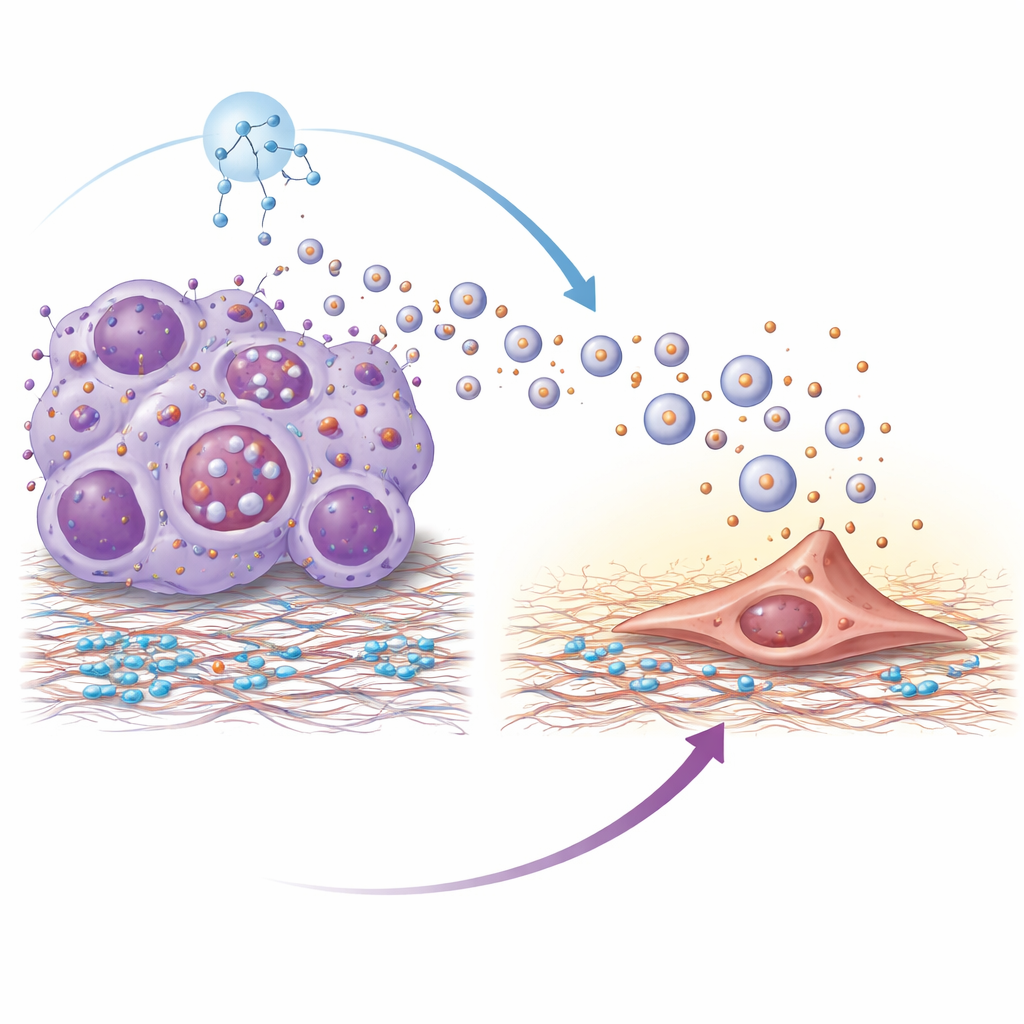
Uma estratégia combinada com pistas clínicas
Em camundongos, a combinação de rapamicina com lenvatinibe reduziu os tumores resistentes de forma mais eficaz, diminuiu as metástases pulmonares e prolongou a sobrevida em comparação com cada fármaco isoladamente. Vesículas de células resistentes tratadas com rapamicina foram muito menos capazes de ativar fibroblastos pulmonares ou promover um nicho pulmonar pré‑metastático. Em amostras de sangue de pacientes com câncer de fígado, níveis mais altos de integrina beta‑4 em vesículas circulantes foram associados a pior resposta à lenvatinibe, maior frequência de metástase pulmonar e pior sobrevida, sugerindo que esse marcador pode ajudar a identificar pacientes em risco de disseminação agressiva.
O que isso significa para os pacientes
Para um observador leigo, este trabalho mostra que tumores hepáticos resistentes a medicamentos fazem mais do que simplesmente ignorar o tratamento — eles enviam frotas de pacotes microscópicos que “amolecem” os pulmões, transformando células de suporte locais em cúmplices silenciosos. Ao identificar o mTOR como o interruptor interno que aumenta essas mensagens perigosas, e a integrina beta‑4 como um selo de endereço chave que as guia, o estudo aponta duas oportunidades práticas: usar os níveis de integrina beta‑4 nas vesículas sanguíneas como um sinal de alerta precoce, e combinar fármacos bloqueadores de mTOR como a rapamicina com lenvatinibe para tanto restaurar a sensibilidade ao tratamento quanto conter a metástase pulmonar.
Citação: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Palavras-chave: carcinoma hepatocelular, resistência a fármacos, vesículas extracelulares, metástase pulmonar, sinalização mTOR