Clear Sky Science · de
mTOR-gesteuerte, mit Integrin β4 angereicherte extrazelluläre Vesikel aus lenvatinib-resistentem hepatozellulärem Karzinom fördern Lungenmetastasen durch Bildung einer Fibroblasten-Nische
Warum diese Forschung wichtig ist
Leberkrebs gehört zu den tödlichsten Krebsarten weltweit, und selbst potente neue Medikamente verlieren oft an Wirksamkeit, wenn Tumoren sich anpassen. Diese Studie untersucht, wie Lebertumoren, die gegen das Medikament Lenvatinib resistent geworden sind, tatsächlich besser dazu in der Lage sein können, in die Lunge zu streuen. Indem die Forschenden die verborgenen „Botschaften“ aufdecken, die diese resistenten Tumoren an entfernte Organe senden, identifizieren sie einen Schwachpunkt, der angegriffen werden könnte, um sowohl Metastasen zu verlangsamen als auch die Medikamentenempfindlichkeit wiederherzustellen.
Arzneimittelresistenz mit einem gefährlichen Nebeneffekt
Lenvatinib ist eine zentrale orale Therapie für fortgeschrittenen Leberkrebs, die die Blutversorgung unterbindet und Wachstumssignale blockiert. Viele Patientinnen und Patienten sprechen zwar zunächst an, erleiden aber später oft ein Wiederauftreten, wenn der Tumor Wege findet, die Blockade zu umgehen. In Mausmodellen verglichen die Autorinnen und Autoren ursprüngliche Leberkrebszellen mit Varianten, die Lenvatinib-Resistenz erworben hatten. Sie stellten fest, dass resistente Tumoren nicht nur dem Medikament trotzen, sondern auch schneller wuchsen und deutlich mehr Lungenmetastasen bildeten, was das Überleben verkürzte. Das legt nahe, dass die Resistenz mit einem aggressiveren, stärker streuenden Verhalten verbunden ist und nicht nur mit einem Verlust der Medikamentenwirkung.
Winzige Boten, die die Lunge vorbereiten
Um zu verstehen, wie resistente Tumoren diesen metastatischen Vorteil erlangen, konzentrierte sich das Team auf extrazelluläre Vesikel — winzige Bläschen, die von Zellen abgesondert werden und Proteine sowie andere Fracht durch den Blutkreislauf transportieren. Mit Bildgebung und Partikelverfolgung zeigten sie, dass Lenvatinib-resistente Leberkrebszellen deutlich mehr dieser Vesikel freisetzten als nicht-resistente Gegenstücke und dass sich die Vesikel bevorzugt in den Lungen der Mäuse ansammelten. Wenn gesunde Mäuse vorab mit Vesikeln aus resistenten Tumoren „vorausbehandelt“ wurden, führten spätere Injektionen von Leberkrebszellen zu deutlich mehr Lungentumoren — ein Beleg dafür, dass die Vesikel aktiv einen einladenden „Boden“ für Krebssamen vorbereiten. 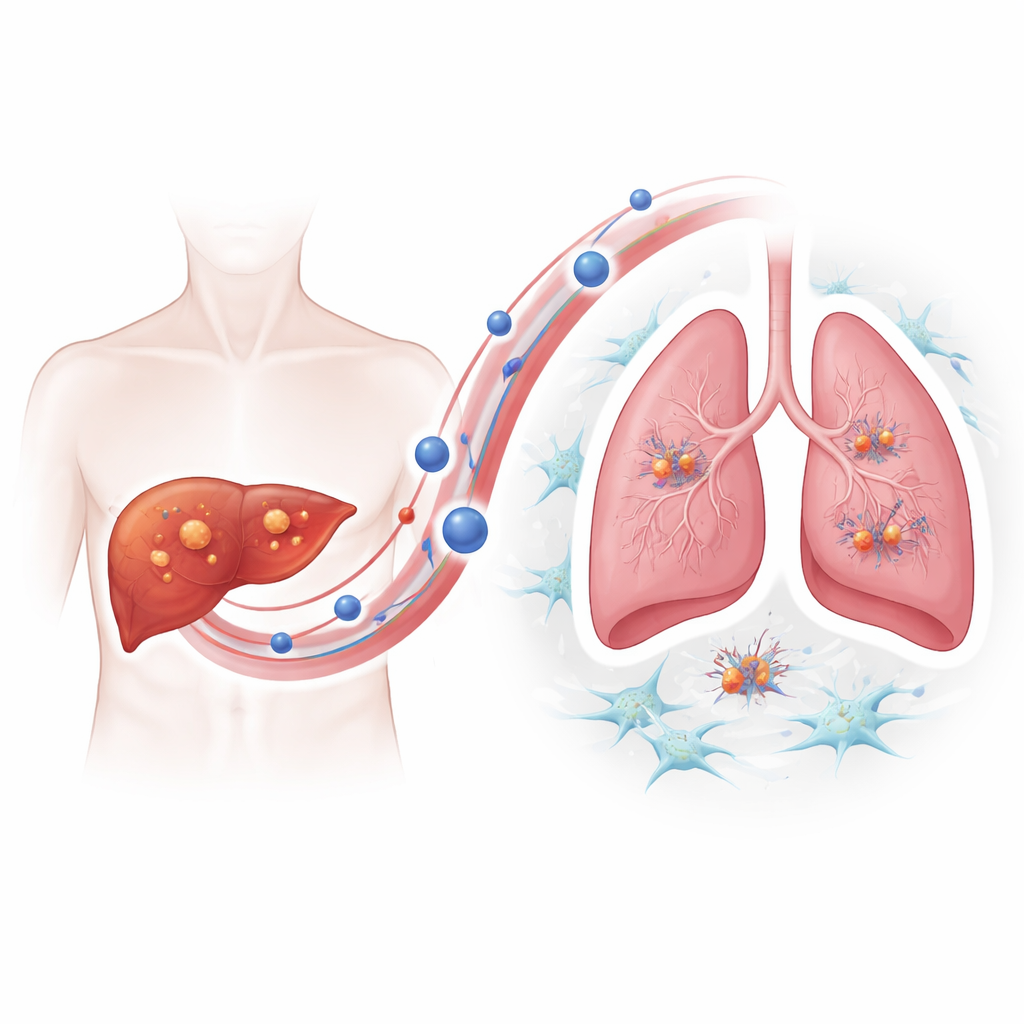
Ein molekularer Händedruck, der Lungen‑Helfer weckt
Proteomanalysen ergaben, dass Vesikel aus resistenten Tumoren mit dem Oberflächenprotein Integrin Beta‑4 angereichert waren. Integrine helfen Zellen, sich an ihre Umgebung anzuheften; hier fungierte Integrin Beta‑4 auf den Vesikeln wie ein molekularer Händedruck mit Laminin, einem wichtigen Bestandteil des Lungengewebes. Die Vesikel wurden am effizientesten von Lungenfibroblasten aufgenommen — Stützzellen, die Gewebe umgestalten können. Nach Aktivierung durch diese Vesikel nahmen Fibroblasten einen muskulöseren, kontraktilen Zustand an und begannen, entzündungsfördernde Moleküle und Wachstumsfaktoren zu sezernieren. Dieser Prozess hing von einer Signalkaskade innerhalb der Fibroblasten ab, die als PI3K–AKT–p65‑Weg bekannt ist; die Blockade zentraler Schritte dieser Kaskade dämpfte die Aktivierung der Fibroblasten und verringerte die pro‑metastatischen Signale, die sie produzierten. Vesikel ohne Integrin Beta‑4 verloren weitgehend ihre Fähigkeit, die Besiedlung der Lunge zu fördern.
Ein interner Schalter, der die Vesikelfreisetzung steigert
Warum setzen resistente Tumorzellen überhaupt so viele Vesikel frei? Die Autorinnen und Autoren führten dies auf eine Hyperaktivierung eines zentralen Wachstumsregulators namens mTOR zurück, der auch ein zelluläres Recycling‑System namens Autophagie steuert. In resistenten Zellen beeinträchtigte aktives mTOR den normalen Abbau multivesikulärer Körper — interne Kompartimente, die entweder abgebaut oder mit der Zelloberfläche verschmelzen können, um Vesikel freizusetzen. Wenn der Abbau blockiert war, wurden diese Kompartimente in Richtung Sekretion umgeleitet, was die Vesikelausgabe stark erhöhte. Die Behandlung resistenter Zellen mit Rapamycin, einem klassischen mTOR‑Inhibitor, stellte den autophagischen Abbau dieser Kompartimente wieder her, verringerte die Vesikelfreisetzung und senkte die Menge an Integrin Beta‑4 in den verbleibenden Vesikeln. 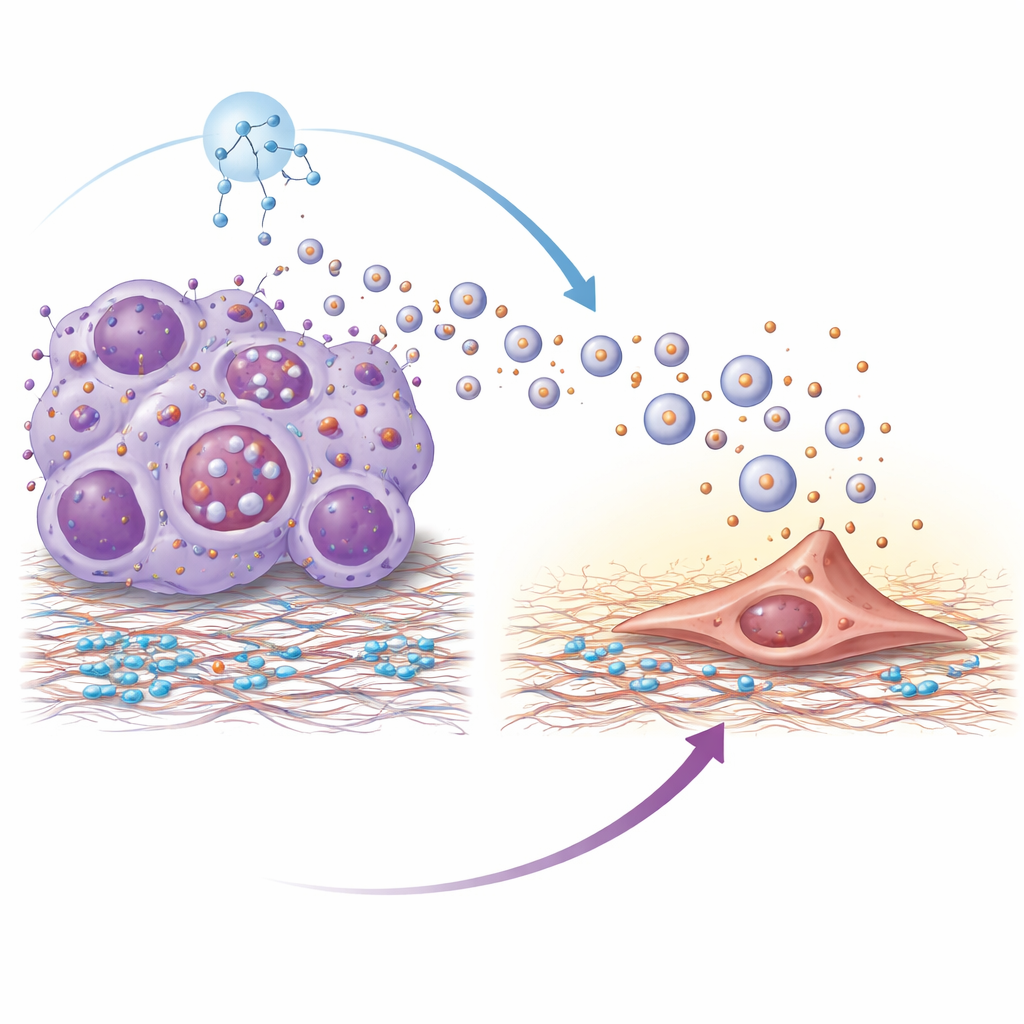
Eine Kombinationsstrategie mit klinischen Hinweisen
Bei Mäusen schrumpfte die Kombination aus Rapamycin und Lenvatinib resistente Tumoren effektiver, reduzierte Lungenmetastasen und verlängerte das Überleben im Vergleich zu einem der beiden Medikamente allein. Vesikel aus Rapamycin‑behandelten resistenten Zellen waren deutlich weniger in der Lage, Lungenfibroblasten zu aktivieren oder eine prämetastatische Lungennische zu fördern. In Blutproben von Patientinnen und Patienten mit Leberkrebs waren höhere Spiegel von Integrin Beta‑4 auf zirkulierenden Vesikeln mit schlechterer Reaktion auf Lenvatinib, häufigerem Auftreten von Lungenmetastasen und schlechterem Überleben verknüpft, was nahelegt, dass dieser Marker helfen könnte, Patienten mit Risiko für aggressive Streuung zu identifizieren.
Was das für Patientinnen und Patienten bedeutet
Für Laien zeigt diese Arbeit, dass medikamentenresistente Lebertumoren mehr tun, als nur eine Behandlung zu ignorieren — sie verschicken Heerscharen mikroskopischer Pakete, die die Lunge „aufweichen“ und lokale Stützzellen zu stillen Komplizen machen. Indem die Studie mTOR als den internen Schalter identifiziert, der diese gefährlichen Botschaften verstärkt, und Integrin Beta‑4 als wichtigen Adressaufkleber, weist sie auf zwei praktische Möglichkeiten hin: die Messung von Integrin Beta‑4 auf Vesikeln im Blut als Frühwarnsignal sowie die Kombination von mTOR‑blockierenden Medikamenten wie Rapamycin mit Lenvatinib, um sowohl die Medikamentenempfindlichkeit wiederherzustellen als auch Lungenmetastasen einzudämmen.
Zitation: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Schlüsselwörter: hepatozelluläres Karzinom, Arzneimittelresistenz, extrazelluläre Vesikel, Lungenmetastasen, mTOR-Signalübertragung