Clear Sky Science · sv
mTOR-drivna integrin β4-rika extracellulära vesiklar från lenvatinib-resistent hepatocellulär cancer främjar lungmetastasering via fibroblast-nischbildning
Varför denna forskning är viktig
Levercancer är en av de dödligaste cancerformerna globalt, och även kraftfulla nya läkemedel förlorar ofta effekt när tumörer anpassar sig. Denna studie undersöker hur levertumörer som utvecklat resistens mot läkemedlet lenvatinib faktiskt kan bli bättre på att sprida sig till lungorna. Genom att avslöja de dolda ”meddelanden” som dessa resistenta tumörer skickar till avlägsna organ identifierar forskarna en svag punkt som skulle kunna riktas för att både bromsa metastasering och återställa läkemedelskänslighet.
Läkemedelsresistens med en farlig sidoeffekt
Lenvatinib är en förstahandsbehandling i tablettform för avancerad levercancer som fungerar genom att skära av blodtillförseln och blockera tillväxtsignaler. Många patienter svarar initialt men får senare återfall när tumören hittar sätt att kringgå blockaden. I musmodeller jämförde författarna ursprungliga levercancerceller med varianter som förvärvat resistens mot lenvatinib. De fann att resistenta tumörer inte bara överlevde läkemedlet utan också växte snabbare och gav avsevärt fler lungmetastaser, vilket förkortade överlevnaden. Detta tyder på att resistens var kopplat till ett mer aggressivt, spridningsbenäget beteende snarare än enbart en förlust av läkemedelseffekt.
Små budbärare som förbereder lungorna
För att förstå hur resistenta tumörer får denna metastatiska fördel fokuserade teamet på extracellulära vesiklar—små blåsor som celler avger och som bär proteiner och annat innehåll genom blodomloppet. Med hjälp av bildteknik och partikelspårning visade de att lenvatinib-resistenta levercancerceller släppte avsevärt fler av dessa vesiklar än sina icke-resistenta motsvarigheter, och att vesiklarna föredrog att ackumuleras i lungorna hos möss. När friska möss ”förbehandlades” med vesiklar från resistenta tumörer gav senare injektioner av levercancerceller många fler lungtumörer, vilket visar att vesiklarna aktivt förbereder en välkomnande ”jord” för cancerfrön. 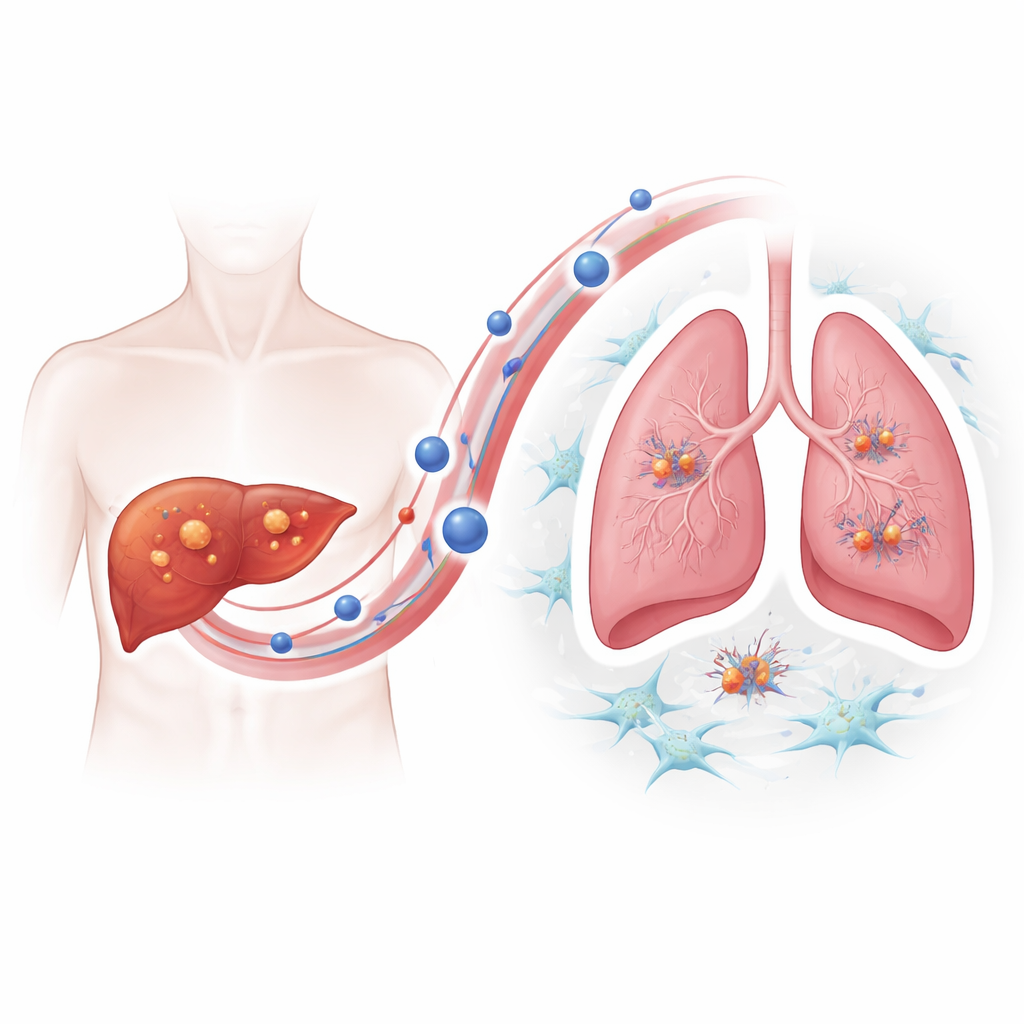
En molekylär handskakning som väcker lunghjälpare
Proteomanalys avslöjade att vesiklar från resistenta tumörer var berikade med ett ytligt protein kallat integrin beta-4. Integriner hjälper celler att fästa vid sin omgivning, och här fungerade integrin beta-4 på vesiklarna som en molekylär handskakning med laminin, en huvudkomponent i lungvävnad. Vesiklarna togs upp mest effektivt av lungfibroblaster—stödjeceller som kan omforma vävnad. När fibroblasterna aktiverades av dessa vesiklar antog de ett mer muskulärt, kontraktilt tillstånd och började utsöndra inflammatoriska molekyler och tillväxtfaktorer. Denna process var beroende av en signalväg inne i fibroblasterna känd som PI3K–AKT–p65; blockering av nyckelsteg i denna kaskad dämpade fibroblastaktivering och minskade de prometastatiska signalerna de producerade. Vesiklar utan integrin beta-4 förlorade i stort sett sin förmåga att driva lungkolonisering.
En intern brytare som ökar vesikelutsläpp
Varför släpper resistenta tumörceller ut så många vesiklar från början? Författarna spårade detta till hyperaktivering av en huvudregulator för tillväxt kallad mTOR, som också styr ett cellulärt återvinningssystem känt som autofagi. I resistenta celler hämmande aktivt mTOR den normala nedbrytningen av multivesikulära kroppar—inre kompartment som antingen kan brytas ner eller fusera med cellmembranet för att släppa ut vesiklar. När nedbrytningen blockerades styrdes dessa kompartment mot sekretion, vilket kraftigt ökade vesikelproduktionen. Behandling av resistenta celler med rapamycin, en klassisk mTOR-hämmare, återställde den autofagiska nedbrytningen av dessa kompartment, minskade vesikelutsöndringen och sänkte mängden integrin beta-4 på de återstående vesiklarna. 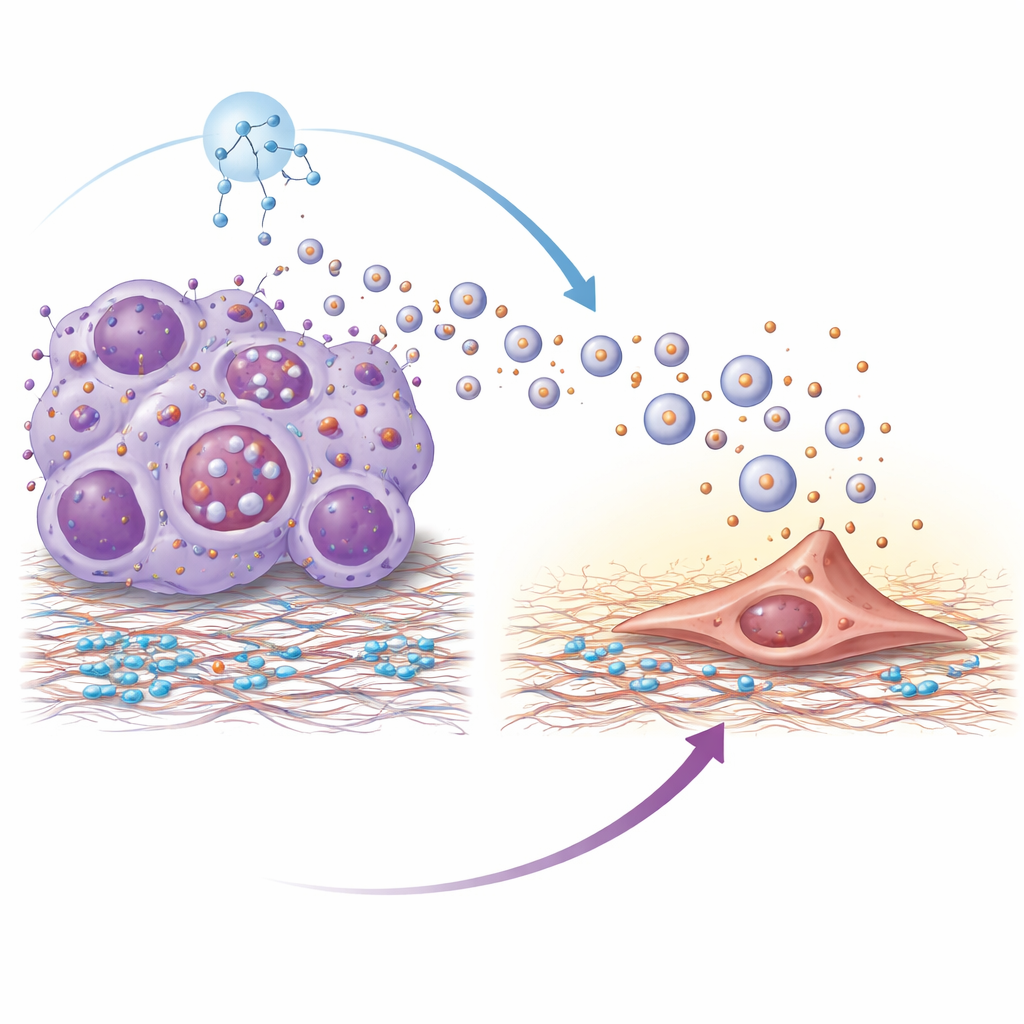
En kombinationsstrategi med kliniska ledtrådar
Hos möss krympte kombinationen av rapamycin och lenvatinib resistenta tumörer mer effektivt, minskade lungmetastaser och förlängde överlevnaden jämfört med något av läkemedlen ensamt. Vesiklar från rapamycinbehandlade resistenta celler var mycket mindre kapabla att aktivera lungfibroblaster eller främja en pre-metastatisk lungnisch. I blodprover från levercancerpatienter kopplades högre nivåer av integrin beta-4 på cirkulerande vesiklar till dålig respons på lenvatinib, oftare lungmetastasering och sämre överlevnad, vilket tyder på att denna markör kan hjälpa till att identifiera patienter i riskzonen för aggressiv spridning.
Vad detta innebär för patienter
För en lekman visar detta arbete att läkemedelsresistenta levertumörer gör mer än att bara ignorera behandling—de skickar ut flottor av mikroskopiska paket som ”mjukar upp” lungorna och förvandlar lokala stödjeceller till tysta medhjälpare. Genom att identifiera mTOR som den interna brytaren som ökar dessa farliga meddelanden, och integrin beta-4 som en viktig adresslapp som styr dem, pekar studien på två praktiska möjligheter: att använda integrin beta-4-nivåer på vesiklar i blodet som en tidig varningssignal, och att kombinera mTOR-hämmande läkemedel som rapamycin med lenvatinib för att både återställa läkemedelskänslighet och begränsa lungmetastasering.
Citering: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Nyckelord: hepatocellulärt karcinom, läkemedelsresistens, extracellulära vesiklar, lungmetastas, mTOR-signalering