Clear Sky Science · pl
pęcherzyki z integryną β4 wzbogacone przez mTOR w lenwatynibie opornym raku wątroby napędzają przerzuty do płuc poprzez tworzenie fibroblastowego nisz
Dlaczego to badanie ma znaczenie
Rak wątroby jest jednym z najbardziej śmiertelnych nowotworów na świecie, a nawet silne nowe leki często tracą skuteczność, gdy guzy się adaptują. To badanie analizuje, w jaki sposób guzy wątroby, które stały się oporne na lek lenwatynib, mogą w rzeczywistości lepiej rozprzestrzeniać się do płuc. Odkrywając ukryte „wiadomości”, jakie te oporne guzy wysyłają do odległych narządów, badacze identyfikują słaby punkt, który można by wykorzystać, by zarówno spowolnić przerzuty, jak i przywrócić wrażliwość na lek.
Oporność na lek z niebezpiecznym skutkiem ubocznym
Lenwatynib to lek doustny stosowany w zaawansowanym raku wątroby, który działa przez ograniczanie ukrwienia i blokowanie sygnałów wzrostu. Jednak wielu pacjentów, mimo początkowej odpowiedzi, później doświadcza nawrotu, gdy guz znajduje sposoby obejścia blokady. W modelach mysich autorzy porównali pierwotne komórki raka wątroby z ich wersjami, które nabyły oporność na lenwatynib. Stwierdzili, że guzy oporne nie tylko przetrwały leczenie, lecz także rosły szybciej i dawały znacznie więcej przerzutów do płuc, skracając czas przeżycia. Sugeruje to, że oporność wiąże się z bardziej agresywnym, przerzutowym zachowaniem, a nie jedynie z utratą działania leku.
Maleńcy posłańcy przygotowujący płuca
Aby zrozumieć, jak guzy oporne zyskują przewagę w przerzutowaniu, zespół skupił się na pęcherzykach zewnątrzkomórkowych — maleńkich pęcherzykach uwalnianych przez komórki, które przenoszą białka i inne ładunki przez krwiobieg. Za pomocą obrazowania i śledzenia cząstek wykazali, że komórki raka wątroby oporne na lenwatynib uwalniały znacząco więcej tych pęcherzyków niż ich niewrażliwe odpowiedniki, a pęcherzyki te kumulowały się preferencyjnie w płucach myszy. Gdy zdrowe myszy były „wstępnie poddawane” działaniu pęcherzyków z opornych guzów, późniejsze wstrzyknięcia komórek raka wątroby powodowały znacznie więcej guzów płucnych, co dowodzi, że pęcherzyki aktywnie przygotowują przyjazne „podłoże” dla zarodków nowotworowych. 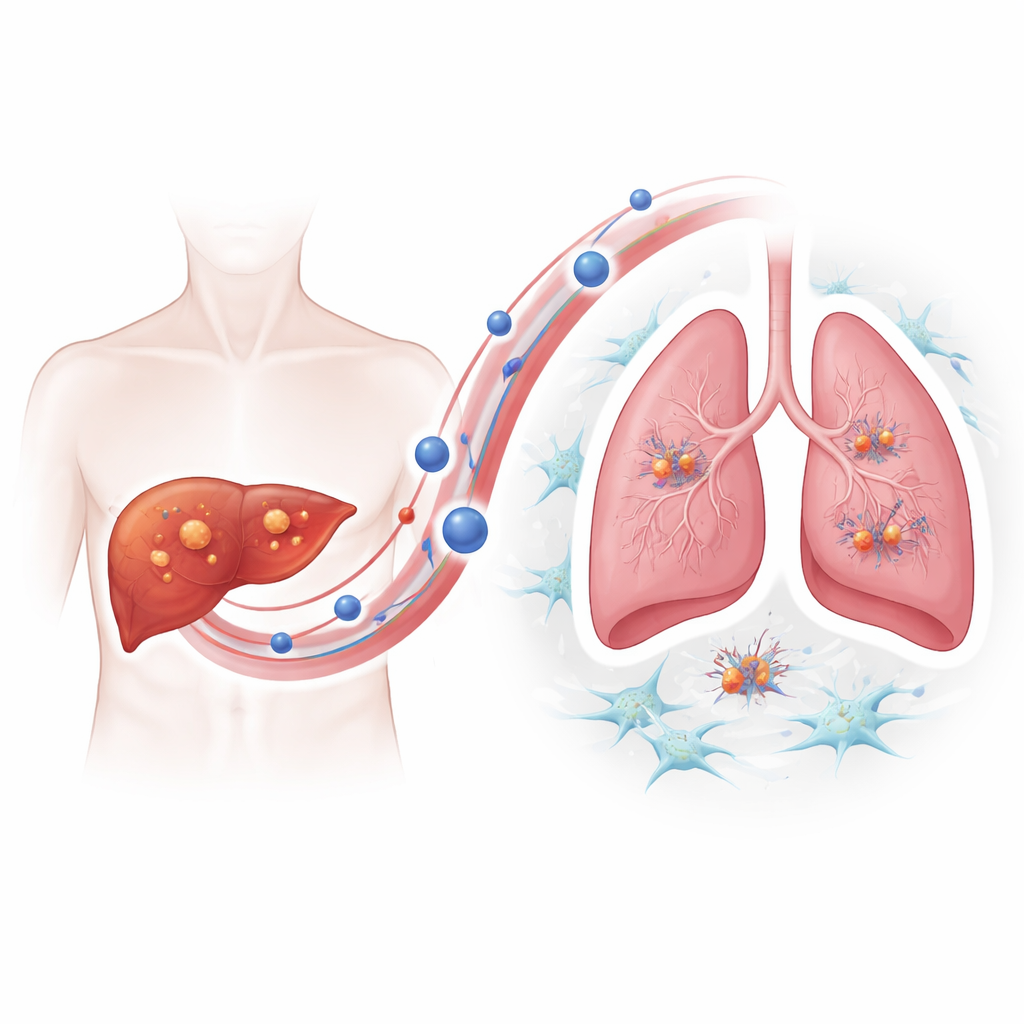
Molekularne uściśnięcie dłoni, które pobudza pomocników w płucach
Analiza proteomiczna ujawniła, że pęcherzyki pochodzące z opornych guzów były wzbogacone w białko powierzchniowe zwane integryną beta-4. Integryny pomagają komórkom przyczepiać się do otoczenia, a tutaj integryna beta-4 na pęcherzykach pełniła rolę molekularnego uściśnięcia dłoni z lamininą — głównym składnikiem tkanki płucnej. Pęcherzyki były najchętniej pobierane przez fibroblasty płucne — komórki podporowe zdolne do przebudowy tkanki. Po aktywacji przez te pęcherzyki fibroblasty przyjmowały bardziej mięśniowy, kurczliwy stan i zaczynały wydzielać molekuły zapalne oraz czynniki wzrostu. Proces ten zależał od kaskady sygnałowej wewnątrz fibroblastów znanej jako szlak PI3K–AKT–p65; blokowanie kluczowych kroków w tej kaskadzie osłabiało aktywację fibroblastów i zmniejszało pro-przerzutowe sygnały, które wytwarzały. Pęcherzyki pozbawione integryny beta-4 w dużej mierze traciły zdolność napędzania kolonizacji płuc.
Wewnętrzny przełącznik, który zwiększa uwalnianie pęcherzyków
Dlaczego komórki oporne uwalniają w pierwszym rzędzie tak wiele pęcherzyków? Autorzy wyśledzili to do nadaktywacji głównego regulatora wzrostu zwanego mTOR, który kontroluje także komórkowy system recyklingu znany jako autofagia. W komórkach opornych aktywny mTOR upośledzał normalną degradację wielopęcherzykowych ciałek — wewnętrznych przedziałów, które mogą być albo degradowane, albo łączyć się z powierzchnią komórki, by uwalniać pęcherzyki. Gdy degradacja była zablokowana, te przedziały były kierowane w stronę sekrecji, co znacznie zwiększało wydzielanie pęcherzyków. Leczenie komórek opornych rapamycyną, klasycznym inhibitorem mTOR, przywracało autofagiczną degradację tych przedziałów, zmniejszało uwalnianie pęcherzyków i obniżało ilość integryny beta-4 przenoszonej przez pozostałe pęcherzyki. 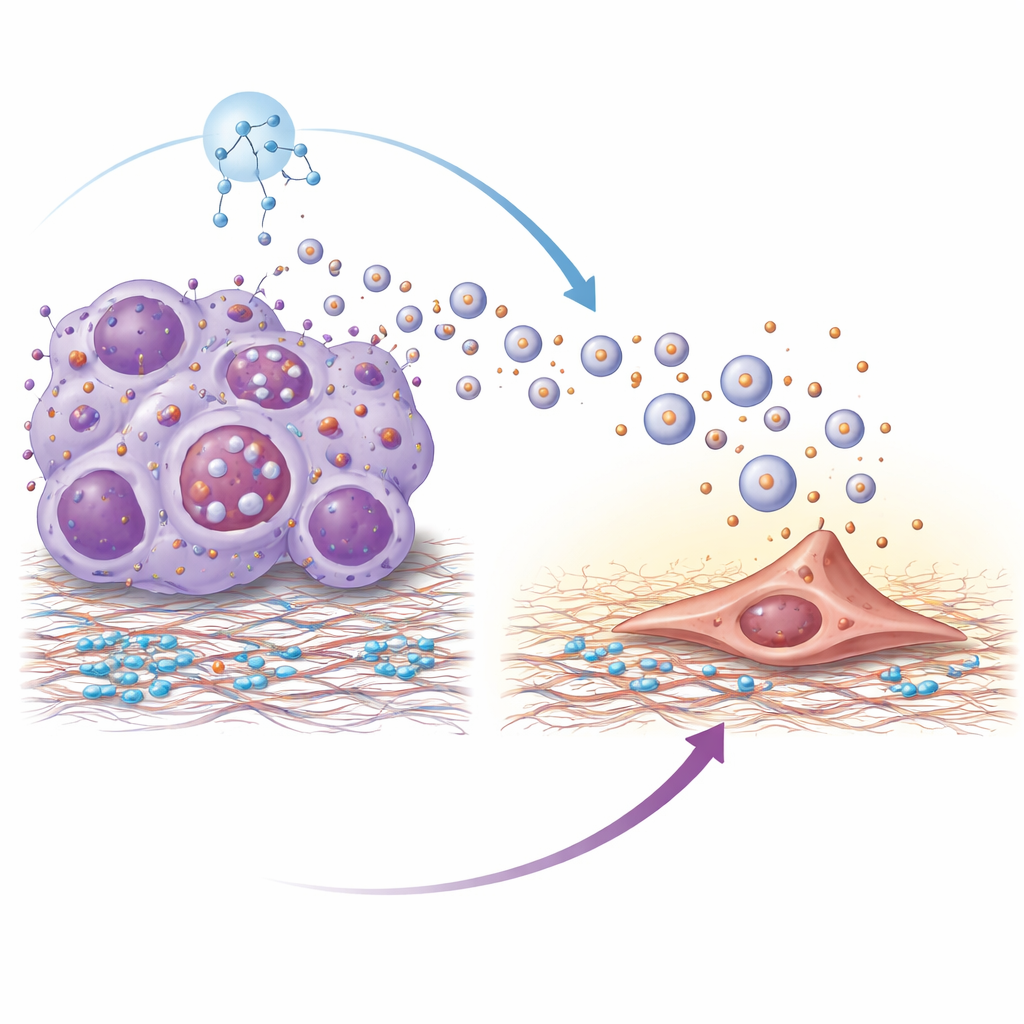
Strategia łączona z przesłankami klinicznymi
U myszy łączenie rapamycyny z lenwatynibem skuteczniej zmniejszało oporne guzy, redukowało przerzuty do płuc i wydłużało przeżycie w porównaniu z każdym z leków stosowanych osobno. Pęcherzyki z komórek opornych traktowanych rapamycyną znacznie rzadziej aktywowały fibroblasty płucne lub sprzyjały tworzeniu przed-przerzutowej niszy w płucach. W próbkach krwi pacjentów z rakiem wątroby wyższe poziomy integryny beta-4 na krążących pęcherzykach łączyły się ze słabą odpowiedzią na lenwatynib, częstszymi przerzutami do płuc i gorszym przeżyciem, co sugeruje, że ten marker mógłby pomóc wyłapać pacjentów zagrożonych agresywnym rozsiewem.
Co to oznacza dla pacjentów
Dla laika ta praca pokazuje, że guzy wątroby oporne na leczenie robią więcej niż tylko ignorują terapię — wysyłają flotę mikroskopijnych paczek, które „zmiękczają” płuca, przekształcając miejscowe komórki podporowe w cichych wspólników. Identyfikując mTOR jako wewnętrzny przełącznik zwiększający te niebezpieczne sygnały oraz integrynę beta-4 jako kluczowy adresowy etykietę je kierującą, badanie wskazuje na dwie praktyczne możliwości: użycie poziomów integryny beta-4 na pęcherzykach we krwi jako wczesnego sygnału alarmowego oraz łączenie leków blokujących mTOR, takich jak rapamycyna, z lenwatynibem, by jednocześnie przywrócić wrażliwość na lek i ograniczyć przerzuty do płuc.
Cytowanie: Zou, T., Wang, X., Sun, H. et al. mTOR-driven integrin β4-enriched extracellular vesicles from lenvatinib-resistant hepatocellular carcinoma fuel lung metastasis via fibroblast-niche formation. Sig Transduct Target Ther 11, 138 (2026). https://doi.org/10.1038/s41392-026-02625-4
Słowa kluczowe: rak wątrobowokomórkowy, oporność na leki, pęcherzyki zewnątrzkomórkowe, przerzuty do płuc, szlak mTOR