Clear Sky Science · zh
进展为七重难治性骨髓瘤涉及 CD38、BCMA 和 GPRC5D 的依次丧失
当癌症连最新药物也被识破
多发性骨髓瘤是骨髓中浆细胞的恶性肿瘤,近年受益于一波新药,尤其是复杂的免疫基于疗法。然而,一些患者最终进入一种疾病对所有主要药物类别均失效的阶段。本研究聚焦这一终末期——称为“七重难治”(hepta‑refractory)骨髓瘤——以理解癌症如何进化以规避众多疗法,并探索医生仍可能找到的有效选项。
骨髓瘤的一个新极端阶段
研究者将七重难治定义为对七类关键治疗均不再响应:两类免疫调节口服药、两类蛋白酶体抑制剂、一种针对细胞表面标志 CD38 的抗体,以及两种瞄准 BCMA 和 GPRC5D 的新型免疫疗法。在若干中心收治的 37 名此类患者中,尽管接受了强化治疗,生存仍很差。达到该阶段后,患者的中位生存约为 13 个月,每增加一线“挽救”治疗通常只能控制病情约三个月。尽管总体预后不佳,但个体差异显著:少数患者表现明显更好,提示其潜在生物学并不完全相同。
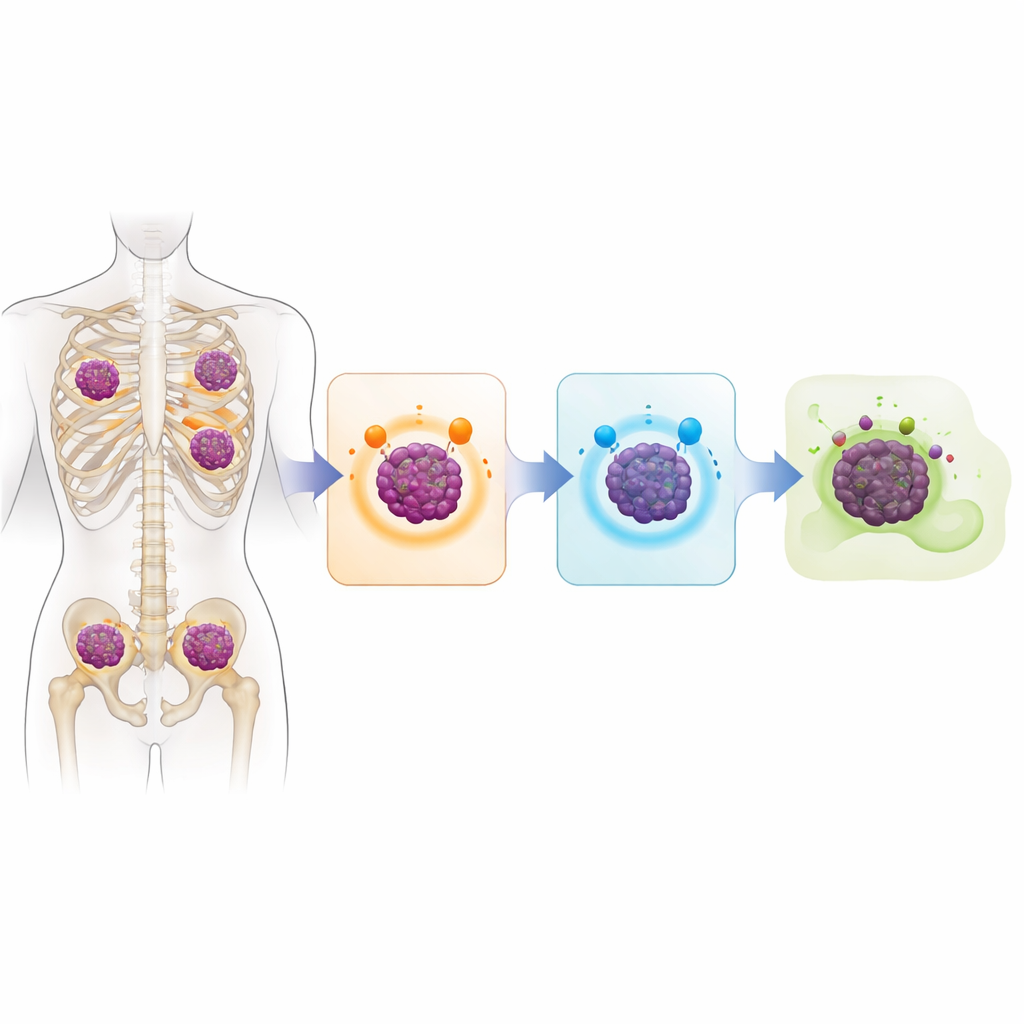
充满警示信号的癌症基因组
为弄清这些肿瘤的特点,团队采用了全基因组测序,这一技术读取肿瘤几乎所有的 DNA。在 17 名有样本的患者中,他们发现基因组高度受损并发生重排,许多经典的抑癌基因受到重击,这些基因通常限制细胞生长或诱导细胞死。常见受损位点包括 TP53 和 CDKN2C,以及其他常与高度侵袭性疾病相关的基因。这些严重改变常见于已经从骨髓扩散到软组织的肿瘤,符合患者病情进展迅速的特点。DNA 模式还带有既往治疗留下的“伤痕”——例如与化疗药物甲氮咪唑类(melphalan)相关的变化——表明多年治疗塑造了癌症的进化轨迹。
肿瘤细胞如何脱除其靶点
核心问题是骨髓瘤细胞如何对现代免疫疗法“隐身”,这些疗法依赖识别细胞表面的特定分子。研究显示,在许多情况下,肿瘤细胞干脆停止产生这些分子。在约 40% 的测序患者中,BCMA 基因的两等位拷贝均被敲除,通常表现为大片段缺失。大约三分之一的患者出现了类似的双等位位点损伤影响 GPRC5D,通常通过缺失与小的致损突变的组合实现。有些患者也丧失了 CD38。被分析组中近三分之一同时丧失了 BCMA 与 GPRC5D,意味着它们不再展示多种当今最强效疗法所需的靶点。
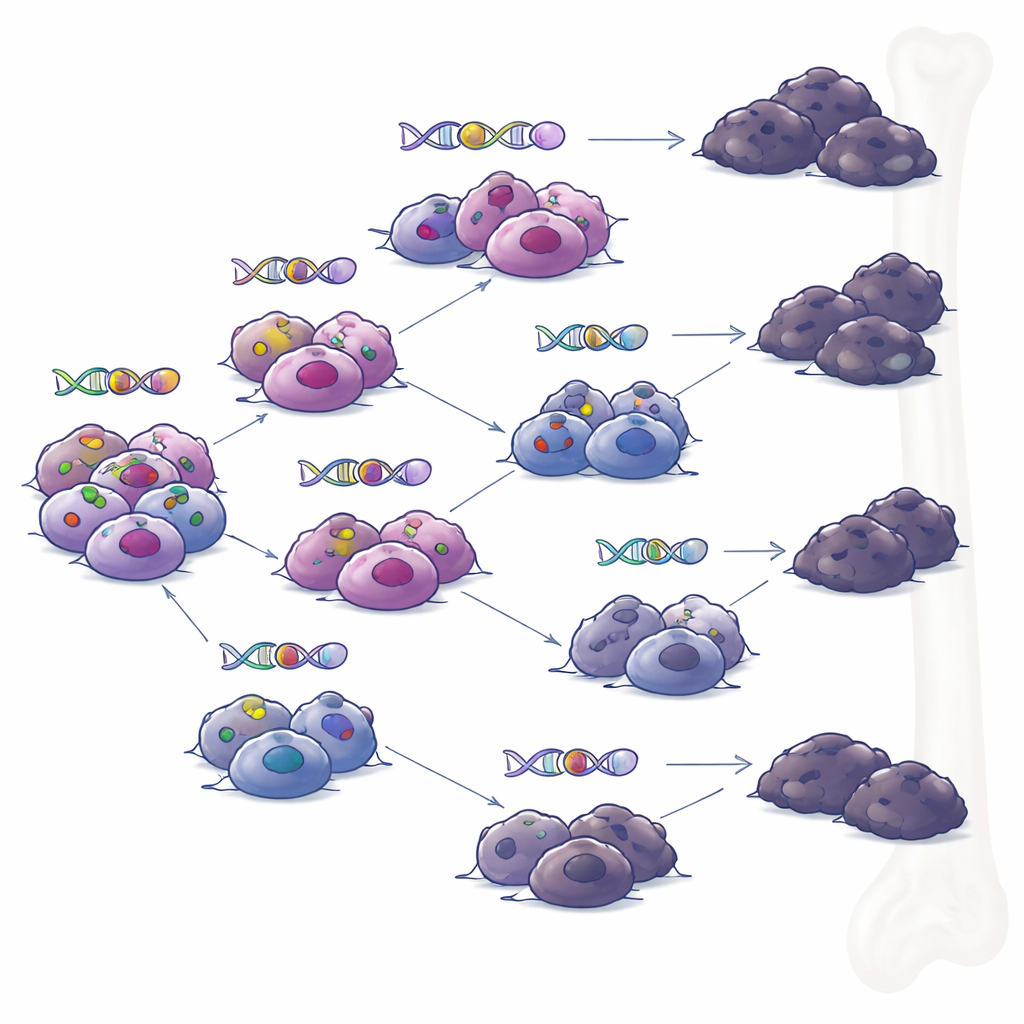
不是单一恶性克隆,而是分支式演化
当团队检查来自同一患者不同时间点的样本时,他们重建了肿瘤的系统发育树。与单一优势克隆不断累积改变不同,他们观察到分支式进化:多个相关的细胞亚群分岔并随着时间获得不同的突变。在针对性免疫疗法压力下,多个分支独立地发展出丧失 BCMA 或 GPRC5D 的方式。这一模式表明,即便治疗看似诱导了深度缓解,具有遗传多样性的小群细胞仍可存留并在随后引发复发,每个分支带有各自的耐药组合策略。
用更深入的检测来指导重治机会
因为基因测序只捕获 DNA,研究者还使用了免疫组化染色方法,以显示 BCMA 蛋白是否确实出现在肿瘤细胞表面。所有在基因层面丧失了 BCMA 双拷贝的肿瘤均显示 BCMA 蛋白完全缺失,但一些在基因上未见明显损伤的肿瘤也在表面几乎看不到 BCMA,暗示存在其他更细微的耐药机制。关键的是,在一小组此前接受过 BCMA 靶向治疗的患者中,那些肿瘤仍保留 BCMA 基因并且显示至少部分 BCMA 蛋白的患者,在再次使用另一种 BCMA 定向 CAR T 细胞治疗时常能再次获益。相比之下,肿瘤完全丧失 BCMA 的患者从此类再治疗中未见获益。
对患者与未来治疗的意义
对多发性骨髓瘤患者而言,这项研究既带来令人警醒的信息,也带来希望。一方面,有些肿瘤能通过系统性丢弃高级免疫疗法所依赖的标志物,演化为高度耐药的状态。另一方面,对肿瘤 DNA 与蛋白标志物的详细检测可以揭示仍然存在的靶点,帮助避免在靶点已丧失时施以徒劳且有副作用的治疗。作者主张,将广泛的基因组分析与染色基于的检测相结合,应成为非常晚期骨髓瘤患者护理的一部分。这样的做法可以更好地将患者与仍有希望的再治疗策略相匹配,同时指导寻找不依赖单一、易丢失靶点的新疗法。
引用: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
关键词: 多发性骨髓瘤, 治疗耐药, 免疫疗法, 抗原丧失, 基因组分析