Clear Sky Science · de
Die Entwicklung zum hepta-refrraktären Myelom umfasst sequenziellen Verlust von CD38, BCMA und GPRC5D
Wenn Krebs sogar die neuesten Medikamente überlistet
Das multiple Myelom, ein Krebs der Plasmazellen im Knochenmark, hat von einer Reihe neuer Wirkstoffe profitiert, darunter hochentwickelte immunbasierte Therapien. Dennoch erreichen manche Patienten inzwischen einen Zustand, in dem ihre Erkrankung allen verfügbaren Hauptwirkstoffklassen entkommt. Diese Studie untersucht genau dieses Endstadium – als „hepta‑refraktär“ bezeichnetes Myelom – um zu verstehen, wie der Krebs sich so vielen Therapien entzieht und welche Optionen Ärztinnen und Ärzte trotzdem noch finden könnten.
Ein neues extremes Stadium des Myeloms
Die Forschenden definieren hepta‑refraktäres Myelom als eine Erkrankung, die nicht mehr auf sieben zentrale Behandlungskategorien anspricht: zwei Arten von immunmodulierenden Tabletten, zwei Typen von Proteasom‑Hemmern, einen Antikörper gegen einen Oberflächenmarker namens CD38 sowie zwei neuere Immuntherapien, die auf die Ziele BCMA und GPRC5D gerichtet sind. In einer Gruppe von 37 solchen Patienten, die an mehreren Zentren behandelt wurden, war das Überleben trotz intensiver Versorgung gering. Nachdem dieses Stadium erreicht war, lebten die Patienten im Mittel etwa 13 Monate, und jede neue „Salvage“-Therapielinie hielt die Krankheit im Durchschnitt nur rund drei Monate in Schach. Die Ergebnisse variierten jedoch: Einige wenige Personen schnitten deutlich besser ab, was darauf hindeutet, dass die zugrunde liegende Biologie nicht in jedem Fall gleich ist.
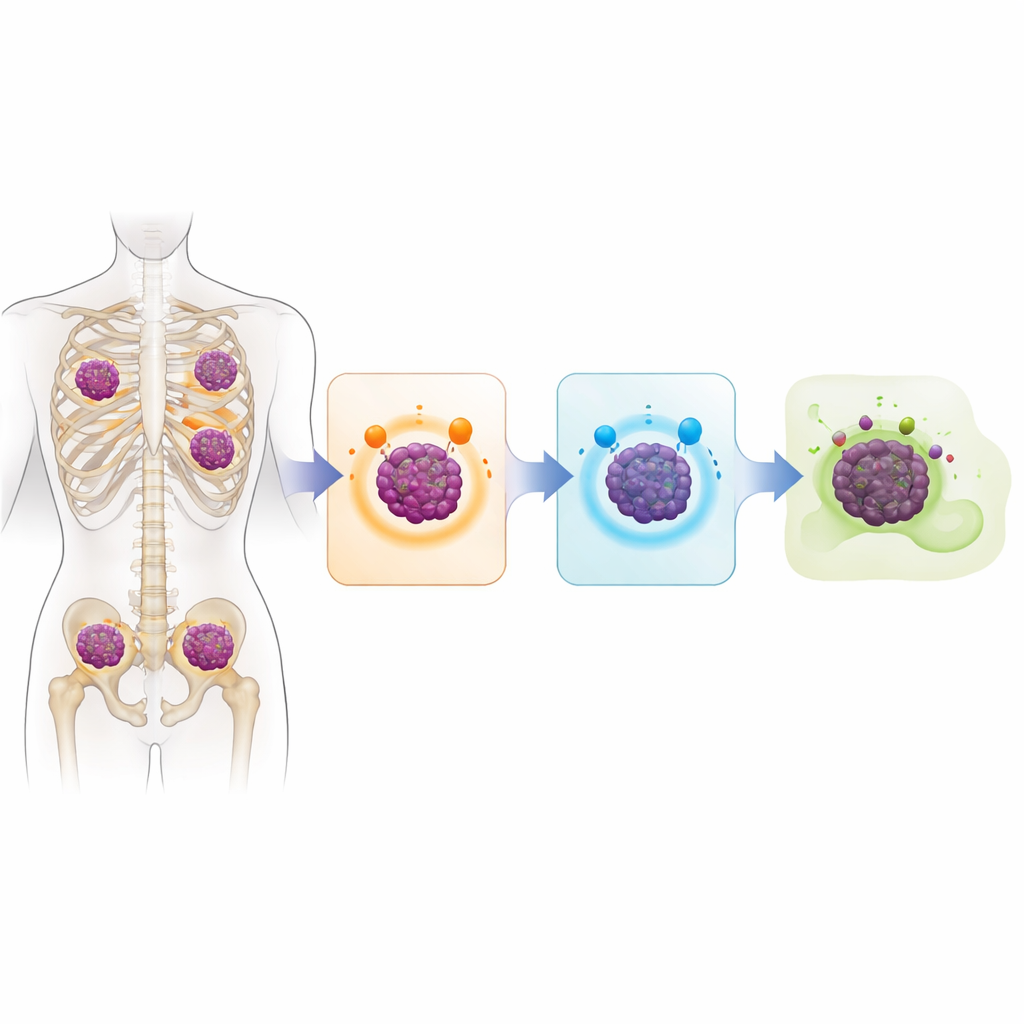
Ein Krebsgenom voller Warnsignale
Um zu sehen, was diese Tumoren unterscheidet, nutzte das Team die Ganzgenomsequenzierung, eine Methode, die praktisch die gesamte DNA eines Tumors liest. Bei 17 Patienten mit verfügbaren Proben fanden sie stark beschädigte und umstrukturierte Genome mit zahlreichen Treffern in klassischen Schutzgenen, die normalerweise das Zellwachstum bremsen oder den Zelltod auslösen. Häufig betroffene Regionen umfassten TP53 und CDKN2C sowie andere, die oft mit besonders aggressiver Erkrankung in Verbindung stehen. Viele dieser schweren Veränderungen traten in Tumoren auf, die sich außerhalb des Knochenmarks in Weichteile ausgebreitet hatten, was zum schnellen Verlauf der Erkrankung passte. Die DNA‑Muster trugen zudem charakteristische „Narben“ vergangener Therapien — etwa Veränderungen, die mit dem Chemotherapeutikum Melphalan assoziiert sind — und zeigten, dass Jahre der Behandlung die Evolution des Krebses geprägt hatten.
Wie Tumorzellen ihre Ziele ablegen
Die zentrale Frage war, wie Myelomzellen für moderne immunbasierte Medikamente unsichtbar werden, die darauf ausgelegt sind, bestimmte Moleküle auf der Zelloberfläche zu erkennen. Die Studie zeigt, dass Tumorzellen in vielen Fällen einfach aufhören, diese Moleküle zu produzieren. Bei etwa 40 Prozent der sequenzierten Patienten war das BCMA‑Gen auf beiden Chromosomenkopien ausgeschaltet, oft durch eine vollständige Deletion. Ungefähr ein Drittel wies ähnliche doppelte Schäden am GPRC5D‑Gen auf, meist durch eine Kombination aus Deletionen und kleinen schädigenden Mutationen. Einige Patienten verloren auch CD38. Fast ein Drittel der analysierten Gruppe hatte sowohl BCMA als auch GPRC5D verloren, sodass die Tumoren die genau jenen Ziele nicht mehr zeigten, die für mehrere der derzeit stärksten Therapien erforderlich sind.
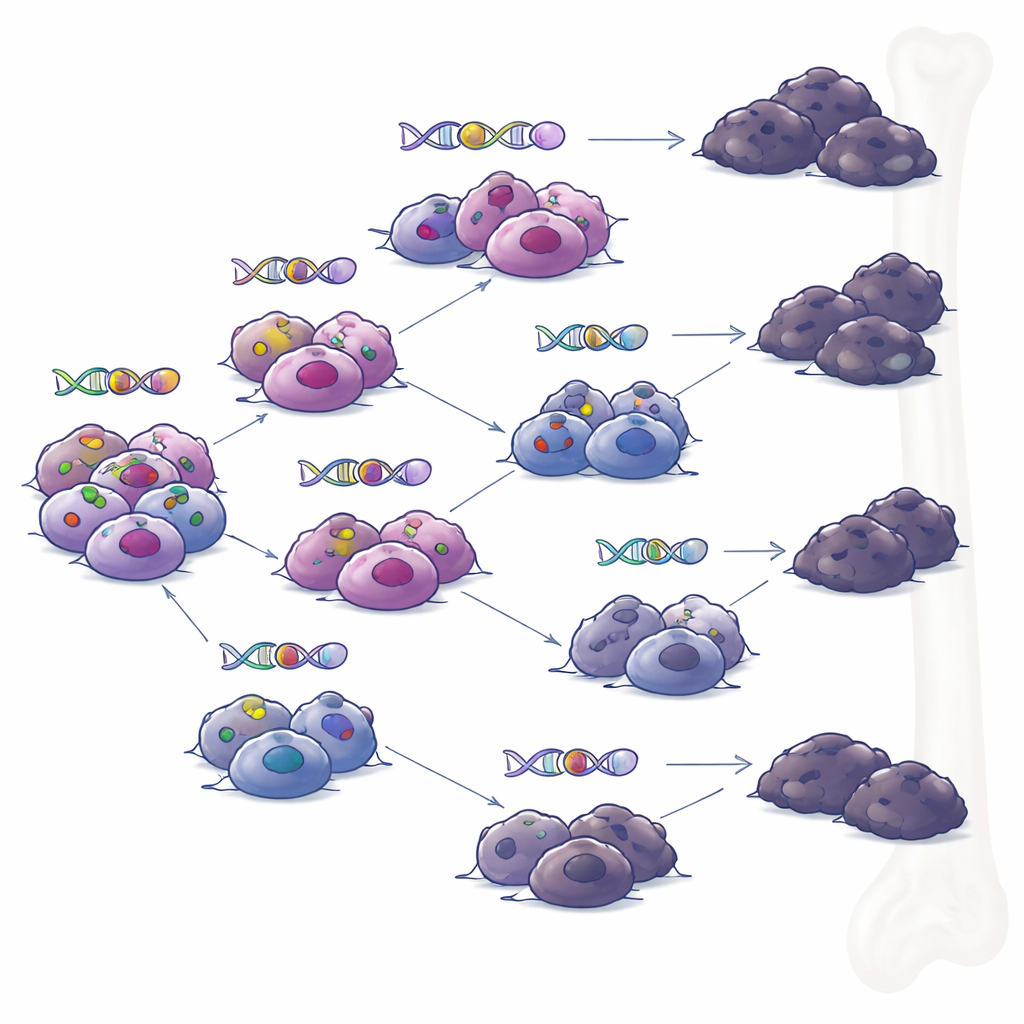
Verzweigte Pfade statt eines einzigen abtrünnigen Klons
Als das Team Proben untersuchte, die zu unterschiedlichen Zeitpunkten von denselben Patienten entnommen worden waren, rekonstruierten sie die Stammbäume der Tumoren. Statt eines einzelnen dominanten Klons, der kontinuierlich Veränderungen akkumuliert, sahen sie verzweigte Evolution: mehrere verwandte Untergruppen von Zellen, die sich aufspalteten und im Laufe der Zeit unterschiedliche Mutationensets erwarben. Unter dem Druck gezielter Immuntherapien entwickelten mehrere Zweige unabhängig voneinander Mechanismen, um BCMA oder GPRC5D zu verlieren. Dieses Muster legt nahe, dass selbst wenn eine Behandlung scheinbar zu einer tiefen Remission führt, kleine Nischen genetisch vielfältiger Zellen überdauern können und später einen Rückfall auslösen — jeweils mit eigenen Kombinationen von Resistenzstrategien.
Tiefere Tests nutzen, um zweite Chancen zu steuern
Weil die Gen-Sequenzierung nur die DNA erfasst, nutzten die Forschenden zusätzlich die Immunhistochemie, eine Färbemethode, die zeigt, ob das BCMA‑Protein tatsächlich auf Tumorzellen vorhanden ist. Jeder Tumor, bei dem beide BCMA‑Genkopien verloren waren, zeigte auch einen vollständigen Verlust des BCMA‑Proteins, aber einige Tumoren ohne offensichtliche Gendefekte wiesen ebenfalls wenig oder kein BCMA an der Oberfläche auf, was auf zusätzliche, subtilere Resistenzmechanismen hindeutet. Entscheidend ist: In einer kleinen Patientengruppe, die zuvor BCMA‑gerichtete Behandlungen erhalten hatte, sprachen diejenigen, deren Tumoren das BCMA‑Gen behielten und noch mindestens etwas BCMA‑Protein zeigten, oft wieder an, wenn sie mit einer anderen BCMA‑gerichteten CAR‑T‑Zelltherapie erneut behandelt wurden. Im Gegensatz dazu profitierten Patienten, deren Tumoren BCMA vollständig verloren hatten, nicht von einer solchen Wiederbehandlung.
Was das für Patienten und die zukünftige Versorgung bedeutet
Für Menschen mit Myelom vermittelt diese Studie eine zugleich ernüchternde und hoffnungsvolle Botschaft. Einerseits können sich einige Tumoren zu einem hochgradig medikamentenresistenten Zustand entwickeln, indem sie systematisch genau jene Marker ablegen, auf die fortschrittliche Immuntherapien angewiesen sind. Andererseits können detaillierte Tests von Tumor‑DNA und Proteinmarkern offenbaren, welche Ziele noch vorhanden sind, und so helfen, sinnlose, nebenwirkungsreiche Behandlungen zu vermeiden, wenn ein Ziel verloren ist. Die Autorinnen und Autoren plädieren dafür, breit angelegte genomische Analysen mit färbungsbasierten Tests zu kombinieren und als Teil der Versorgung von Patienten mit sehr fortgeschrittenem Myelom zu etablieren. Solche Ansätze könnten Patienten besser zu Wiederbehandlungsstrategien führen, die noch Aussicht auf Erfolg haben, und die Suche nach neuen Therapien leiten, die nicht von einem einzelnen, leicht verlierbaren Ziel abhängig sind.
Zitation: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Schlüsselwörter: multiples Myelom, Therapieresistenz, Immuntherapie, Antigenverlust, genomische Profilierung