Clear Sky Science · pt
A evolução para mieloma hepta-refratário envolve perda sequencial de CD38, BCMA e GPRC5D
Quando o câncer vence até os medicamentos mais novos
O mieloma múltiplo, um câncer das células plasmáticas na medula óssea, beneficiou-se de uma onda de medicamentos novos, incluindo tratamentos imunológicos sofisticados. Ainda assim, alguns pacientes chegam agora a um estágio em que a doença escapou de todos os principais tipos de drogas disponíveis. Este estudo examina de perto esse estágio final — chamado de mieloma “hepta‑refratário” — para entender como o câncer evolui para evitar tantas terapias e explorar como os médicos ainda podem encontrar opções úteis.
Um novo estágio extremo do mieloma
Os pesquisadores definem mieloma hepta‑refratário como a doença que não responde mais a sete categorias-chave de tratamento: dois tipos de fármacos imunomoduladores orais, dois tipos de inibidores do proteassoma, um anticorpo contra um marcador de superfície chamado CD38 e duas imunoterapias mais recentes direcionadas a alvos conhecidos como BCMA e GPRC5D. Em um grupo de 37 pacientes desse tipo tratados em vários centros, a sobrevida foi baixa apesar dos cuidados intensivos. Após alcançar esse estágio, os pacientes viveram, em média, cerca de 13 meses, e cada nova linha de terapia de “salvamento” conteve a doença por apenas cerca de três meses. Ainda assim, os desfechos variaram: alguns indivíduos foram notavelmente melhores, sugerindo que a biologia subjacente não é a mesma em todos os casos.
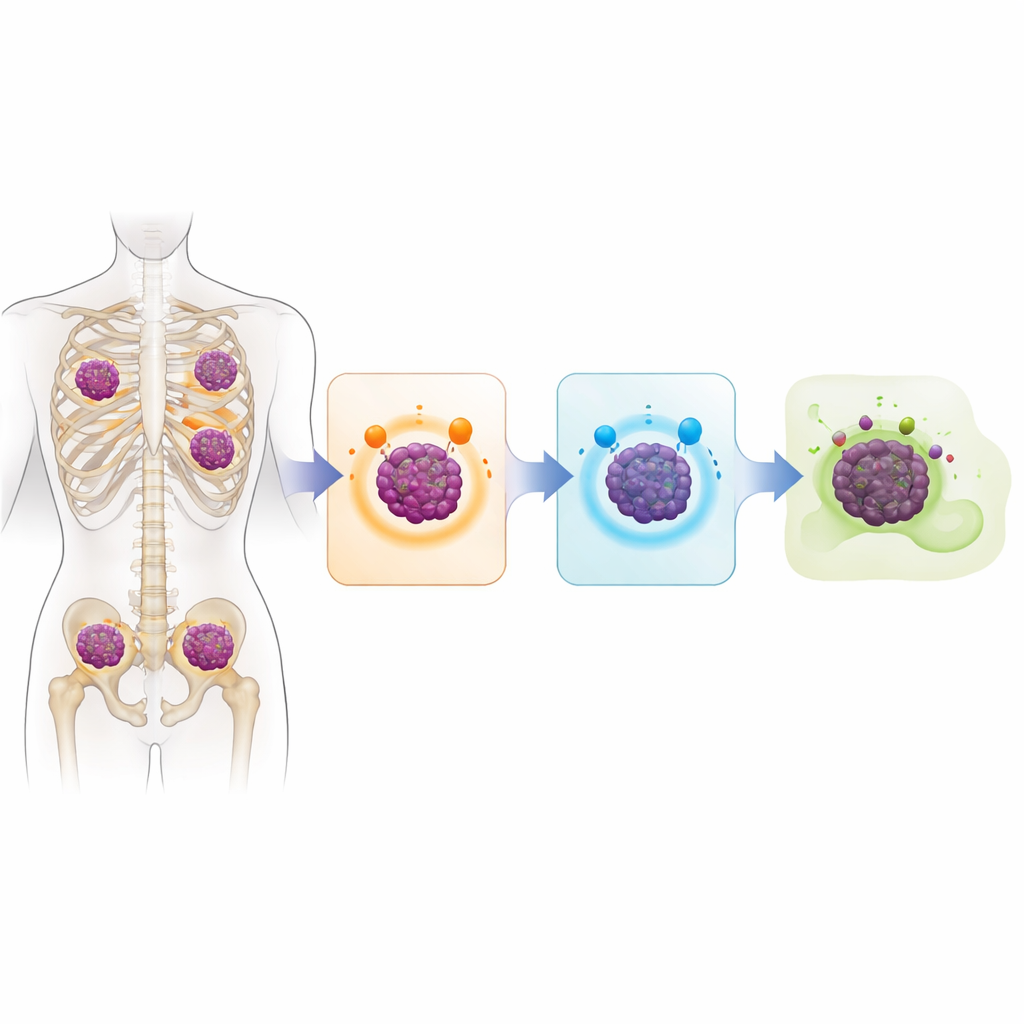
Um genoma do câncer cheio de sinais de alerta
Para ver o que diferenciava esses cânceres, a equipe usou sequenciamento do genoma inteiro, uma técnica que lê essencialmente todo o DNA de um tumor. Em 17 pacientes com amostras disponíveis, eles encontraram genomas muito danificados e rearranjados com muitos impactos em genes de salvaguarda clássicos que normalmente contêm o crescimento celular ou desencadeiam a morte celular. Áreas problemáticas comuns incluíam TP53 e CDKN2C, entre outros frequentemente ligados a doenças especialmente agressivas. Muitas dessas alterações severas apareceram em tumores que haviam se espalhado fora da medula óssea para tecidos moles, condizendo com a doença de progressão rápida dos pacientes. Os padrões de DNA também carregavam “cicatrizes” típicas de tratamentos passados — como alterações associadas ao agente quimioterápico melfalano — mostrando que anos de terapia moldaram a evolução do câncer.
Como as células tumorais descartam seus alvos
A questão central era como as células do mieloma se tornam invisíveis às drogas imunológicas modernas, projetadas para reconhecer moléculas específicas na superfície celular. O estudo mostra que, em muitos casos, as células tumorais simplesmente deixam de produzir essas moléculas. Em cerca de 40% dos pacientes sequenciados, o gene do BCMA foi inativado em ambas as cópias cromossômicas, frequentemente por deleção direta. Aproximadamente um terço apresentou danos duplos semelhantes afetando GPRC5D, geralmente por uma mistura de deleções e pequenas mutações deletérias. Alguns pacientes também perderam CD38. Quase um terço do grupo analisado havia perdido tanto BCMA quanto GPRC5D, o que significa que já não exibiam os próprios alvos necessários para que várias das terapias mais potentes de hoje funcionem.
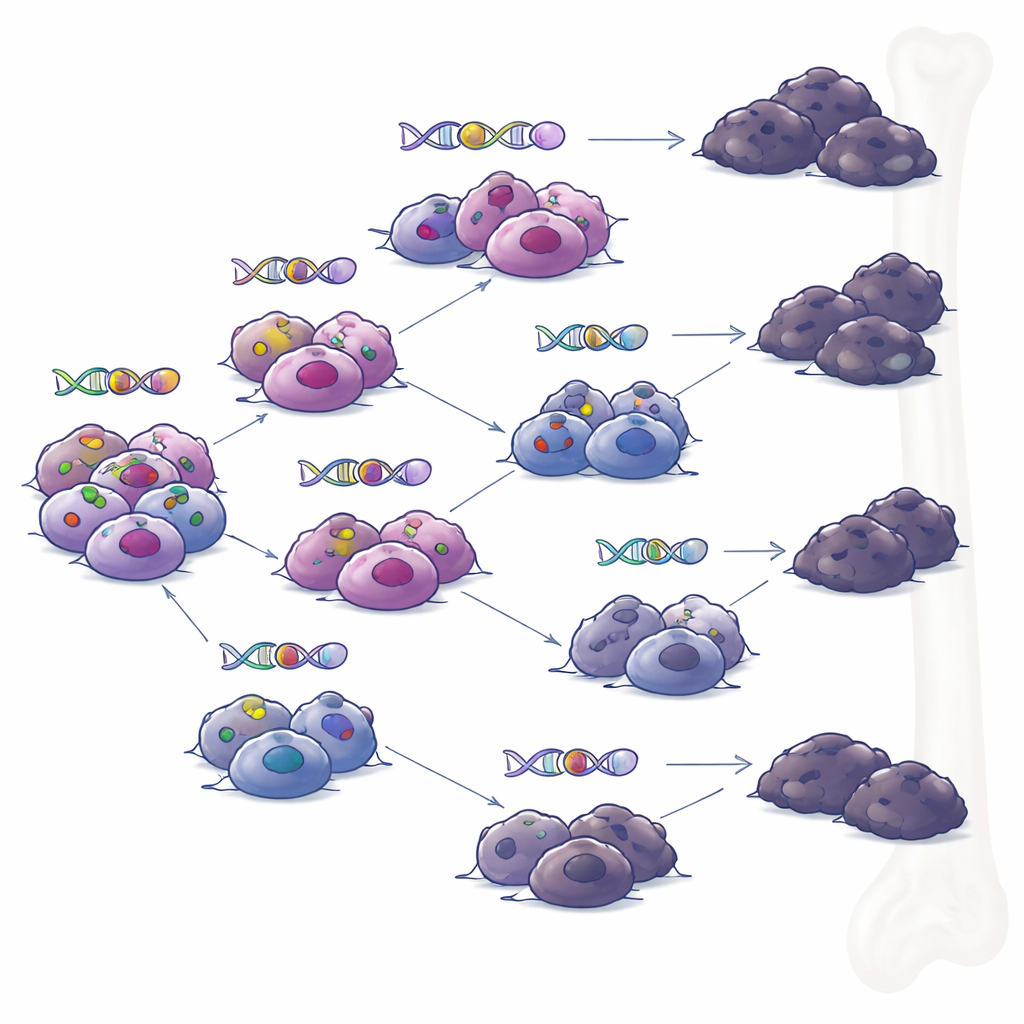
Caminhos ramificados em vez de um único clone rebelde
Quando a equipe examinou amostras coletadas dos mesmos pacientes em momentos diferentes, eles reconstruíram as árvores genealógicas dos tumores. Em vez de um único clone dominante acumulando mudanças de forma contínua, observaram evolução ramificada: vários subgrupos celulares relacionados que divergiram e adquiriram diferentes conjuntos de mutações ao longo do tempo. Sob pressão de terapias imunológicas direcionadas, múltiplos ramos desenvolveram independentemente maneiras de perder BCMA ou GPRC5D. Esse padrão sugere que, mesmo quando o tratamento parece produzir uma remissão profunda, pequenos bolsões de células geneticamente diversas podem persistir e mais tarde provocar recaída, cada um com sua própria combinação de truques de resistência.
Usando testes mais aprofundados para orientar novas chances
Como o sequenciamento genético captura apenas o DNA, os pesquisadores também usaram imuno-histoquímica, um método de coloração que mostra se a proteína BCMA está realmente presente nas células tumorais. Todo tumor com perda de ambas as cópias do gene BCMA mostrou perda completa da proteína BCMA, mas alguns tumores sem dano genético óbvio também apresentaram pouco ou nenhum BCMA em sua superfície, implicando mecanismos de resistência adicionais mais sutis. Crucialmente, em um pequeno conjunto de pacientes que haviam recebido anteriormente tratamento direcionado ao BCMA, aqueles cujos tumores ainda apresentavam o gene BCMA e mostravam ao menos alguma proteína BCMA frequentemente responderam novamente quando retratados com outra terapia CAR T dirigida ao BCMA. Em contraste, pacientes cujos tumores haviam perdido completamente o BCMA não se beneficiaram desse retratamento.
O que isso significa para pacientes e cuidados futuros
Para pessoas vivendo com mieloma, este estudo destaca uma mensagem ao mesmo tempo sóbria e esperançosa. Por um lado, alguns tumores podem evoluir para um estado altamente resistente a drogas ao descartar sistematicamente os marcadores em que as terapias imunológicas avançadas se apoiam. Por outro, testes detalhados do DNA tumoral e de marcadores proteicos podem revelar quais alvos permanecem e ajudar a evitar tratamentos fúteis e com efeitos colaterais quando um alvo desapareceu. Os autores defendem que combinar análises genômicas amplas com testes baseados em coloração deveria fazer parte do cuidado de pacientes com mieloma muito avançado. Essas abordagens podem alinhar melhor as pessoas a estratégias de retratamento que ainda têm chance de funcionar, enquanto orientam a busca por novas terapias que não dependam de um único alvo facilmente perdido.
Citação: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Palavras-chave: mieloma múltiplo, resistência ao tratamento, imunoterapia, perda de antígeno, perfil genômico