Clear Sky Science · ru
Эволюция до гепта‑рефрактерной миеломы включает последовательную потерю CD38, BCMA и GPRC5D
Когда рак перехитряет даже новейшие препараты
Множественная миелома, рак плазматических клеток костного мозга, выиграла от волны новых препаратов, включая сложные иммунные подходы. Тем не менее некоторые пациенты доходят до стадии, когда их болезнь ускользнула от всех основных доступных типов терапии. В этом исследовании подробно рассматривают эту конечную стадию — так называемую «гепта‑рефрактерную» миелому — чтобы понять, как опухоль эволюционирует и ухитряется избежать столь многих методов лечения, и изучить, какие варианты остаются для врачей.
Новая крайняя стадия миеломы
Исследователи определяют гепта‑рефрактерную миелому как болезнь, не отвечающую на семь ключевых категорий лечения: два типа иммуномодулирующих пероральных препаратов, два класса ингибиторов протеасомы, антитело против поверхностного маркера CD38 и два новых иммунных подхода, нацеленных на BCMA и GPRC5D. В когорте из 37 таких пациентов, пролеченных в нескольких центрах, выживаемость была низкой, несмотря на интенсивную терапию. После достижения этой стадии пациенты в среднем жили примерно 13 месяцев, а каждая очередная линия «спасительного» лечения сдерживала болезнь только около трёх месяцев. В то же время результаты варьировали: некоторые пациенты проявляли заметно лучшее течение, что говорит о том, что биология болезни различается у разных людей.
Опухолевый геном, полный тревожных знаков
Чтобы понять, что отличает эти опухоли, команда применила секвенирование всего генома — метод, читающий практически всю ДНК опухоли. У 17 пациентов с доступными образцами они обнаружили сильно повреждённые и перестроенные геномы с множеством поражений в классических генах‑сторожах, которые обычно сдерживают рост клетки или запускают её гибель. Часто поражались TP53 и CDKN2C и другие области, связанные с особенно агрессивным течением. Многие из этих тяжёлых изменений встречались в опухолях, распространившихся за пределы костного мозга в мягкие ткани, что соответствовало быстрому прогрессированию болезни у пациентов. Шаблоны ДНК также содержали характерные «шрамы» от прошлых курсов лечения — например изменения, ассоциированные с химиопрепаратом мелфалан — показывая, что годами терапии формировалась эволюция рака.
Как опухолевые клетки теряют свои мишени
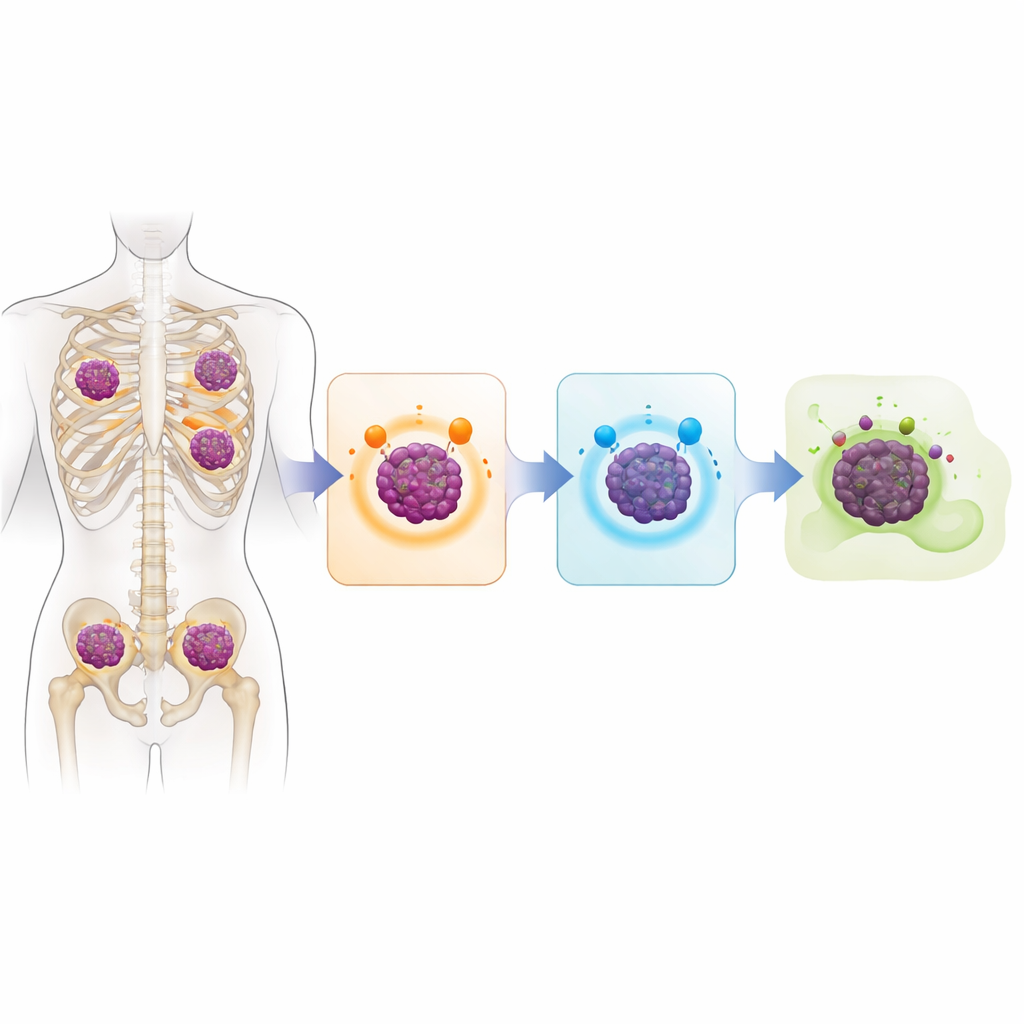
Ключевой вопрос заключался в том, как клетки миеломы становятся невидимыми для современных иммунных препаратов, которые распознают специфические молекулы на поверхности клетки. Исследование показывает, что во многих случаях опухолевые клетки просто перестают синтезировать эти молекулы. Примерно у 40 % секвенированных пациентов ген BCMA был инактивирован в обеих копиях хромосомы, часто вследствие полной делеции. Около трети имели аналогичные двуаллельные поражения GPRC5D, обычно в результате сочетания делеций и небольших повреждающих мутаций. У некоторых пациентов также пропадал CD38. Почти треть проанализированной группы утратила одновременно и BCMA, и GPRC5D, то есть больше не экспонировала те самые мишени, от которых зависят несколько из наиболее мощных современных терапий.
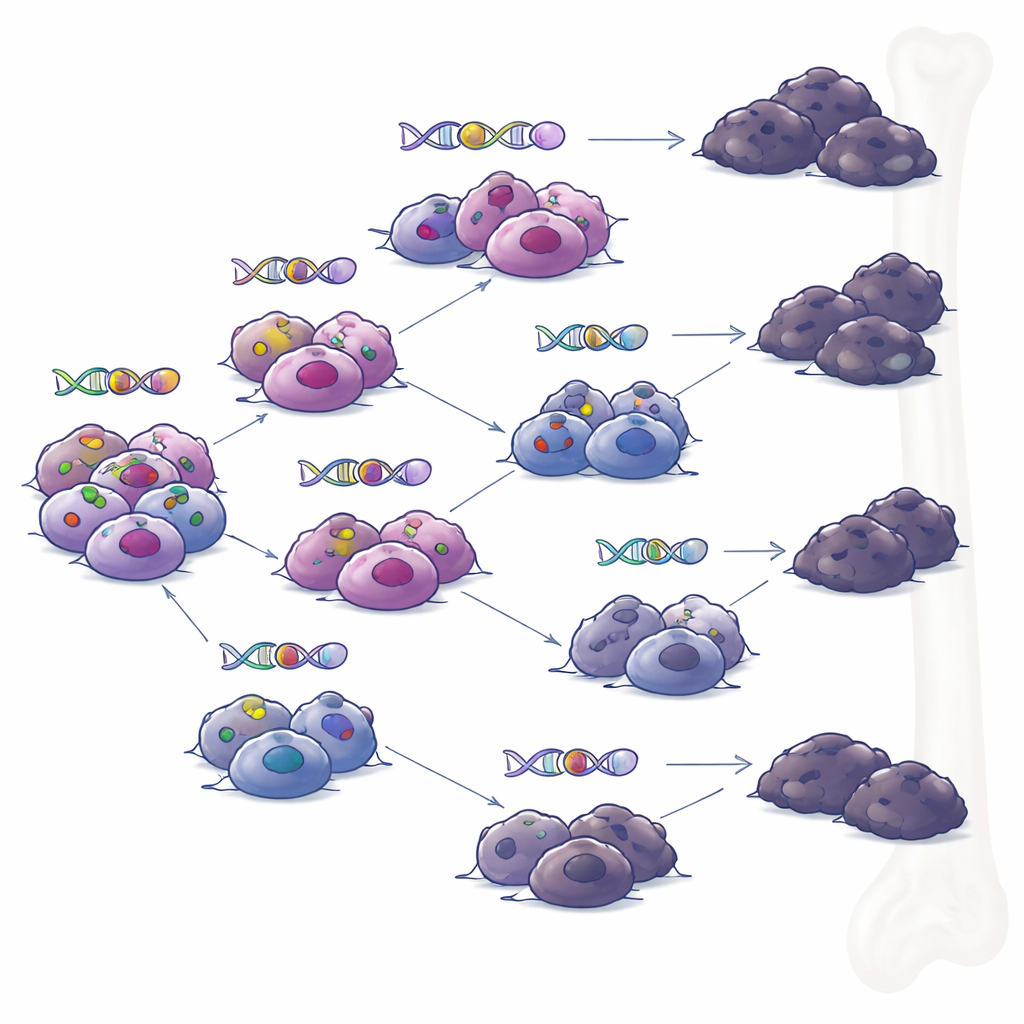
Разветвлённые пути вместо единственного злого клона
При анализе образцов, взятых у одних и тех же пациентов в разное время, команда восстановила «родословные» опухолей. Вместо одного доминирующего клона, постепенно накапливающего изменения, они увидели разветвлённую эволюцию: несколько родственных подгрупп клеток, которые расходились и со временем приобретали разные наборы мутаций. Под давлением таргетных иммунных терапий множество ветвей независимо разрабатывало способы утраты BCMA или GPRC5D. Этот паттерн указывает на то, что даже когда лечение вызывает глубокую ремиссию, небольшие очаги генетически разнообразных клеток могут выживать и затем приводить к рецидиву, каждая — со своим набором приёмов устойчивости.
Использование более глубокой диагностики для новых шансов
Поскольку секвенирование охватывает только ДНК, исследователи также применили иммуногистохимию — окрашивание, показывающее, присутствует ли белок BCMA на опухолевых клетках. Каждая опухоль с потерей обеих копий гена BCMA демонстрировала полное отсутствие белка BCMA, но некоторые опухоли без явных повреждений гена тоже имели мало или совсем не экспонировали BCMA на поверхности, что указывает на дополнительные, более тонкие механизмы устойчивости. Важно, что в небольшой группе пациентов, ранее получавших терапию, нацеленную на BCMA, те, в чьих опухолях ген BCMA сохранялся и присутствовал по крайней мере в некоторой степени на белковом уровне, часто снова отвечали на повторное лечение другой CAR‑Т‑терапией, нацеленной на BCMA. В то же время пациенты с полной утратой BCMA не получали пользы от такого повторного лечения.
Что это значит для пациентов и будущей практики
Для людей с миеломой это исследование несёт одновременно мрачное и обнадеживающее послание. С одной стороны, некоторые опухоли могут эволюционировать в сильно лекарственно‑устойчивое состояние, системно отказываясь от маркеров, на которых основаны современные иммунные терапии. С другой — детальное тестирование ДНК и белковых маркеров опухоли может показать, какие мишени ещё доступны, и помочь избежать бесполезных, с побочными эффектами, лечений, когда мишень утрачена. Авторы утверждают, что сочетание широкого геномного анализа с тестами на экспрессию белка должно войти в практику для пациентов с очень продвинутой миеломой. Такие подходы позволят лучше подбирать повторные стратегии лечения, которые ещё имеют шанс сработать, и направлять поиск новых терапий, не зависящих от одной легко утрачиваемой мишени.
Цитирование: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Ключевые слова: множественная миелома, устойчивость к лечению, иммунотерапия, потеря антигена, геномный профиль