Clear Sky Science · it
L’evoluzione verso il mieloma epta‑refrattario comporta la perdita sequenziale di CD38, BCMA e GPRC5D
Quando il cancro inganna anche i farmaci più nuovi
Il mieloma multiplo, un tumore delle plasmacellule nel midollo osseo, ha beneficiato di un’ondata di nuovi farmaci, comprese terapie immunitarie sofisticate. Tuttavia alcuni pazienti raggiungono oggi uno stadio in cui la loro malattia ha eluso tutti i principali tipi di farmaco disponibili. Questo studio esamina da vicino quello stadio terminale — chiamato “epta‑refrattario” — per capire come il tumore evolva fino a sfuggire a così tante terapie e per esplorare come i clinici possano ancora trovare opzioni utili.
Un nuovo stadio estremo del mieloma
I ricercatori definiscono il mieloma epta‑refrattario come una malattia che non risponde più a sette categorie chiave di trattamento: due tipi di farmaci immunomodulatori orali, due tipi di inibitori del proteasoma, un anticorpo contro un marcatore di superficie chiamato CD38 e due terapie immunitarie più recenti mirate a bersagli noti come BCMA e GPRC5D. In un gruppo di 37 pazienti trattati in diversi centri, la sopravvivenza è risultata scarsa nonostante cure intensive. Dopo aver raggiunto questo stadio, i pazienti vivevano in media circa 13 mesi, e ogni nuova linea di terapia di “salvataggio” teneva la malattia sotto controllo per solo circa tre mesi. Tuttavia, gli esiti variavano: alcuni individui andarono sensibilmente meglio, suggerendo che la biologia sottostante non è la stessa in tutti i casi.
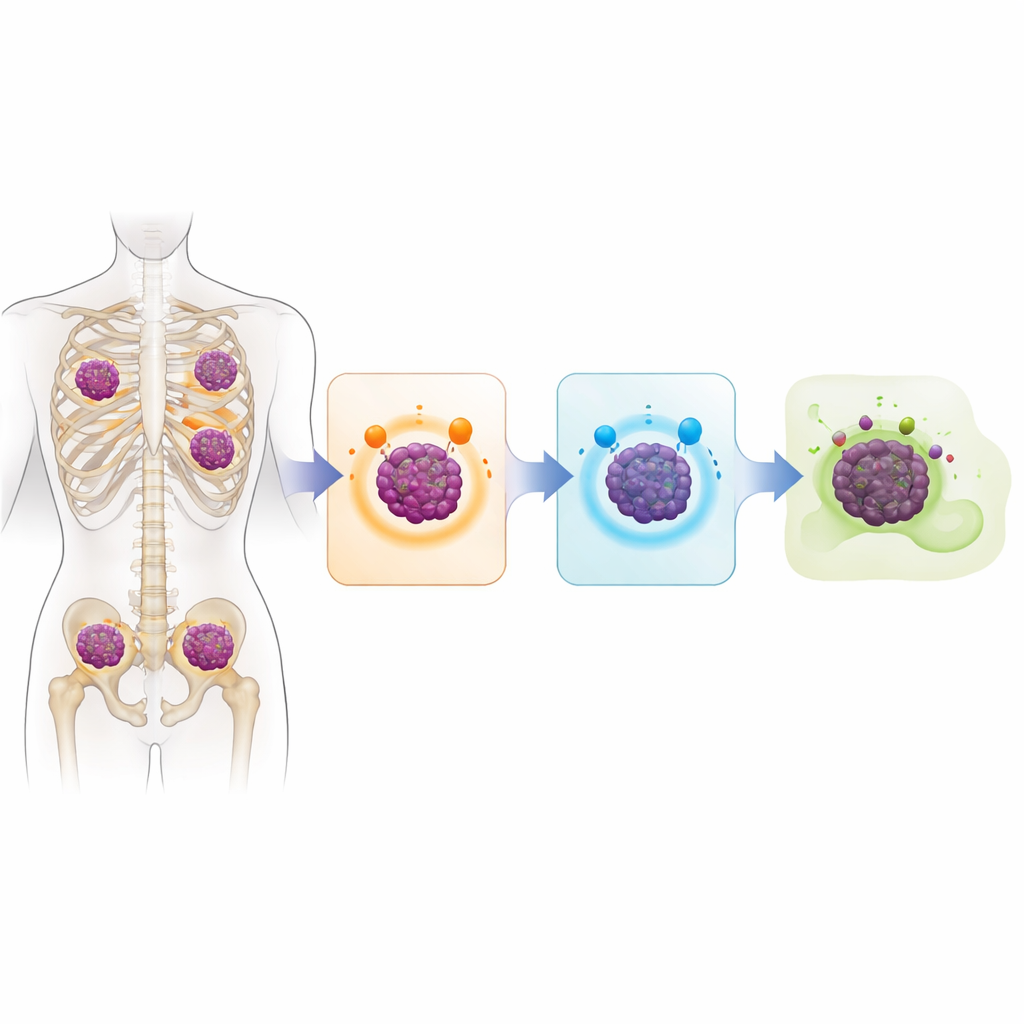
Un genoma tumorale pieno di segnali d’allarme
Per capire cosa distinguesse questi tumori, il team ha usato il sequenziamento dell’intero genoma, una tecnica che legge sostanzialmente tutto il DNA di un tumore. In 17 pazienti con campioni disponibili hanno trovato genomi altamente danneggiati e riorganizzati con molteplici colpi a geni di protezione classici che normalmente reprimono la crescita cellulare o innescano la morte cellulare. Aree problematiche comuni includevano TP53 e CDKN2C, fra gli altri spesso associati a malattie particolarmente aggressive. Molti di questi cambiamenti gravi sono comparsi in tumori che si erano diffusi al di fuori del midollo osseo nei tessuti molli, in linea con la rapida progressione della malattia nei pazienti. I modelli nel DNA portavano anche le “cicatrici” tipiche di trattamenti passati — come alterazioni associate al chemioterapico melphalan — mostrando che anni di terapia hanno plasmato l’evoluzione del cancro.
Come le cellule tumorali scotomizzano i loro bersagli
La questione centrale era come le cellule del mieloma diventino invisibili ai farmaci immunoterapici moderni, progettati per riconoscere molecole specifiche sulla superficie cellulare. Lo studio mostra che, in molti casi, le cellule tumorali semplicemente smettono di produrre queste molecole. In circa il 40 percento dei pazienti sequenziati, il gene per BCMA era inattivato su entrambe le copie del cromosoma, spesso tramite una delezione netta. Circa un terzo presentava colpi doppi simili che interessavano GPRC5D, di solito attraverso una combinazione di delezioni e piccole mutazioni dannose. Alcuni pazienti persero anche CD38. Quasi un terzo del gruppo analizzato aveva perso sia BCMA sia GPRC5D, il che significa che non esprimevano più i bersagli necessari per il funzionamento di molte delle terapie più potenti oggi disponibili.
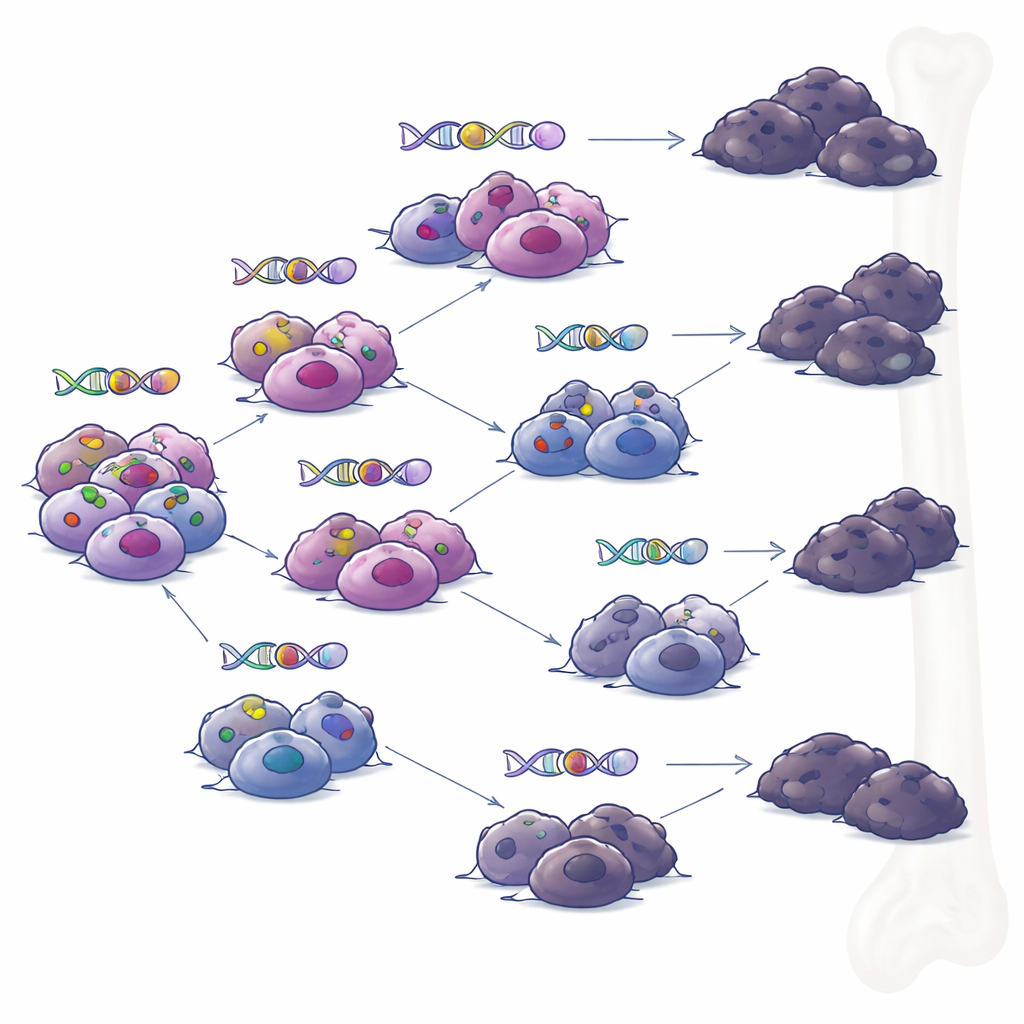
Ramificazioni evolutive piuttosto che un singolo clone fuorilegge
Quando il team ha esaminato campioni prelevati dagli stessi pazienti in momenti diversi, ha ricostruito gli alberi genealogici dei tumori. Invece di un singolo clone dominante che accumula progressivamente variazioni, hanno osservato un’evoluzione a rami: diversi sottogruppi correlati di cellule che si sono divisi e hanno acquisito insiemi differenti di mutazioni nel tempo. Sotto la pressione delle terapie immunitarie mirate, più rami hanno sviluppato indipendentemente modi per perdere BCMA o GPRC5D. Questo schema suggerisce che, anche quando il trattamento sembra ottenere una remissione profonda, piccole sacche di cellule geneticamente diverse possono persistere e poi innescare una ricaduta, ognuna con la propria combinazione di trucchi di resistenza.
Usare test più approfonditi per indirizzare seconde possibilità
Poiché il sequenziamento genico cattura solo il DNA, i ricercatori hanno anche usato l’immunoistochimica, un metodo di colorazione che mostra se la proteina BCMA è effettivamente presente sulle cellule tumorali. Ogni tumore con entrambe le copie del gene BCMA perse mostrava una perdita completa della proteina BCMA, ma alcuni tumori privi di danni genici evidenti mostravano ugualmente poco o nessun BCMA sulla loro superficie, implicando meccanismi di resistenza aggiuntivi e più sottili. Crucialmente, in un piccolo sottogruppo di pazienti che avevano già ricevuto trattamenti mirati a BCMA, coloro i cui tumori conservavano il gene BCMA e mostravano almeno una certa espressione della proteina spesso rispondevano nuovamente quando venivano trattati di nuovo con una terapia CAR T cellulare diretta contro BCMA. Al contrario, i pazienti i cui tumori avevano perso completamente BCMA non beneficiarono di tali ritreatments.
Cosa significa questo per i pazienti e per le cure future
Per le persone che convivono con il mieloma, questo studio sottolinea un messaggio al tempo stesso scoraggiante e speranzoso. Da un lato, alcuni tumori possono evolvere fino a uno stato altamente resistente ai farmaci scartando sistematicamente i marcatori su cui si basano le terapie immunitarie avanzate. Dall’altro, test dettagliati sul DNA tumorale e sui marcatori proteici possono rivelare quali bersagli restano e aiutare a evitare trattamenti inutili e carichi di effetti collaterali quando un bersaglio è scomparso. Gli autori sostengono che combinare un’analisi genomica ampia con test basati sulla colorazione dovrebbe diventare parte della cura per i pazienti con mieloma molto avanzato. Tali approcci potrebbero meglio abbinare i pazienti a strategie di ritratamento che hanno ancora chance di funzionare, guidando al contempo la ricerca di nuove terapie che non dipendano da un singolo bersaglio facilmente eliminabile.
Citazione: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Parole chiave: mieloma multiplo, resistenza al trattamento, immunoterapia, perdita dell’antigene, profilazione genomica