Clear Sky Science · tr
Hepta-refrakter miyelom evrimi CD38, BCMA ve GPRC5D’nin ardışık kaybını içeriyor
Kanser En Yeni İlaçları Bile Nasıl Akla Getiriyor?
Kemik iliğindeki plazma hücrelerinin kanseri olan multipl miyelom, ileri düzey bağışıklık temelli tedaviler de dahil olmak üzere bir dizi yeni ilaçtan yarar gördü. Yine de bazı hastalar artık mevcut ana ilaç türlerinin tamamından kaçmış bir evreye ulaşıyor. Bu çalışma, bu son evre—"hepta‑refrakter" miyelom—üzerine odaklanarak kanserin bu kadar çok terapiyi nasıl atlattığını anlamaya ve hekimlerin hâlâ işe yarayabilecek seçenekleri nasıl bulabileceğini keşfetmeye çalışıyor.
Miyelomda Yeni Bir Aşırı Evre
Araştırmacılar hepta‑refrakter miyelomu şu yedi ana tedavi kategorisine artık yanıt vermeyen hastalık olarak tanımlıyor: iki çeşit immünomodülatör hap, iki tür proteazom inhibitörü, yüzey belirteci CD38’e karşı bir antikor ve BCMA ile GPRC5D olarak bilinen hedeflere yönelik iki daha yeni immün terapi. Birkaç merkezde tedavi edilen 37 hastalık bir grupta, yoğun bakıma rağmen sağkalım kötüydü. Bu evreye ulaştıktan sonra hastalar ortalama yaklaşık 13 ay yaşadı ve her yeni ‘kurtarma’ tedavi hattı hastalığı genellikle yalnızca yaklaşık üç ay kontrol altında tuttu. Yine de sonuçlar farklılık gösteriyordu: birkaç hasta belirgin şekilde daha iyi durumda olup, altta yatan biyolojinin her vakada aynı olmadığını düşündürüyor.
Uyarı İşaretleriyle Dolu Bir Kanser Genomu
Bu kanserleri farklı kılanı görmek için ekip, tümörün neredeyse tüm DNA’sını okuyan tüm genom dizilemesini kullandı. Mevcut örnekleri olan 17 hastada, hücre büyümesini sınırlayan veya hücre ölümünü tetikleyen klasik koruyucu genlere çok sayıda darbeyle birlikte ağır hasarlı ve yeniden düzenlenmiş genomlar bulundu. Ortak sorun alanları arasında TP53 ve CDKN2C vardı; bunlar sıklıkla özellikle agresif hastalıkla ilişkilendirilen diğer bölgelerle birlikte görüldü. Bu ağır değişiklikların birçoğu kemiğin dışına, yumuşak dokulara yayılan tümörlerde ortaya çıktı ve hastaların hızlı seyreden hastalığıyla örtüştü. DNA modelleri ayrıca geçmiş tedavilere ait belirgin “izler” taşıyordu—melphalan gibi kemoterapi ilaçlarıyla ilişkilendirilen değişiklikler gibi—yıllarca süren tedavinin kanserin evrimini şekillendirdiğini gösteriyordu.
Tümör Hücreleri Hedeflerini Nasıl Kaybediyor?
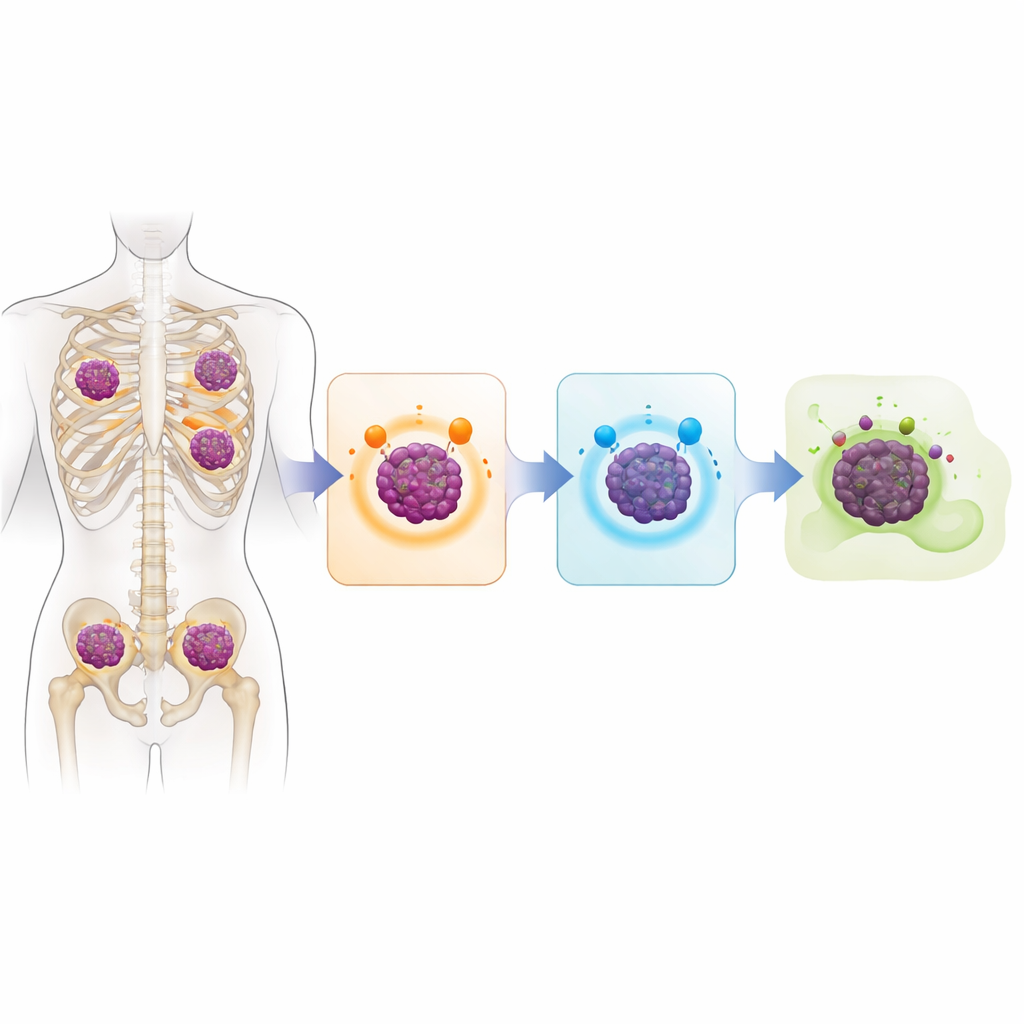
Merkezi soru, miyelom hücrelerinin belirli yüzey moleküllerini tanımaya yönelik modern immün temelli ilaçlara nasıl görünmez hâle geldiğiydi. Çalışma, birçok durumda tümör hücrelerinin bu molekülleri üretmeyi basitçe bırakıldığını gösteriyor. Dizilenen hastaların yaklaşık yüzde 40’ında BCMA geninin kromozomun her iki kopyasında da yok edildiği, çoğunlukla açıkça silinme yoluyla olduğu bulundu. Yaklaşık üçte birinde benzer çift darbeler GPRC5D’yi etkiledi; genellikle silinmelerle ve küçük zarar verici mutasyonların bir karışımıyla. Bazı hastalarda CD38 de kayboldu. Analiz edilen grubun neredeyse üçte birinde hem BCMA hem de GPRC5D kaybı vardı; bu da onların günümüzün en güçlü terapilerinden bazıları için gereken hedefleri artık sergilemedikleri anlamına geliyordu.
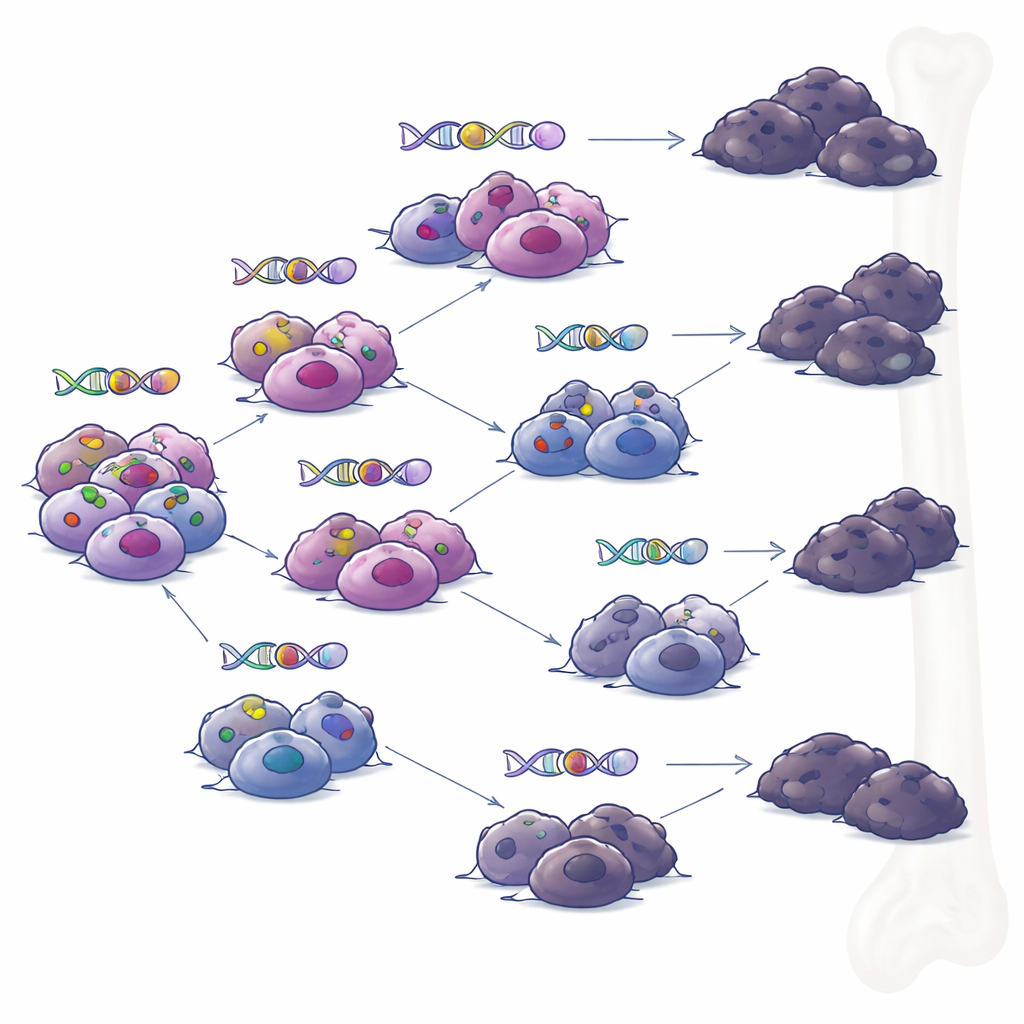
Tek Bir Asi Klondan Çok Dallanmış Yollar
Araştırma ekibi aynı hastalardan farklı zamanlarda alınan örnekleri incelediğinde tümörlerin soy ağaçlarını yeniden yapılandırdı. Değişiklikleri sürekli birikmiş tek bir baskın kloğun yerine, dallanan evrim görüldü: zamanla farklı mutasyon kümeleri edinen birkaç ilgili alt hücre grubu. Hedefe yönelik immün terapilerin baskısı altında, birden fazla dal bağımsız olarak BCMA veya GPRC5D’yi kaybetme yolları geliştirdi. Bu desen, tedavi derin bir remisyona yol açmış gibi görünse bile, genetik olarak çeşitli küçük hücre ceplerinin kalmaya devam edip daha sonra her biri kendi direnç hileleriyle nüksleri başlatabileceğini düşündürüyor.
Daha Derin Testleri İkinci Şanslara Yönlendirmek
Gen dizilemesinin yalnızca DNA’yı yakaladığı düşünüldüğünde, araştırmacılar BCMA proteininin gerçekten tümör hücrelerinde var olup olmadığını gösteren bir boyama yöntemi olan immünohistokimyayı da kullandı. Her iki BCMA gen kopyasını kaybetmiş tüm tümörlerde BCMA proteininde tam kayıp görüldü; ancak bazı tümörler belirgin gen hasarı olmasa bile yüzeylerinde çok az veya hiç BCMA bulunmuyordu; bu da ek, daha ince direnç mekanizmalarının varlığını ima ediyordu. Kritik olarak, daha önce BCMA’ya yönelik tedavi almış küçük bir hasta grubunda, tümörlerinde BCMA geni hâlâ bulunan ve en azından biraz BCMA proteini gösterenler genellikle başka bir BCMA‑yönelimli CAR T‑hücresiyle yeniden tedavi edildiğinde tekrar yanıt verdi. Buna karşılık, tümörü BCMA’yı tamamen kaybetmiş olan hastalar bu tür yeniden tedaviden fayda görmedi.
Bu Hastalar ve Gelecekteki Bakım İçin Ne Anlama Geliyor?
Miyelomla yaşayan insanlar için bu çalışma hem karamsar hem de umut verici bir mesajı vurguluyor. Bir yandan bazı tümörler, gelişmiş immün terapilerin dayandığı belirteçleri sistematik olarak elden çıkararak son derece ilaç‑dirençli bir duruma evrilebilir. Öte yandan, tümör DNA’sı ve protein belirteçlerinin ayrıntılı testleri hangi hedeflerin hâlâ mevcut olduğunu ortaya koyabilir ve bir hedef kaybolduğunda faydasız, yan etki yüklü tedavilerden kaçınmaya yardımcı olabilir. Yazarlar, geniş genomik analizlerin boyama temelli testlerle birleştirilmesinin çok ileri miyelomlu hastaların bakımının bir parçası olması gerektiğini savunuyor. Bu yaklaşımlar, insanları hâlâ işe yarama şansı olan yeniden tedavi stratejileriyle daha iyi eşleştirebilir ve kolayca kaybedilen tek bir hedefe dayanmayan yeni terapilerin aranmasına rehberlik edebilir.
Atıf: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Anahtar kelimeler: multipl miyelom, tedavi direnci, immünoterapi, antijen kaybı, genomik profilleme