Clear Sky Science · sv
Evolutionen till hepta‑refraktärt myelom innebär sekventiell förlust av CD38, BCMA och GPRC5D
När cancer överlistar även de nyaste läkemedlen
Multipelt myelom, en cancer i plasmaceller i benmärgen, har gynnats av en våg av nya läkemedel, inklusive sofistikerade immunbaserade behandlingar. Ändå når vissa patienter numera ett stadium där deras sjukdom har undkommit varje större tillgänglig läkemedelstyp. Denna studie undersöker noggrant det slutstadiet — kallat ”hepta‑refraktärt” myelom — för att förstå hur cancern utvecklas för att undvika så många terapier och för att utforska hur läkare ändå kan hitta användbara alternativ.
En ny extrem fas av myelom
Forskarna definierar hepta‑refraktärt myelom som sjukdom som inte längre svarar på sju viktiga behandlingskategorier: två typer av immunmodulerande tabletter, två typer av proteasomhämmare, en antikropp mot en ytmarkör kallad CD38 samt två nyare immunterapier riktade mot målen BCMA och GPRC5D. I en grupp om 37 sådana patienter som behandlats vid flera centra var överlevnaden dålig trots intensiv vård. Efter att ha nått detta stadium levde patienterna i genomsnitt omkring 13 månader, och varje ny linje av ”räddnings”behandling höll sjukdomen tillbaka i bara omkring tre månader. Resultaten varierade dock: några individer klarade sig betydligt bättre, vilket antyder att den bakomliggande biologin inte är densamma i alla fall.
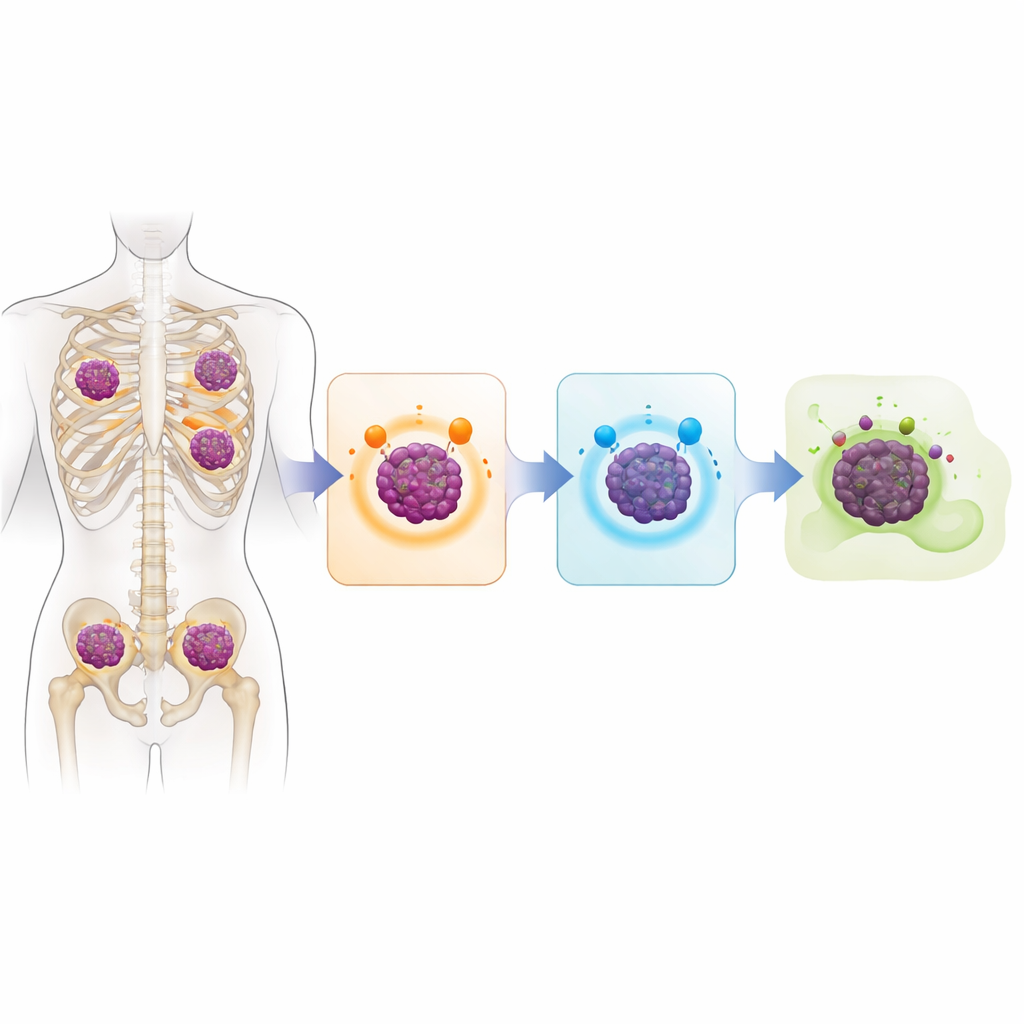
Ett cancergenom fullt av varningstecken
För att se vad som särskilde dessa cancerformer använde teamet helgenomsekvensering, en teknik som avläser i princip all DNA i en tumör. Hos 17 patienter med tillgängliga prov fann de kraftigt skadade och omarrangerade genom med många träffar mot klassiska skyddsgener som normalt begränsar celltillväxt eller utlöser celldöd. Vanliga problemområden inkluderade TP53 och CDKN2C, bland andra som ofta kopplas till särskilt aggressiv sjukdom. Många av dessa svåra förändringar förekom i tumörer som spridit sig utanför benmärgen till mjukvävnad, vilket stämmer med patienternas snabbrörliga sjukdom. DNA‑mönstren bar också tydliga ”ärr” av tidigare behandlingar — såsom förändringar associerade med cytostatikan melphalan — vilket visar att åratal av behandling format cancerutvecklingen.
Hur tumörceller tappar sina mål
Huvudfrågan var hur myelomceller blir osynliga för moderna immunbaserade läkemedel som är designade för att känna igen specifika molekyler på cellens yta. Studien visar att tumörceller i många fall helt enkelt slutar tillverka dessa molekyler. I ungefär 40 procent av de sekvenserade patienterna hade genen för BCMA slagits ut på båda kromosomkopiorna, ofta genom direkt deletion. Ungefär en tredjedel hade liknande dubbelträffar som påverkade GPRC5D, vanligtvis genom en kombination av deletioner och små skadliga mutationer. Vissa patienter förlorade även CD38. Nästan en tredjedel av den analyserade gruppen hade förlorat både BCMA och GPRC5D, vilket innebär att de inte längre visade de mål som krävs för att flera av dagens mest kraftfulla terapier ska fungera.
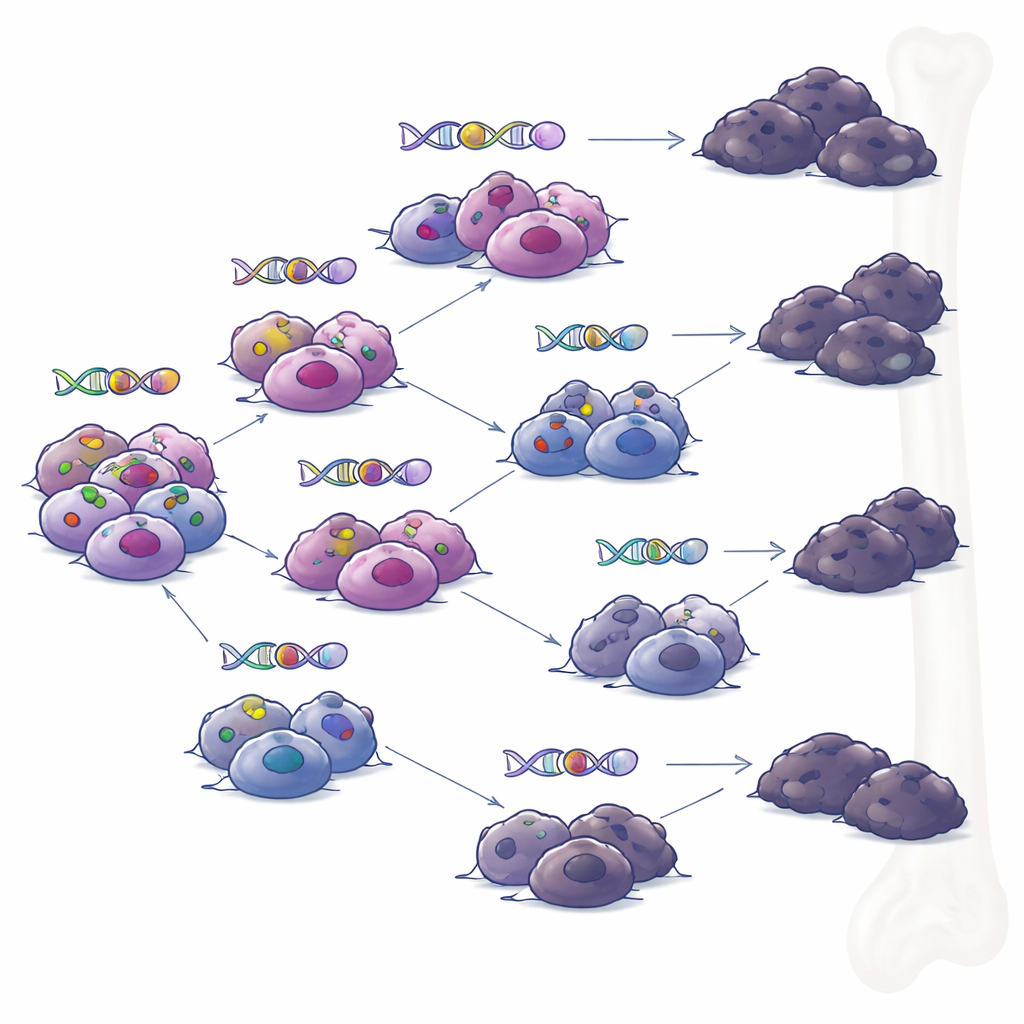
Förgrenade vägar snarare än en enda syndabocksklon
När teamet undersökte prover tagna från samma patienter vid olika tidpunkter rekonstruerade de tumörernas familjeträd. Istället för en enda dominerande klon som stadigt ackumulerade förändringar såg de förgrenad utveckling: flera besläktade undergrupper av celler som skilde sig åt och förvärvade olika uppsättningar mutationer över tiden. Under trycket från riktade immunterapier utvecklade flera grenar oberoende sätt att förlora BCMA eller GPRC5D. Detta mönster tyder på att även när behandling till synes ger en djup remission kan små foci av genetiskt olika celler kvarstå och senare utlösa återfall, var och en med sin egen kombination av resistensmekanismer.
Användning av djupare tester för att styra andra chanser
Där gensekvensering bara fångar DNA använde forskarna också immunohistokemi, en färgningsmetod som visar om BCMA‑proteinet faktiskt finns på tumörcellerna. Varje tumör med båda BCMA‑genkopiorna förlorade visade komplett förlust av BCMA‑protein, men vissa tumörer utan uppenbara genskador hade ändå lite eller inget BCMA på ytan, vilket tyder på ytterligare, mer subtila resistensmekanismer. Avgörande var att i en liten grupp patienter som tidigare fått BCMA‑riktad behandling svarade de vars tumörer fortfarande bar BCMA‑genen och visade åtminstone en del BCMA‑protein ofta igen när de återbehandlades med en annan BCMA‑inriktad CAR T‑cellsbehandling. I kontrast drog patienter vars tumörer helt förlorat BCMA ingen nytta av sådan återbehandling.
Vad detta betyder för patienter och framtida vård
För personer som lever med myelom betonar denna studie både ett dyster och ett hoppfullt budskap. Å ena sidan kan vissa tumörer utvecklas till ett mycket läkemedelsresistent tillstånd genom att systematiskt kasta bort de markörer som avancerade immunterapier är beroende av. Å andra sidan kan detaljerad provtagning av tumörens DNA och proteinmarkörer avslöja vilka mål som finns kvar och hjälpa till att undvika uttömmande, biverkningsfyllda behandlingar när ett mål är förlorat. Författarna argumenterar för att kombinera bred genomisk analys med färgningsbaserade tester bör bli en del av vården för patienter med mycket avancerat myelom. Sådana angreppssätt skulle bättre kunna matcha människor med återbehandlingsstrategier som fortfarande har en chans att fungera, samtidigt som de vägleder sökandet efter nya terapier som inte är beroende av ett enda, lätt förlorat mål.
Citering: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Nyckelord: multipelt myelom, behandlingsresistens, immunterapi, antigenförlust, genomisk profilering