Clear Sky Science · fr
L’évolution vers le myélome hepta‑réfractaire implique une perte séquentielle de CD38, BCMA et GPRC5D
Lorsque le cancer devance même les médicaments les plus récents
Le myélome multiple, un cancer des cellules plasmatiques de la moelle osseuse, a bénéficié d’une vague de nouveaux médicaments, y compris des traitements immunitaires sophistiqués. Pourtant, certains patients atteignent désormais un stade où leur maladie a échappé à tous les grands types de médicaments disponibles. Cette étude examine de près ce stade terminal — appelé « myélome hepta‑réfractaire » — pour comprendre comment le cancer évolue afin d’échapper à tant de thérapies et pour explorer comment les médecins pourraient encore trouver des options utiles.
Un nouveau stade extrême du myélome
Les chercheurs définissent le myélome hepta‑réfractaire comme une maladie qui ne répond plus à sept catégories de traitement clés : deux types de médicaments immunomodulateurs, deux types d’inhibiteurs du protéasome, un anticorps ciblant un marqueur de surface nommé CD38, et deux immunothérapies plus récentes visant des cibles connues sous les noms de BCMA et GPRC5D. Dans un groupe de 37 patients traités dans plusieurs centres, la survie était mauvaise malgré des soins intensifs. Après avoir atteint ce stade, les patients vivaient en moyenne environ 13 mois, et chaque nouvelle ligne de traitement de « sauvetage » contrôlait la maladie seulement pendant environ trois mois. Pourtant, les résultats variaient : quelques individus s’en sortaient nettement mieux, suggérant que la biologie sous‑jacente n’est pas la même dans tous les cas.
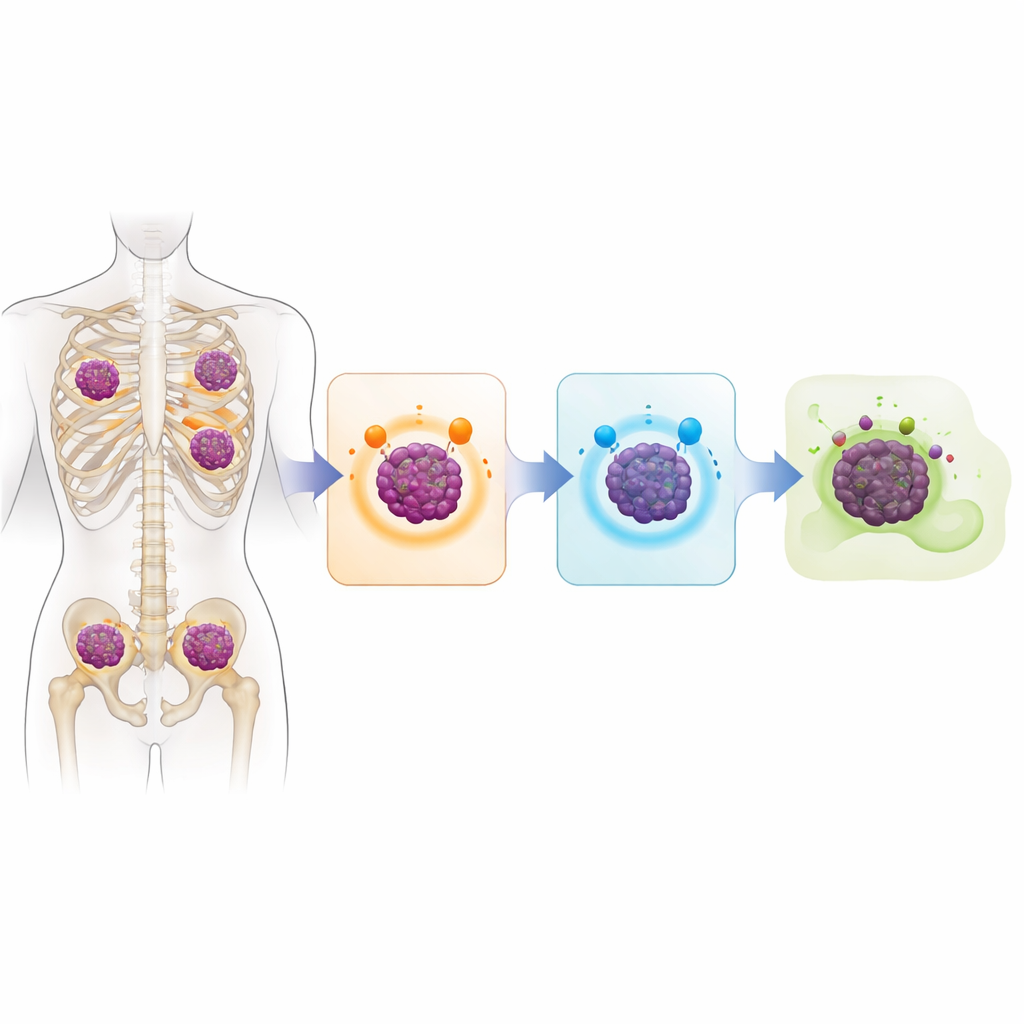
Un génome tumoral rempli de signaux d’alerte
Pour déterminer ce qui distinguait ces cancers, l’équipe a utilisé le séquençage du génome entier, une technique qui lit essentiellement tout l’ADN d’une tumeur. Chez 17 patients avec des échantillons disponibles, ils ont trouvé des génomes fortement endommagés et réarrangés avec de nombreux coups portés à des gènes de sauvegarde classiques qui limitent normalement la croissance cellulaire ou déclenchent la mort cellulaire. Les zones problématiques fréquentes incluaient TP53 et CDKN2C, parmi d’autres souvent associées à des formes particulièrement agressives. Beaucoup de ces altérations sévères apparaissaient dans des tumeurs qui s’étaient étendues hors de la moelle osseuse vers les tissus mous, concordant avec la progression rapide de la maladie chez les patients. Les profils d’ADN portaient aussi les « cicatrices » caractéristiques de traitements antérieurs — comme des modifications associées au médicament chimiothérapeutique mélphalan — montrant que des années de thérapies avaient façonné l’évolution du cancer.
Comment les cellules tumorales perdent leurs cibles
La question centrale était de savoir comment les cellules myélomateuses deviennent invisibles aux médicaments immunitaires modernes conçus pour reconnaître des molécules spécifiques à la surface cellulaire. L’étude montre que, dans de nombreux cas, les cellules tumorales cessent tout simplement de produire ces molécules. Chez environ 40 % des patients séquencés, le gène codant BCMA était inactivé sur les deux copies chromosomiques, souvent par une délétion pure et simple. Environ un tiers présentaient des atteintes doubles similaires concernant GPRC5D, généralement via un mélange de délétions et de petites mutations dommageables. Certains patients perdaient aussi CD38. Près d’un tiers du groupe analysé avait perdu à la fois BCMA et GPRC5D, ce qui signifie qu’ils n’exprimaient plus les cibles nécessaires au fonctionnement de plusieurs des thérapies les plus puissantes d’aujourd’hui.
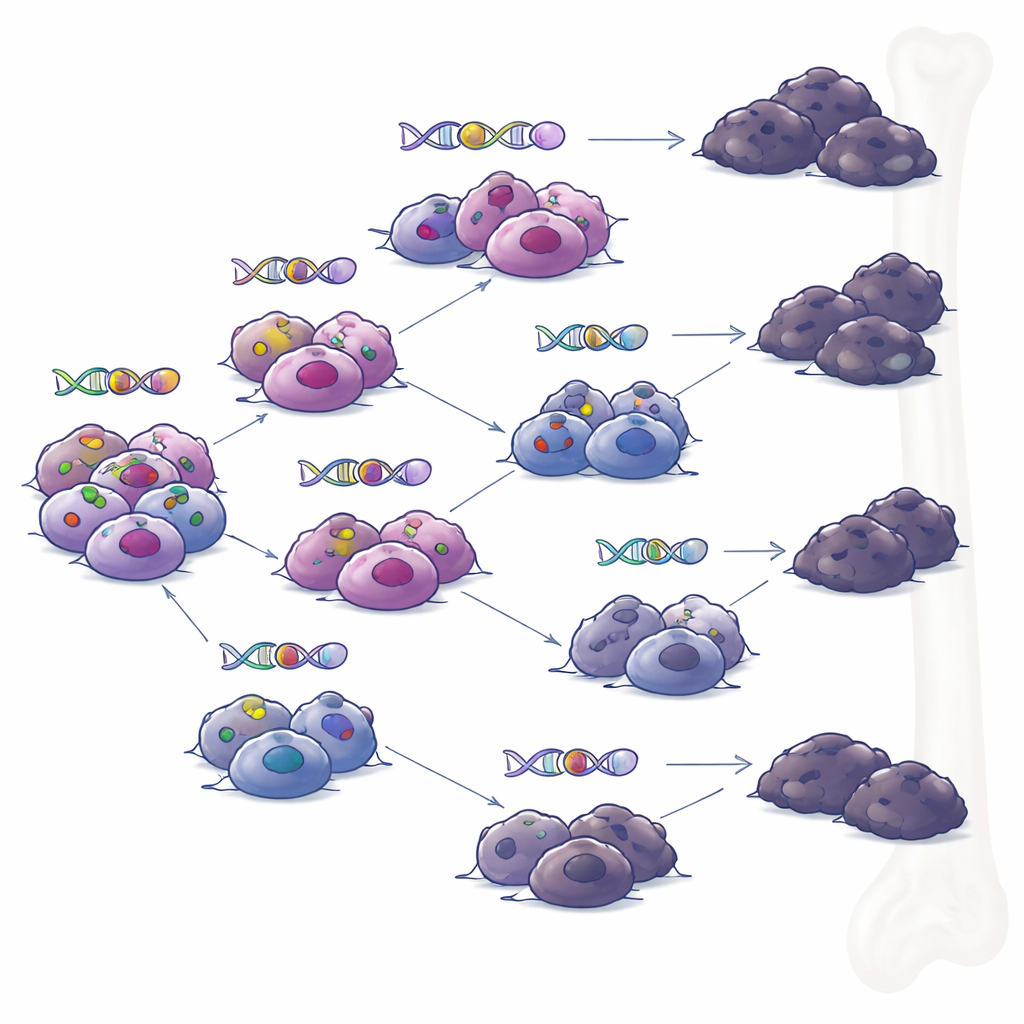
Des trajectoires divergentes plutôt qu’un clone unique et dominant
Lorsque l’équipe a examiné des échantillons prélevés chez les mêmes patients à des moments différents, ils ont reconstitué les arbres généalogiques des tumeurs. Plutôt que de voir un clone unique et dominant accumuler progressivement les altérations, ils ont observé une évolution en branches : plusieurs sous‑groupes cellulaires apparentés ont divergé et acquis différents ensembles de mutations au fil du temps. Sous la pression des immunothérapies ciblées, de multiples branches ont développé indépendamment des moyens de perdre BCMA ou GPRC5D. Ce schéma suggère que même lorsqu’un traitement semble provoquer une rémission profonde, de petites poches de cellules génétiquement diverses peuvent persister et ultérieurement provoquer une rechute, chacune avec sa propre combinaison de mécanismes de résistance.
Utiliser des tests plus approfondis pour guider de nouvelles chances
Parce que le séquençage ne capture que l’ADN, les chercheurs ont également utilisé l’immunohistochimie, une méthode de coloration qui montre si la protéine BCMA est effectivement présente à la surface des cellules tumorales. Chaque tumeur ayant perdu les deux copies du gène BCMA montrait une perte complète de la protéine BCMA, mais certaines tumeurs sans altération génique évidente présentaient aussi peu ou pas de BCMA à leur surface, impliquant des mécanismes de résistance supplémentaires et plus subtils. Surtout, dans un petit sous‑groupe de patients ayant déjà reçu un traitement ciblant BCMA, ceux dont les tumeurs conservaient le gène BCMA et montraient au moins un peu de protéine BCMA ont souvent répondu de nouveau lorsqu’ils ont été retraités par une autre thérapie CAR T dirigée contre BCMA. En revanche, les patients dont les tumeurs avaient perdu complètement BCMA n’ont pas tiré bénéfice d’un tel retraitement.
Ce que cela signifie pour les patients et les soins futurs
Pour les personnes vivant avec un myélome, cette étude souligne à la fois un message sobre et un message porteur d’espoir. D’une part, certaines tumeurs peuvent évoluer vers un état hautement résistant aux médicaments en se débarrassant systématiquement des marqueurs sur lesquels reposent les immunothérapies avancées. D’autre part, des tests détaillés de l’ADN tumoral et des marqueurs protéiques peuvent révéler quelles cibles restent présentes et aider à éviter des traitements vains et chargés d’effets indésirables lorsque une cible a disparu. Les auteurs plaident pour que l’analyse génomique large combinée à des tests basés sur la coloration devienne partie intégrante de la prise en charge des patients présentant un myélome très avancé. De telles approches pourraient mieux assortir les patients à des stratégies de retraitement qui ont encore une chance de fonctionner, tout en orientant la recherche de nouvelles thérapies qui ne dépendent pas d’une cible unique facilement perdue.
Citation: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Mots-clés: myélome multiple, résistance aux traitements, immunothérapie, perte d’antigène, profilage génomique