Clear Sky Science · ar
تطوّر المايلوما المقاوِمة حتى المرحلة السبع-مقاومة ينطوي على خسارة متسلسلة لـ CD38 وBCMA وGPRC5D
عندما يتفوق السرطان حتى على أحدث الأدوية
المايلوما المتعددة، وهو سرطان يصيب الخلايا البلازمية في نخاع العظم، استفادت من موجة من الأدوية الجديدة، بما في ذلك علاجات مناعية متقدمة. ومع ذلك، يصل بعض المرضى الآن إلى مرحلة حيث يتهرب مرضهم من كل أنواع الأدوية الرئيسية المتاحة. تدرس هذه الدراسة عن كثب تلك المرحلة النهائية — المسماة «المايلوما السبع-مقاومة» — لفهم كيف يتطور السرطان ليتفادى هذا الكم من العلاجات وللبحث في كيفية أن يظل لدى الأطباء خيارات مفيدة.
مرحلة جديدة متطرفة من المايلوما
يعرّف الباحثون المايلوما السبع-مقاومة بأنها حالة لا تستجيب بعد الآن لسبع فئات علاجية رئيسية: نوعان من الحبوب المعدلة للمناعة، ونوعان من مثبطات البروتيازوم، وجسم مضاد ضد علامة سطحية تسمى CD38، واثنتان من العلاجات المناعية الأحدث الموجهة إلى أهداف تُعرف باسم BCMA وGPRC5D. في مجموعة مؤلفة من 37 مريضاً تم علاجهم في مراكز متعددة، كانت النجاة ضعيفة رغم الرعاية المكثفة. بعد الوصول إلى هذه المرحلة، عاش المرضى عادة نحو 13 شهراً في المتوسط، وكانت كل دورة جديدة من علاجات «الإنقاذ» تبقي المرض تحت السيطرة نحو ثلاثة أشهر فقط تقريباً. ومع ذلك، تفاوتت النتائج: بعض الأفراد أدوا أداءً أفضل بصورة ملحوظة، مشيراً إلى أن الأحياء البيولوجية الأساسية ليست متطابقة في كل الحالات.
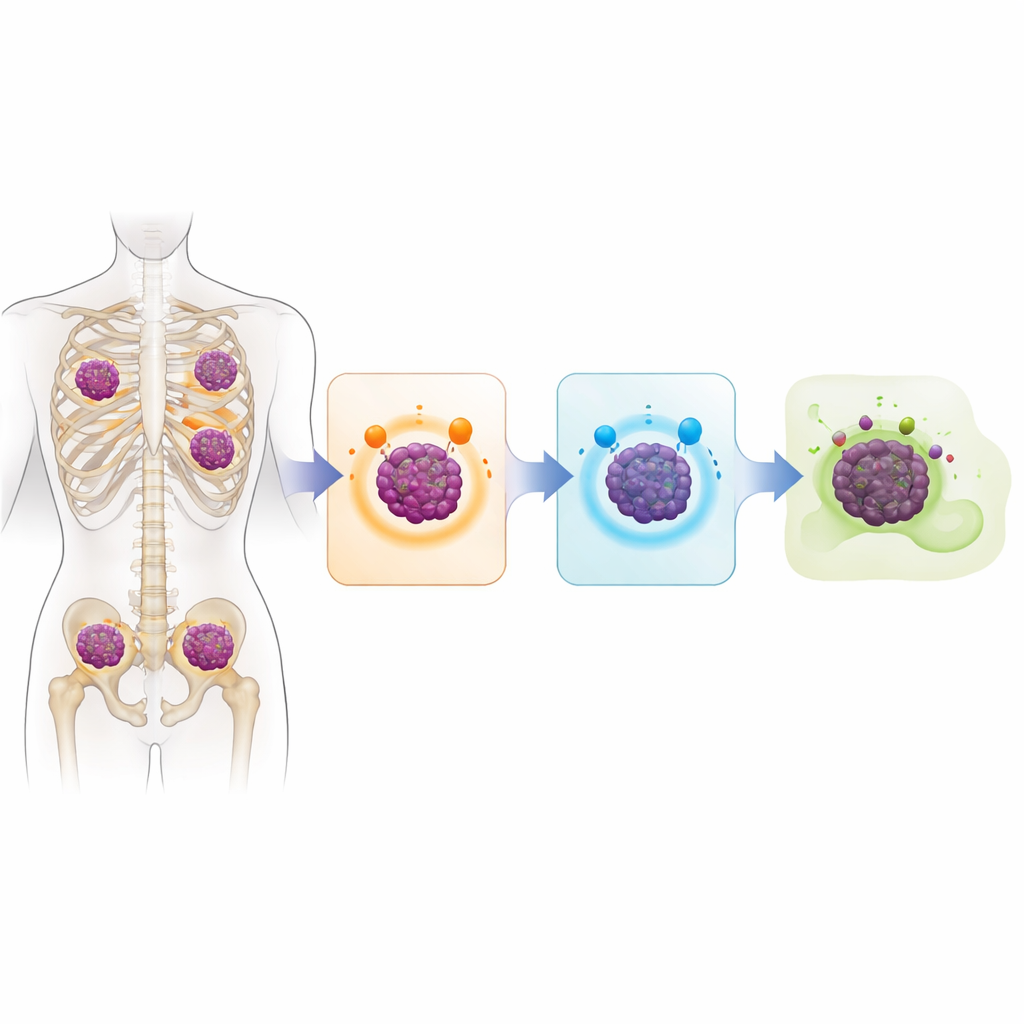
جِنوم سرطاني مليء بعلامات التحذير
لفهم ما يميز هذه الأورام، استخدم الفريق تسلسل الجينوم الكامل، وهي تقنية تقرأ تقريباً كامل حمض نووي الورم. في 17 مريضاً توافرت لهم عينات، وجدوا جينومات متضررة ومُعاد تركيبها بشدّة مع إصابات عديدة في جينات الحماية الكلاسيكية التي عادة ما تقيد نمو الخلايا أو تحفز موتها. شملت مناطق المشكلة الشائعة TP53 وCDKN2C، من بين أخرى غالباً ما ترتبط بمرض عدواني بشكل خاص. ظهرت العديد من هذه التغيرات الشديدة في أورام امتدت خارج نخاع العظم إلى الأنسجة الرخوة، متماشية مع مسار المرض السريع لدى المرضى. كما حملت أنماط الحمض النووي «ندوباً» تدل على العلاجات السابقة — مثل تغيرات مرتبطة بعقار الكيمياء العلاجية ميلفالان — مما يبيّن أن سنوات العلاج شكّلت تطور السرطان.
كيف تتخلى الخلايا السرطانية عن أهدافها
السؤال المركزي كان كيف تصبح خلايا المايلوما غير مرئية للأدوية المناعية الحديثة المصممة للتعرف على جزيئات محددة على سطح الخلية. تُظهر الدراسة أن الخلايا الورمية في كثير من الحالات تتوقف ببساطة عن تصنيع هذه الجزيئات. في نحو 40 في المئة من المرضى الذين جرى تسلسل عيناتهم، تُعطّل جينة BCMA في النسختين على كروموسومات الخلية، غالباً عن طريق حذف صريح. وحوالي ثلث المرضى أظهروا إصابات مزدوجة مماثلة تؤثر على GPRC5D، عادة عبر مزيج من الحذوفات وطفرات صغيرة ضارة. فقد بعض المرضى أيضاً CD38. ما يقرب من ثلث المجموعة المحللة فقدت كلّاً من BCMA وGPRC5D، مما يعني أنها لم تعد تعرض الأهداف نفسها المطلوبة لعمل عدة من أقوى العلاجات الحالية.
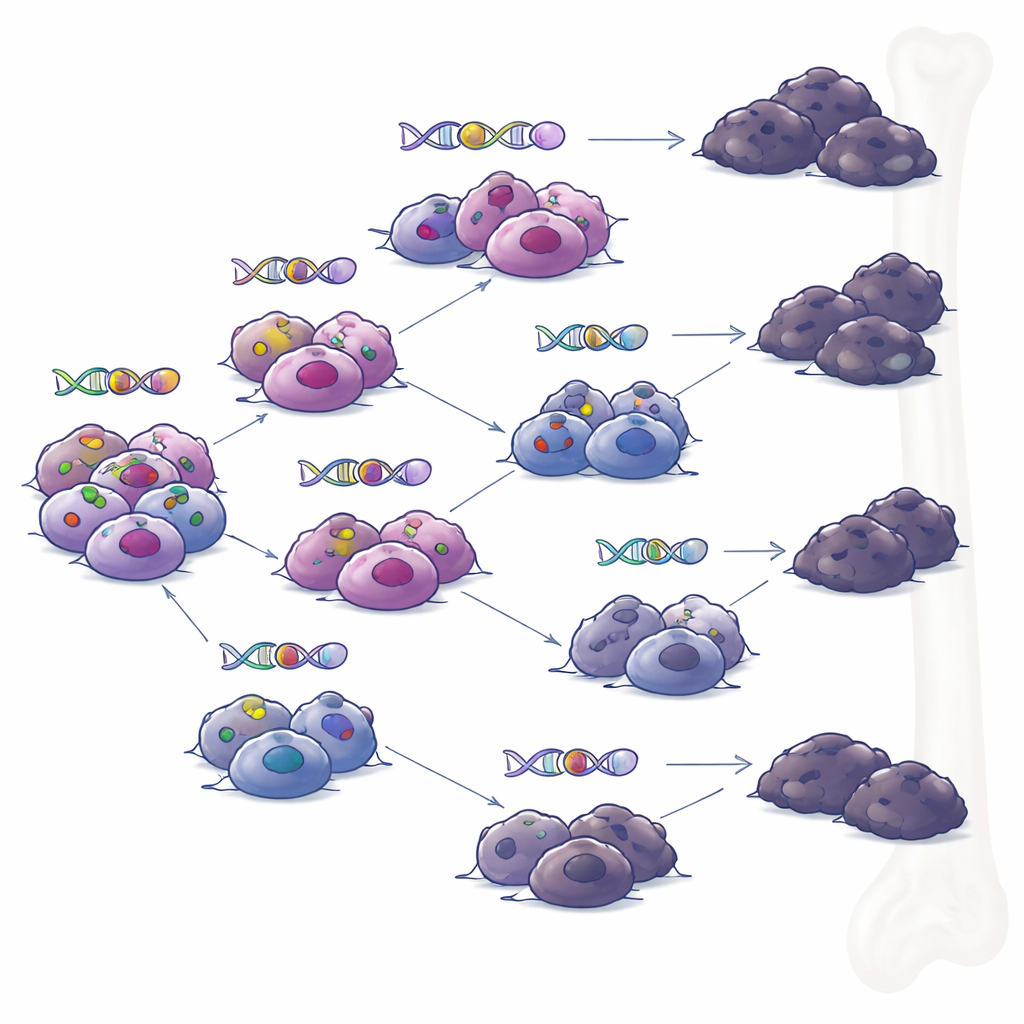
مسارات تفرعية بدلاً من نسخة مارقة واحدة
عند فحص الفريق لعينات مأخوذة من نفس المرضى في أوقات مختلفة، أعادوا بناء أشجار عائلة الأورام. بدلاً من وجود نسخ سائدة واحدة تتراكم عليها التغيرات تدريجياً، رصدوا تطوراً تفريعياً: عدة مجموعات فرعية مرتبطة من الخلايا تباعدت واكتسبت مجموعات مختلفة من الطفرات مع الزمن. تحت ضغط العلاجات المناعية الموجهة، طورت فروع متعددة طرقاً مستقلة لفقدان BCMA أو GPRC5D. يشير هذا النمط إلى أنه حتى عندما يبدو أن العلاج أنتج هدوءاً عميقاً، يمكن لجيوب صغيرة من الخلايا المتنوعة جينياً أن تبقى لاحقاً وتثير الانتكاس، لكلٍ منها مجموعتها الخاصة من حيل المقاومة.
استخدام فحوص أعمق لتوجيه فرص ثانية
لأن تسلسل الجينات يلتقط الحمض النووي فقط، استخدم الباحثون أيضاً الكيمياء النسيجية المناعية، وهي طريقة تلوين تُظهر ما إذا كان بروتين BCMA موجوداً فعلاً على الخلايا الورمية. كل ورم فقد نسختي جين BCMA أظهر فقداناً كاملاً لبروتين BCMA، لكن بعض الأورام التي لم يظهر فيها تلف جيني واضح كان سطحها يحتوي على قليل من BCMA أو لا يحتويه إطلاقاً، مما يوحي بوجود آليات مقاومة إضافية أكثر دقة. والأهم من ذلك، في مجموعة صغيرة من المرضى سبق أن تلقوا علاجات موجهة إلى BCMA، استجاب أولئك الذين كانت أورامهم لا تزال تحمل جين BCMA وتظهر بعض بروتين BCMA عند إعادة علاجهم بخلايا CAR T موجهة إلى BCMA مرة أخرى. بالمقابل، لم يستفد المرضى الذين فقدت أورامهم BCMA بالكامل من مثل هذا الإعادة للعلاج.
ماذا يعني هذا للمرضى والرعاية المستقبلية
بالنسبة للأشخاص الذين يعيشون مع المايلوما، تؤكد هذه الدراسة رسالة مزدوجة مفعمة بالتشاؤم والأمل. من جهة، يمكن لبعض الأورام أن تتطور إلى حالة عالية المقاومة للأدوية عن طريق التخلص المنهجي من العلامات نفسها التي تعتمد عليها العلاجات المناعية المتقدمة. ومن جهة أخرى، يمكن للاختبارات التفصيلية لحمض نووي الورم وعلامات البروتين أن تكشف الأهداف المتبقية وتساعد على تجنب علاجات عديمة الجدوى ومصحوبة بآثار جانبية عندما يختفي الهدف. يجادل المؤلفون أن دمج التحليل الجينومي الواسع مع اختبارات التلوين النسيجي يجب أن يصبح جزءاً من الرعاية للمرضى ذوي المايلوما المتقدمة جداً. قد تساعد مثل هذه النهج في ملاءمة المرضى بشكل أفضل لاستراتيجيات إعادة العلاج التي قد تنجح، مع توجيه البحث نحو علاجات جديدة لا تعتمد على هدف واحد سهل الفقدان.
الاستشهاد: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
الكلمات المفتاحية: المايلوما المتعددة, مقاومة العلاج, العلاج المناعي, فقدان المستضد, التحليل الجينومي