Clear Sky Science · pl
Ewolucja do myeloma hepta-refrakcyjnego obejmuje sekwencyjną utratę CD38, BCMA i GPRC5D
Kiedy nowotwór przechytrza nawet najnowsze leki
Szpiczak mnogi, nowotwór komórek plazmatycznych w szpiku kostnym, skorzystał z fali nowych leków, w tym zaawansowanych terapii wykorzystujących układ odpornościowy. Mimo to niektórzy pacjenci osiągają teraz etap, w którym ich choroba wymyka się przed każdym głównym dostępnym rodzajem leczenia. Badanie to przygląda się dokładnie temu stadium — określanemu jako „hepta‑refrakcyjne” — by zrozumieć, jak rak ewoluuje, by unikać tylu terapii, i by zbadać, jakie opcje nadal mogą być użyteczne dla lekarzy.
Nowe, ekstremalne stadium szpiczaka
Naukowcy definiują myelomę hepta‑refrakcyjną jako chorobę, która nie reaguje już na siedem kluczowych kategorii leczenia: dwa rodzaje doustnych leków modulujących odporność, dwa typy inhibitorów proteasomu, przeciwciało przeciwko markerowi powierzchniowemu o nazwie CD38 oraz dwie nowsze terapie immunologiczne skierowane przeciwko celom znanym jako BCMA i GPRC5D. W grupie 37 takich pacjentów leczonych w kilku ośrodkach przeżycie było słabe pomimo intensywnej opieki. Po osiągnięciu tego stadium chorzy zwykle żyli średnio około 13 miesięcy, a każda kolejna linia terapii „ratunkowej” utrzymywała chorobę w ryzach tylko przez około trzy miesiące. Wyniki jednak się różniły: u kilku osób obserwowano znacznie lepsze przeżycie, co sugeruje, że podłoże biologiczne nie jest identyczne we wszystkich przypadkach.
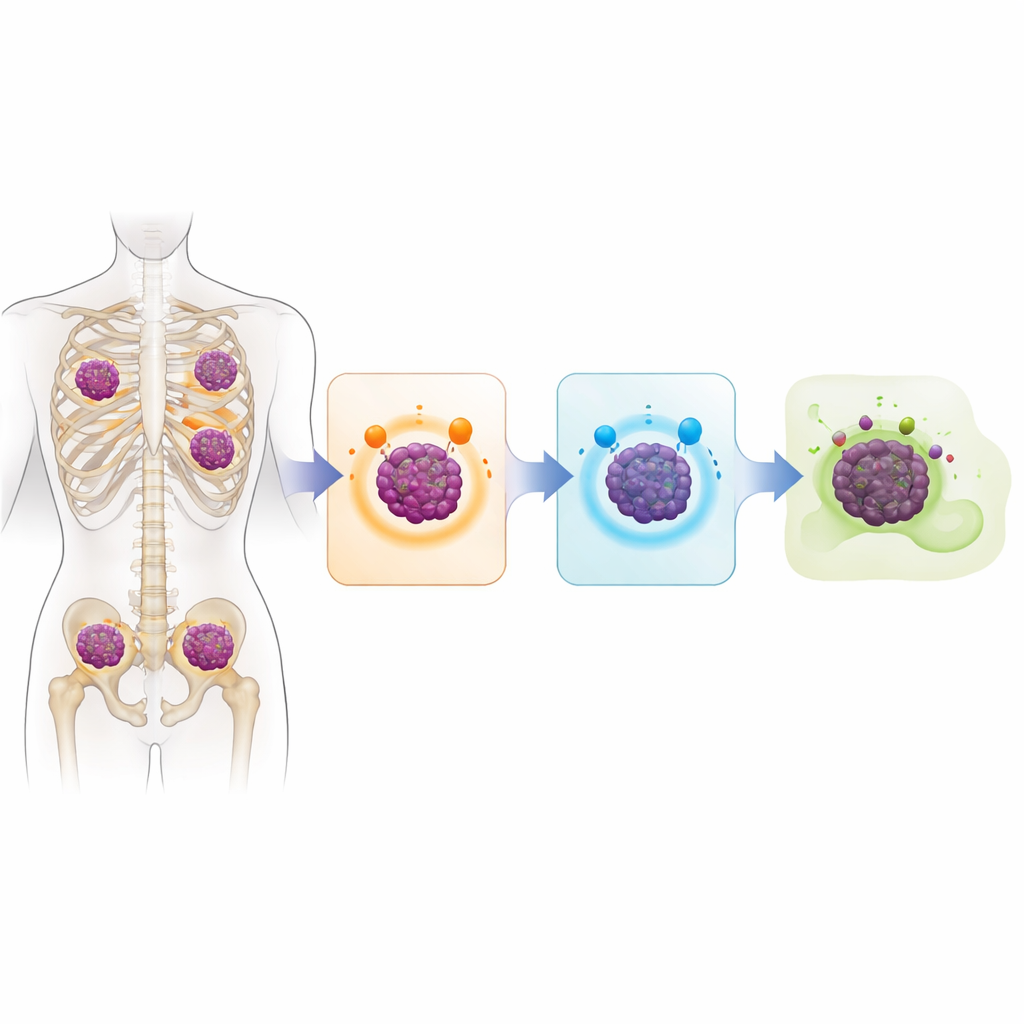
Genom raka pełen ostrzegawczych znaków
Aby zobaczyć, co wyróżnia te nowotwory, zespół zastosował sekwencjonowanie całego genomu — technikę odczytującą praktycznie całe DNA guza. U 17 pacjentów z dostępnymi próbkami stwierdzono silnie uszkodzone i przearanżowane genomy z wieloma uderzeniami w klasyczne geny odpowiedzialne za ochronę, które zwykle hamują wzrost komórek lub uruchamiają apoptozę. Często dotknięte były obszary takie jak TP53 i CDKN2C oraz inne zmiany często powiązane ze szczególnie agresywną chorobą. Wiele z tych ciężkich zmian pojawiało się w guzach, które rozsiewały się poza szpik do tkanek miękkich, co odpowiadało szybkiemu przebiegowi choroby u pacjentów. Wzory DNA nosiły też charakterystyczne „blizny” po wcześniejszych terapiach — na przykład zmiany związane z lekiem chemioterapeutycznym melfalanem — co pokazuje, że lata leczenia ukształtowały ewolucję nowotworu.
Jak komórki nowotworowe pozbywają się swoich celów
Główne pytanie brzmiało, jak komórki myelomu stają się niewidoczne dla nowoczesnych leków opartych na układzie odpornościowym, które są zaprojektowane do rozpoznawania określonych cząsteczek na powierzchni komórki. Badanie pokazuje, że w wielu przypadkach komórki guza po prostu przestają wytwarzać te molekuły. U około 40 procent sekwencjonowanych pacjentów gen kodujący BCMA został wyłączony w obu kopiach chromosomu, często przez bezpośrednią delecję. Około jedna trzecia miała podobne podwójne uszkodzenia dotyczące GPRC5D, zwykle poprzez połączenie delecji i drobnych mutacji szkodliwych. Niektórzy pacjenci utracili też CD38. Niemal jedna trzecia analizowanej grupy straciła jednocześnie BCMA i GPRC5D, co oznacza, że nie prezentowały już celów niezbędnych do działania kilku z najsilniejszych współczesnych terapii.
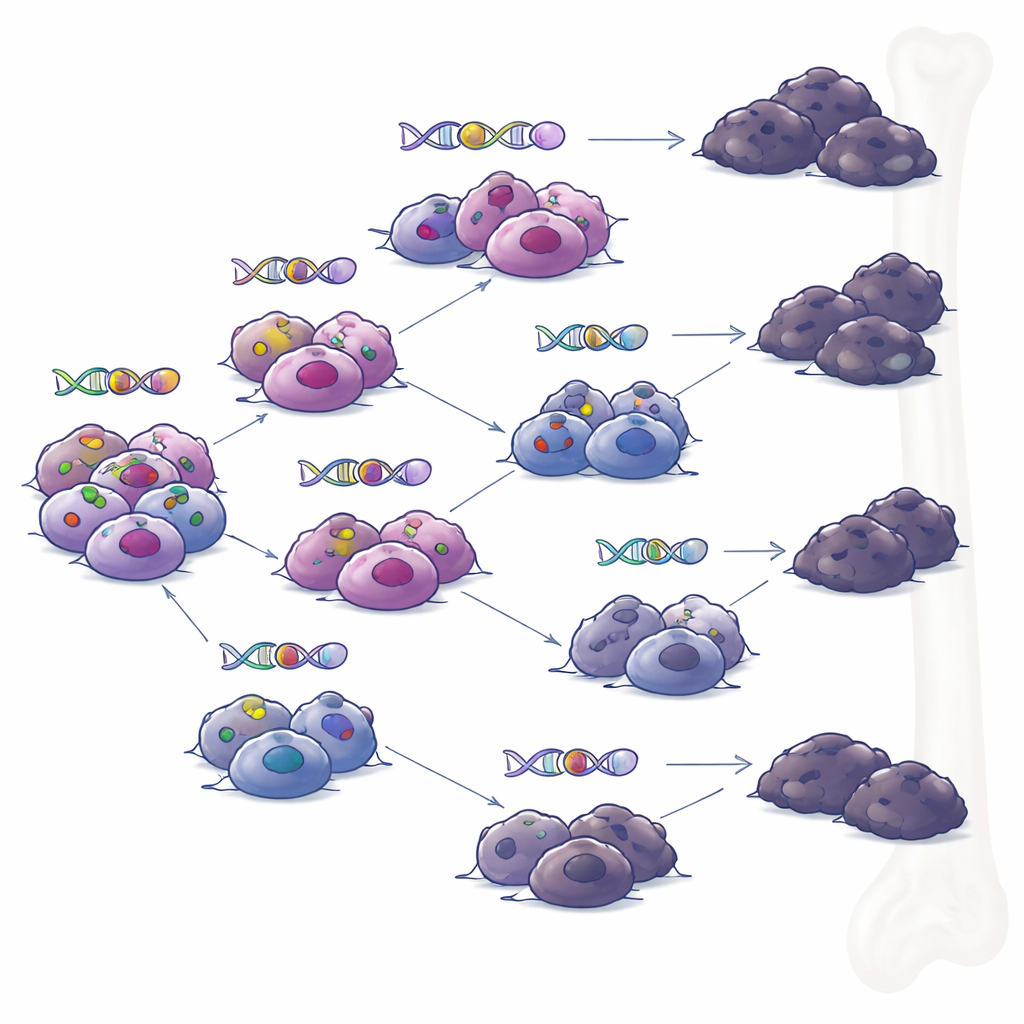
Rozgałęzione ścieżki zamiast jednego zbuntowanego klonu
Gdy zespół przebadał próbki pobrane od tych samych pacjentów w różnych momentach, odtworzył drzewa rodzinne guzów. Zamiast jednego dominującego klonu stopniowo akumulującego zmiany, zaobserwowano ewolucję rozgałęzioną: kilka spokrewnionych podgrup komórek, które rozeszły się w różne strony i nabyły odmienne zestawy mutacji w czasie. Pod presją terapii ukierunkowanych na konkretne cele immunologiczne, wiele gałęzi niezależnie wypracowało sposoby utraty BCMA lub GPRC5D. Ten wzór sugeruje, że nawet gdy terapia wywołuje pozornie głęboką remisję, niewielkie skupiska genetycznie zróżnicowanych komórek mogą przetrwać i później wywołać nawroty, z każdą grupą komórek posiadającą własne kombinacje mechanizmów oporności.
Wykorzystywanie głębszych badań, by prowadzić do drugich szans
Ponieważ sekwencjonowanie genów rejestruje jedynie DNA, badacze użyli również immunohistochemii — metody barwienia, która pokazuje, czy białko BCMA faktycznie występuje na komórkach guza. Każdy guz z utratą obu kopii genu BCMA wykazywał całkowity brak białka BCMA, ale niektóre guzy bez oczywistych uszkodzeń genowych także miały niewiele lub wcale BCMA na powierzchni, co sugeruje dodatkowe, subtelniejsze mechanizmy oporności. Co kluczowe, w niewielkiej grupie pacjentów, którzy wcześniej otrzymali terapię ukierunkowaną na BCMA, ci, których guzy nadal miały gen BCMA i wykazywały przynajmniej częściową ekspresję białka, często ponownie reagowali na powtórne leczenie kolejną terapią CAR T skierowaną przeciw BCMA. Natomiast pacjenci, których guzy całkowicie utraciły BCMA, nie odnosili korzyści z takiego ponownego leczenia.
Co to oznacza dla pacjentów i przyszłej opieki
Dla osób żyjących ze szpiczakiem to badanie niesie zarówno przygnębiający, jak i dający nadzieję przekaz. Z jednej strony niektóre guzy mogą ewoluować do stanu silnej oporności na leki, systematycznie zrzucając markery, na których opierają się zaawansowane terapie immunologiczne. Z drugiej strony szczegółowe badania DNA i markerów białkowych guza mogą ujawnić, które cele pozostały, i pomóc unikać daremnych terapii obarczonych działaniami niepożądanymi, gdy dany cel zniknął. Autorzy argumentują, że łączenie szerokiej analizy genomowej z testami opartymi na barwieniu powinno stać się elementem opieki u pacjentów z bardzo zaawansowanym szpiczakiem. Takie podejście mogłoby lepiej dopasować pacjentów do strategii ponownego leczenia, które wciąż mają szansę zadziałać, jednocześnie ukierunkowując poszukiwania nowych terapii niezależnych od pojedynczego, łatwo utraconego celu.
Cytowanie: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Słowa kluczowe: szpiczak mnogi, oporność na leczenie, immunoterapia, utrata antygenu, profilowanie genomowe