Clear Sky Science · es
La evolución hacia el mieloma hepta‑refractario implica la pérdida secuencial de CD38, BCMA y GPRC5D
Cuando el cáncer supera incluso a los fármacos más nuevos
El mieloma múltiple, un cáncer de las células plasmáticas en la médula ósea, se ha beneficiado de una oleada de medicamentos nuevos, incluidas sofisticadas terapias basadas en el sistema inmunitario. Sin embargo, algunos pacientes alcanzan ahora una fase en la que su enfermedad ha escapado a todos los principales tipos de fármacos disponibles. Este estudio examina de cerca ese estadio final —denominado mieloma “hepta‑refractario”— para entender cómo el cáncer evoluciona para eludir tantas terapias y explorar cómo los médicos podrían todavía encontrar opciones útiles.
Un nuevo estadio extremo del mieloma
Los investigadores definen el mieloma hepta‑refractario como la enfermedad que ya no responde a siete categorías clave de tratamiento: dos tipos de fármacos moduladores del sistema inmunitario, dos clases de inhibidores del proteasoma, un anticuerpo contra un marcador de superficie llamado CD38 y dos terapias inmunitarias más recientes dirigidas a dianas conocidas como BCMA y GPRC5D. En un grupo de 37 pacientes de varios centros, la supervivencia fue baja a pesar de los cuidados intensivos. Tras alcanzar este estadio, los pacientes vivieron por término medio alrededor de 13 meses, y cada nueva línea de terapia de “rescate” mantuvo la enfermedad a raya solo durante aproximadamente tres meses. Aun así, los resultados variaron: algunos individuos lo hicieron notablemente mejor, lo que sugiere que la biología subyacente no es la misma en todos los casos.
Un genoma tumoral lleno de señales de alarma
Para ver qué distinguía a estos cánceres, el equipo utilizó secuenciación del genoma completo, una técnica que lee prácticamente todo el ADN de un tumor. En 17 pacientes con muestras disponibles, encontraron genomas muy dañados y reordenados con numerosos impactos en genes guardianes clásicos que habitualmente restringen el crecimiento celular o desencadenan la muerte celular. Áreas problemáticas comunes incluyeron TP53 y CDKN2C, entre otros relacionados con enfermedad especialmente agresiva. Muchos de estos cambios severos aparecieron en tumores que se habían diseminado fuera de la médula ósea hacia tejidos blandos, lo que encaja con la rápida progresión clínica de los pacientes. Los patrones de ADN también conservaban las señalizaciones características de tratamientos previos —como alteraciones asociadas al fármaco quimioterápico melfalán— lo que muestra que años de terapia han moldeado la evolución del cáncer.
Cómo las células tumorales se desprenden de sus dianas
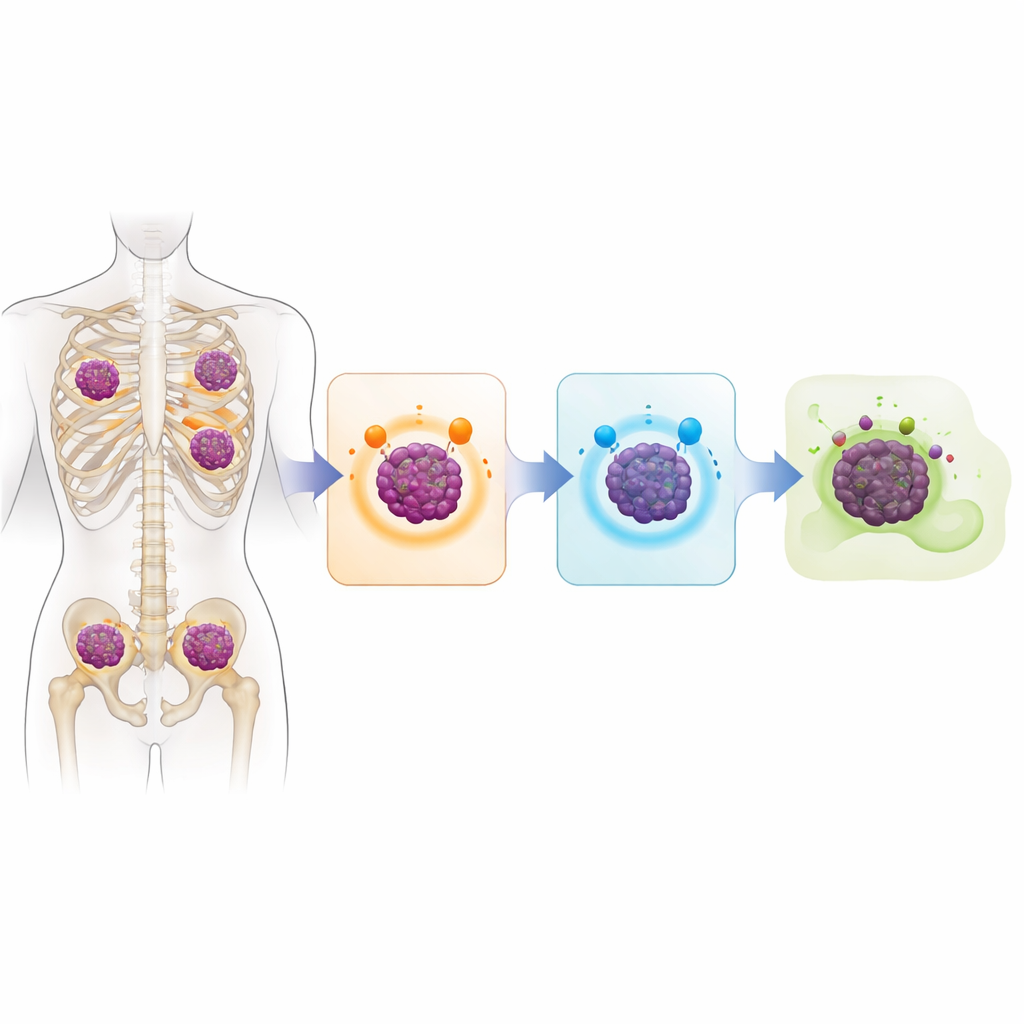
La cuestión central era cómo las células del mieloma se vuelven invisibles a los fármacos inmunitarios modernos, diseñados para reconocer moléculas específicas en la superficie celular. El estudio muestra que, en muchos casos, las células tumorales simplemente dejan de producir esas moléculas. En alrededor del 40% de los pacientes secuenciados, el gen de BCMA quedó inactivado en ambas copias del cromosoma, a menudo por deleciones completas. Aproximadamente un tercio presentó impactos dobles similares que afectaban a GPRC5D, generalmente mediante una mezcla de deleciones y pequeñas mutaciones dañinas. Algunos pacientes también perdieron CD38. Casi un tercio del grupo analizado había perdido tanto BCMA como GPRC5D, lo que significa que ya no mostraban las dianas necesarias para que varias de las terapias más potentes actuales funcionaran.
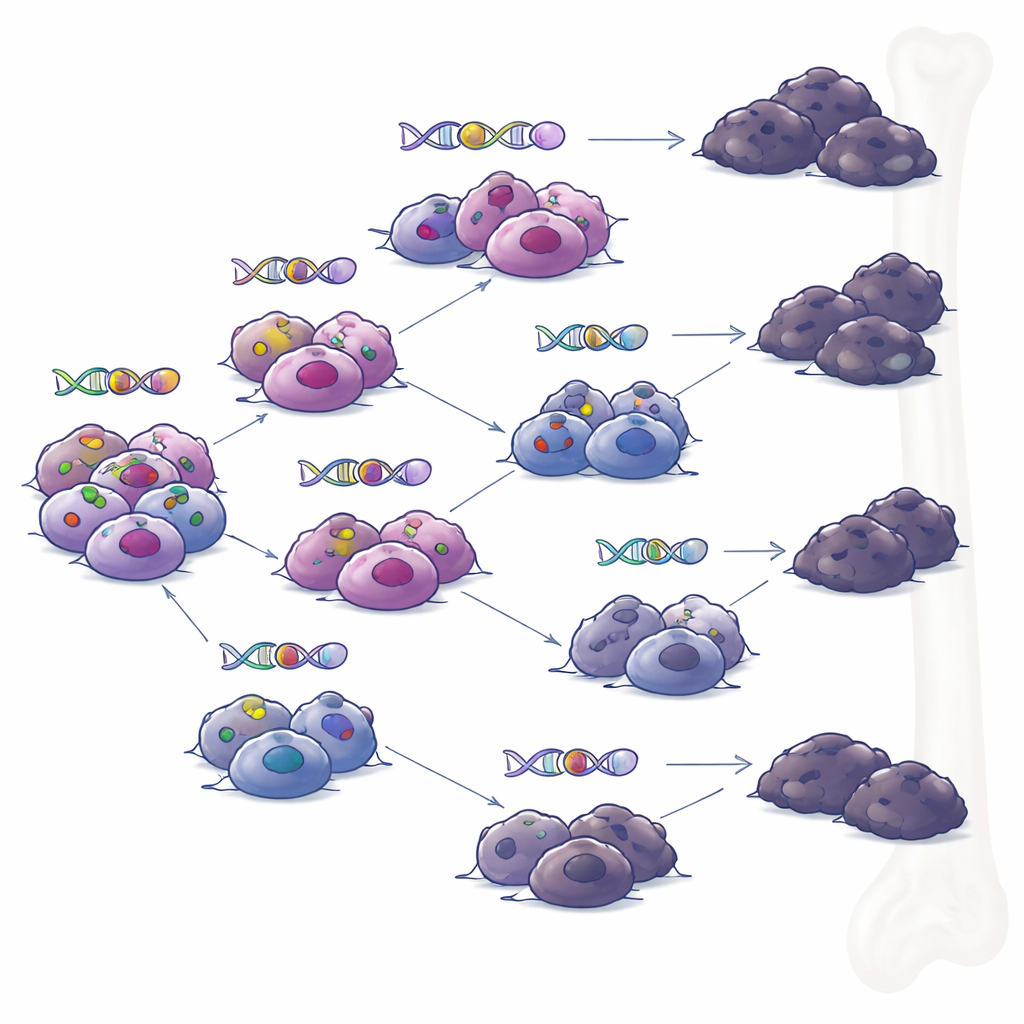
Rutas ramificadas en lugar de un clon único rebelde
Cuando el equipo examinó muestras tomadas de los mismos pacientes en distintos momentos, reconstruyeron los árboles genealógicos de los tumores. En lugar de un clon dominante que acumulara cambios de forma gradual, observaron una evolución ramificada: varios subgrupos relacionados de células que divergieron y adquirieron distintos conjuntos de mutaciones con el tiempo. Bajo la presión de las terapias inmunitarias dirigidas, múltiples ramas desarrollaron de forma independiente maneras de perder BCMA o GPRC5D. Este patrón sugiere que, incluso cuando el tratamiento parece producir una remisión profunda, pequeños focos de células genéticamente diversas pueden persistir y desencadenar más tarde una recaída, cada uno con su propia combinación de trucos de resistencia.
Usar pruebas más profundas para guiar segundas oportunidades
Dado que la secuenciación genética solo captura el ADN, los investigadores también emplearon inmunohistoquímica, un método de tinción que muestra si la proteína BCMA está realmente presente en las células tumorales. Todo tumor con ambas copias del gen BCMA perdidas mostró una ausencia completa de la proteína BCMA, pero algunos tumores sin daño genético evidente también tenían poco o nada de BCMA en su superficie, lo que implica mecanismos de resistencia adicionales y más sutiles. De manera crucial, en un pequeño conjunto de pacientes que habían recibido previamente tratamientos dirigidos a BCMA, aquellos cuyos tumores todavía conservaban el gen BCMA y mostraban al menos algo de proteína BCMA respondieron a menudo de nuevo al ser tratados con otra terapia CAR T dirigida a BCMA. En contraste, los pacientes cuyos tumores habían perdido completamente BCMA no se beneficiaron de ese re‑tratamiento.
Qué significa esto para los pacientes y la atención futura
Para las personas con mieloma, este estudio subraya un mensaje a la vez sombrío y esperanzador. Por un lado, algunos tumores pueden evolucionar hacia un estado de alta resistencia a fármacos al descartarse sistemáticamente los marcadores en los que confían las terapias inmunitarias avanzadas. Por otro, las pruebas detalladas del ADN tumoral y de los marcadores proteicos pueden revelar qué dianas permanecen y ayudar a evitar tratamientos fútiles y con efectos secundarios cuando una diana ha desaparecido. Los autores sostienen que combinar un análisis genómico amplio con pruebas basadas en tinción debería integrarse en la atención de pacientes con mieloma muy avanzado. Tales enfoques podrían emparejar mejor a las personas con estrategias de re‑tratamiento que aún tengan posibilidades de funcionar, a la vez que orientan la búsqueda de nuevas terapias que no dependan de una diana única y fácilmente perdible.
Cita: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Palabras clave: mieloma múltiple, resistencia al tratamiento, inmunoterapia, pérdida de antígenos, perfilado genómico