Clear Sky Science · nl
De evolutie naar hepta-refractair myeloom omvat achtereenvolgend verlies van CD38, BCMA en GPRC5D
Wanneer kanker zelfs de nieuwste medicijnen te slim af is
Multipel myeloom, een kanker van plasmacellen in het beenmerg, heeft geprofiteerd van een reeks nieuwe geneesmiddelen, waaronder geavanceerde immuun-gebaseerde behandelingen. Toch bereiken sommige patiënten nu een stadium waarin hun ziekte aan elk belangrijk beschikbaar medicijntype ontsnapt is. Deze studie bekijkt dat eindstadium — aangeduid als “hepta-refractair” myeloom — om te begrijpen hoe de kanker zich ontwikkelt om zo veel therapieën te ontwijken en om te onderzoeken welke opties artsen mogelijk nog nuttig kunnen vinden.
Een nieuw extreem stadium van myeloom
De onderzoekers definiëren hepta-refractair myeloom als ziekte die niet meer reageert op zeven kerncategorieën van behandeling: twee soorten immuunmodulerende tabletten, twee typen proteasoomremmers, een antilichaam tegen een oppervlakte-eiwit genaamd CD38, en twee nieuwere immuuntherapieën gericht op doelen die bekendstaan als BCMA en GPRC5D. In een groep van 37 dergelijke patiënten behandeld in meerdere centra was de overleving slecht ondanks intensieve zorg. Na het bereiken van dit stadium leefden patiënten gemiddeld ongeveer 13 maanden, en elke nieuwe lijn van ‘salvage’-therapie hield de ziekte slechts ongeveer drie maanden in toom. Toch verschilden de uitkomsten: een paar individuen deden het duidelijk beter, wat suggereert dat de onderliggende biologie niet voor iedereen hetzelfde is.
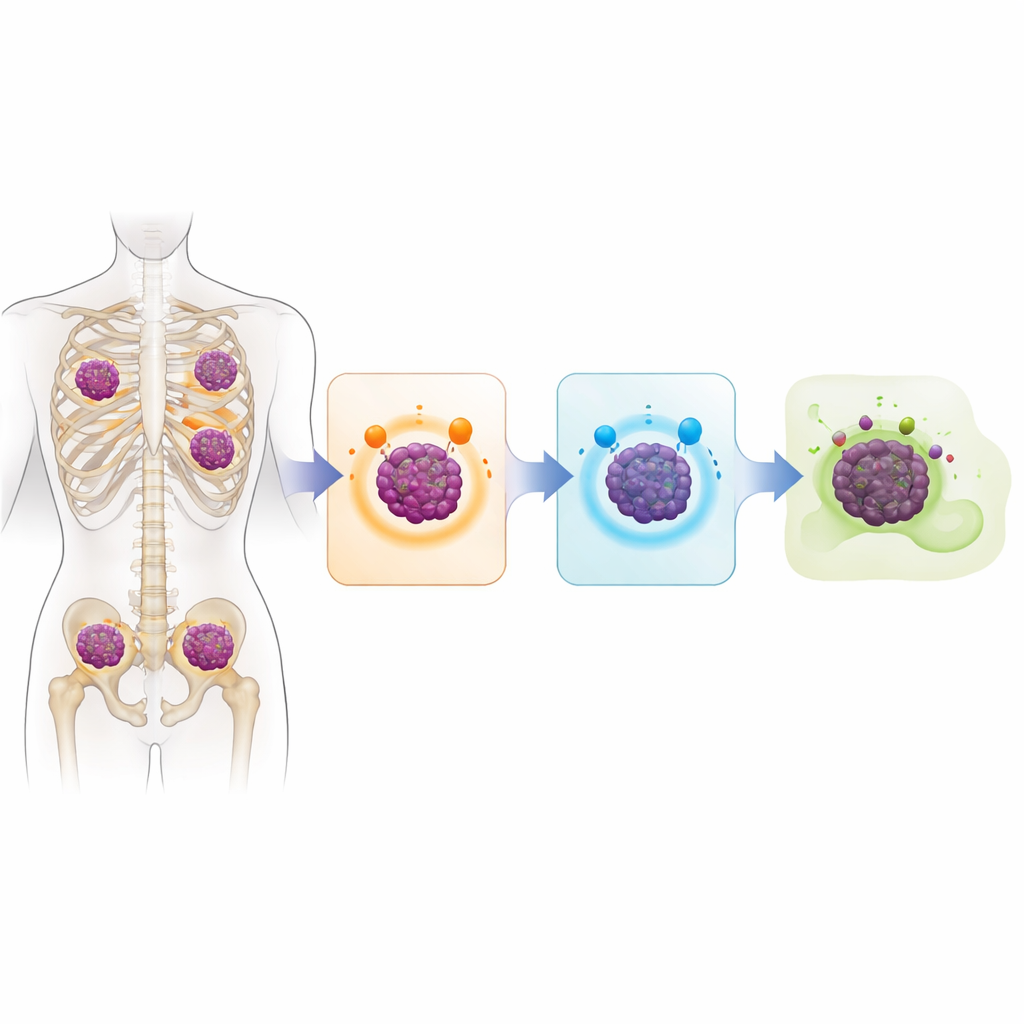
Een kankergenoom vol waarschuwingssignalen
Om te zien wat deze kankers onderscheidde, gebruikte het team gehele-genoomsequencing, een techniek die vrijwel al het DNA van een tumor uitleest. Bij 17 patiënten met beschikbare monsters vonden ze zwaar beschadigde en herschikte genomen met veel treffers in klassieke waakhondgenen die normaal gesproken de celgroei remmen of celdood activeren. Veelvoorkomende probleemgebieden waren onder meer TP53 en CDKN2C, naast andere genen die vaak geassocieerd zijn met bijzonder agressieve ziekte. Veel van deze ernstige veranderingen kwamen voor in tumoren die buiten het beenmerg naar zacht weefsel waren uitgezaaid, wat overeenkomt met het snel voortschrijdende ziektebeeld van de patiënten. De DNA-patronen droegen ook kenmerkende “littekens” van eerdere behandelingen — zoals veranderingen geassocieerd met het chemotherapeuticum melphalan — wat laat zien dat jaren van therapie de evolutie van de kanker hebben gevormd.
Hoe tumorcellen hun doelwitten afwerpen
De centrale vraag was hoe myeloomcellen onzichtbaar worden voor moderne immuun-gebaseerde geneesmiddelen die ontworpen zijn om specifieke moleculen op het celoppervlak te herkennen. De studie toont aan dat tumoren in veel gevallen simpelweg stoppen met het maken van deze moleculen. In ongeveer 40 procent van de gesequenced patiënten was het gen voor BCMA op beide chromosoomkopieën uitgeschakeld, vaak door een volledige deletie. Ongeveer een derde had vergelijkbare dubbele treffers die GPRC5D troffen, meestal door een mix van deleties en kleine schadelijke mutaties. Sommige patiënten verloren ook CD38. Bij bijna een derde van de geanalyseerde groep waren zowel BCMA als GPRC5D verdwenen, wat betekende dat ze de doelen niet langer toonden die nodig zijn voor een aantal van de krachtigste therapieën van vandaag de dag.
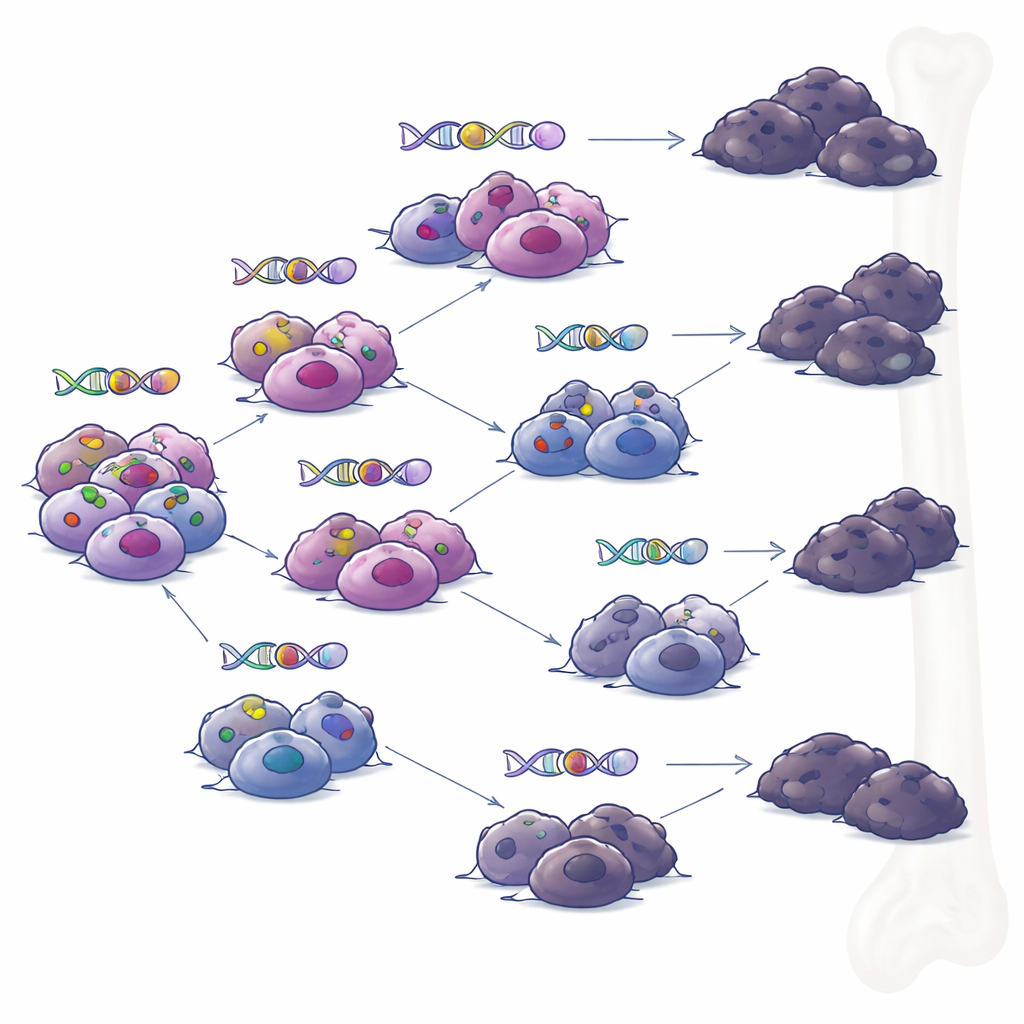
Vertakkende paden in plaats van één uit de toon vallende kloon
Toen het team monsters onderzocht die op verschillende tijdstippen van dezelfde patiënten waren genomen, reconstruerden ze de familiestambomen van de tumoren. In plaats van één dominante kloon die geleidelijk veranderingen ophoopt, zagen ze vertakkende evolutie: meerdere verwante subgroepen van cellen die uiteenwaaierden en in de loop van de tijd verschillende sets mutaties verwierven. Onder druk van gerichte immuuntherapieën ontwikkelden meerdere takken onafhankelijk manieren om BCMA of GPRC5D te verliezen. Dit patroon suggereert dat zelfs wanneer behandeling lijkt te leiden tot een diepe remissie, kleine pockets van genetisch diverse cellen kunnen blijven bestaan en later een terugval kunnen veroorzaken, elk met hun eigen combinatie van resistentiemechanismen.
Diepere tests gebruiken om herkansingen te sturen
Aangezien genensequencing alleen DNA vastlegt, gebruikten de onderzoekers ook immunohistochemie, een kleuringstechniek die laat zien of het BCMA-eiwit daadwerkelijk aanwezig is op tumorcellen. Elke tumor met verlies van beide BCMA-genkopieën toonde volledig verlies van BCMA-eiwit, maar sommige tumoren zonder duidelijke gendefecten hadden ook weinig of geen BCMA op hun oppervlak, wat duidt op aanvullende, subtielere resistentiemechanismen. Cruciaal is dat in een kleine groep patiënten die eerder BCMA-gerichte behandeling hadden gekregen, degenen van wie de tumoren het BCMA-gen nog droegen en ten minste enige BCMA-eiwitexpressie toonden, vaak weer reageerden toen ze opnieuw werden behandeld met een andere BCMA-gerichte CAR-T-celtherapie. Daarentegen hadden patiënten wiens tumoren volledig BCMA hadden verloren geen baat bij zo’n herbehandeling.
Wat dit betekent voor patiënten en toekomstige zorg
Voor mensen die met myeloom leven, benadrukt deze studie zowel een somber als een hoopvol bericht. Aan de ene kant kunnen sommige tumoren zich ontwikkelen tot een zeer medicijnresistent stadium door systematisch de markers te verwijderen waarop geavanceerde immuuntherapieën vertrouwen. Aan de andere kant kunnen gedetailleerde tests van tumor-DNA en proteïnemarkers onthullen welke doelen nog aanwezig zijn en helpen zinloze behandelingen met bijwerkingen vermijden wanneer een doel verdwenen is. De auteurs pleiten ervoor dat het combineren van brede genomische analyse met kleuringgebaseerde tests onderdeel zou moeten worden van de zorg voor patiënten met zeer gevorderd myeloom. Dergelijke benaderingen zouden mensen beter kunnen koppelen aan herbehandelingsstrategieën die nog een kans van slagen hebben, terwijl ze ook de zoektocht naar nieuwe therapieën sturen die niet afhankelijk zijn van één, makkelijk te verliezen doelwit.
Bronvermelding: Riedhammer, C., Truger, M., Lee, H. et al. The evolution to hepta-refractory myeloma involves sequential loss of CD38, BCMA and GPRC5D. Leukemia 40, 730–738 (2026). https://doi.org/10.1038/s41375-026-02889-3
Trefwoorden: multipel myeloom, behandelingsresistentie, immunotherapie, antigeenverlies, genomische profilering